Типы кристаллических решеток
Конденсированное состояние вещества
Жидкости
Строение жидкой воды
Жидкие кристаллы
Любое вещество может находиться в одном из четырех агрегатных состояниях: твердом, жидком, газообразном или в виде плазмы. При низких температурах и(или) высоких давлениях все вещества находятся в твердом состоянии. Твердое и жидкое состояние вещества называют конденсированным состоянием.
Жидкости характеризуются компактным расположением частиц, что вызывает малую их сжимаемость по сравнению с газами. Частицы в жидкости образуют лабильные упорядоченные агрегаты ("ближний порядок"), разделенные областями беспорядоченого расположения частиц. Агрегаты частиц не имеют резких границ: перемещаясь в жидкости, они теряют одни частицы и приобретают другие, могут полностью разрушиться и возникнуть вновь. При понижении температуры агрегаты частиц увеличиваются и размерах, приобретают большую стабильность и упорядоченность в расположении частиц. Вблизи температуры кристаллизации агрегаты превращаются в зародыши кристаллизации твердой фазы.
Жидкости отличаются от твердой фазы большей подвижностью частиц, текучестью и изотропностью, то есть одинаковостью физических свойств по различным направлениям. Между частицами жидкости существуют равномерно распределенные по объему и перемещающиеся пустоты с размрами, сопоставимыми с размерами частиц.
Жидкости присущ определенный объем. Она стремиться принять макую форму, которая способствовала бы минимальной площади ее поверхности, так как для увеличения поверхности жидкости требуется дополнительная энергия, которая определяется поверхностным натяжением. Поверхностное натяжение возникает из-за неуравновешенности межмолекулярных сил, действующих у поверхности жидкости. Оно минимально, когда жидкость принимает сферическую форму.
Строение жидкой воды
Наличие водородных связей в воде вызывает появление ряда характерных свойств. Прежде всего, ассоциация молекул воды ведет к повышению температур плавления и кипения по сравнению со значениями, ожидаемыми из сравнения соответствующих величин для других халькогеноводородов. Увеличение полярности агрегатов молекул воды проявляется также в повышении диэлектрической проницаемости. Для воды при 25 oС она равна 78,5. Свойства жидкой воды как растворителя и сольватирующего агента также в значительной мере определяется способностью ее молекул выступать донором или акцептором при образовании водородных связей.
Способность к образованию водородных мостиков у воды выражена особенно сильно благодаря тому, что в каждой молекуле имеются два атома водорода и две неподеленные электронные пары, которые могут быть акцепторами атомов водорода. В жидкой воде находятся в динамическом равновесии молекулярные ассоциаты, содержащие до 100 молекул воды, представляющие собой осколки структуры льда. На основе анализа кривых радиального распределения электронной плотности, полученных методом рентгеноструктурного анализа, был сделан вывод, что ближайшее окружение каждой молекулы воды состоит из четырех-пяти молекул, образующих первую гидратную оболочку, что отражается в наличии максимума на кривой радиального распределения. На больших расстояниях обнаруживаются другие максимумы, соответствующие более удаленным гидратным оболочкам.
Отдельные молекулы воды могут путем быстрого обмена (~10-11 с) присоединяться к ассоциату или отщепляться от него. В этих агрегатах (кластерах) имеют не только тетраэдрические (как в твердой воде), но и нетерадрические (изогнутые) водородные мостики, в которых атомы водорода несколько смещены в сторону от линии, соединяющей атомы кислорода. Таким образом, упаковка молекул воды становится более плотной, что проявляется в аномальном увеличении плотности при плавлении льда. Лишь при температуре выше 4 oС эффект разрушения тетраэдрической структуры перекрывается обычным термическим расширением благодаря усилению теплового движения молекул.
Кластерной структурой объясняются и другие аномалии воды - высокие значения теплоты испарения, поверхностного натяжения и удельной теплоемкости а также влияние на свойства воды растворенных в ней веществ.
Жидкие кристаллы
При охлаждении некоторых жидких веществ появляется новое их состояние, похожее и на жидкое, и на твердое. В этом состоянии вещество полупрозрачно или непрозрачно, сохраняет текучесть, но уже имеет анизотропные свойства и обладает определенной упорядоченностью структуры.
Такое состояние вещества называют жидкокристаллическим. Жидкокристаллическое состояние было открыто в результате наблюдений за процессами плавления. При плавлении некоторых веществ образуется мутная жидкость, обладающая светорассеянием и двойным лучепреломлением. Образование жидкокристаллического состояния при плавлении сопровождается частичным разрушением дальнего порядка. При дальнейшем нагревании мутный расплав переходит в прозрачную жидкость, обладающую изотропными свойствами.
По степени молекулярной упорядоченности жидкие кристаллы занимают промежуточное положение между твердыми кристаллами, в которых существует трехмерный дальний порядок, и жидкостями, имеющими только ближний порядок в расположении частиц. Поэтому жидкокристаллическое состояние часто называют мезоморфным ("мезос" - промежуточный), а само вещество - мезофазой. Наиболее часто жидкокристаллическое состояние встречается у органических веществ, молекул которых имеют удлиненную или дискообразную форму.
Своеобразное сочетание свойств, присущих как жидкостям, так и кристаллам, обусловлено особенностью внутренней молекулярной структуры жидких кристаллов. Различаются три основных типа жидких кристаллов: смектический, нематический и холестерический.
 Смектические ( от греч. "смегма" - мыло) жидкие кристаллы могут быть образованы веществами, молекулы которых имеют вытянутую сигарообразную форму, причем они ориентированы параллельно друг другу и образуют тонкий слой. Внутри слоев, в боковых направлениях, строгая периодичность в расположении молекул отсутствует. Смектическими жидкими кристаллами являются, например, радужные мыльные пузыри. Смектический слой обладает важнейшим свойством твердого кристалла - анизотропией оптических свойств, так как вдоль длинной оси молекул свет распространяется с меньшей скоростью, чем поперек нее, и показатели преломления в жидком кристалле в этих направлениях различны.
Смектические ( от греч. "смегма" - мыло) жидкие кристаллы могут быть образованы веществами, молекулы которых имеют вытянутую сигарообразную форму, причем они ориентированы параллельно друг другу и образуют тонкий слой. Внутри слоев, в боковых направлениях, строгая периодичность в расположении молекул отсутствует. Смектическими жидкими кристаллами являются, например, радужные мыльные пузыри. Смектический слой обладает важнейшим свойством твердого кристалла - анизотропией оптических свойств, так как вдоль длинной оси молекул свет распространяется с меньшей скоростью, чем поперек нее, и показатели преломления в жидком кристалле в этих направлениях различны.
 Второй тип жидкокристаллических веществ называется нематическим (от греч. "нема" - "нить"). Эти вещества содержат нитевидные частицы, которые либо прилипают к стенкам сосуда, либо остаются свободными. Эти нити выглядят "причесанными" и направлены параллельно друг другу, но могут скользить вверх и вниз. Подходящая аналогия для нематических жидких кристаллов - длинная коробка с короткими карандашами, которые могут свободно поворачиваться вокруг своей оси, перемещаться вдоль коробки, но никогда не встают поперек. Нематические жидкие кристаллы не такие упорядоченные, как смектические. Тем не менее они тоже оптически анизотропны и под микроскопом дают "муаровую" текстуру с чередующимися светлыми и темными полосами. Частицы нематического жидкого кристалла реагируют на электрическое и магнитное поле так же, как железные опилки, располагаясь самым упорядоченным образом вдоль силовых линий поля.
Второй тип жидкокристаллических веществ называется нематическим (от греч. "нема" - "нить"). Эти вещества содержат нитевидные частицы, которые либо прилипают к стенкам сосуда, либо остаются свободными. Эти нити выглядят "причесанными" и направлены параллельно друг другу, но могут скользить вверх и вниз. Подходящая аналогия для нематических жидких кристаллов - длинная коробка с короткими карандашами, которые могут свободно поворачиваться вокруг своей оси, перемещаться вдоль коробки, но никогда не встают поперек. Нематические жидкие кристаллы не такие упорядоченные, как смектические. Тем не менее они тоже оптически анизотропны и под микроскопом дают "муаровую" текстуру с чередующимися светлыми и темными полосами. Частицы нематического жидкого кристалла реагируют на электрическое и магнитное поле так же, как железные опилки, располагаясь самым упорядоченным образом вдоль силовых линий поля.
 Холестерические жидкие кристаллы - это в основном производные холестерина. Здесь плоские и длинные молекулы собраны в слои (как у смектических), но внутри каждого слоя расположение частиц похоже больше на нематические жидкие кристаллы. Интересно то, что тончайшие соседние молекулярные слои в холестерическом жидком кристалле немного повернуты друг относительно друга, благодаря чему стопка подобных слоев описывает в пространстве спираль. В силу столь своеобразного строения эти жидкие кристаллы обладают необычными оптическими свойствами. Обычные свет, проходя через такие вещества, распадается на два луча, которые преломляются по-разному. Когда бесцветный, как вода, холестерический жидкий кристалл попадает в зону с меняющейся температурой, он принимает яркую окраску.
Холестерические жидкие кристаллы - это в основном производные холестерина. Здесь плоские и длинные молекулы собраны в слои (как у смектических), но внутри каждого слоя расположение частиц похоже больше на нематические жидкие кристаллы. Интересно то, что тончайшие соседние молекулярные слои в холестерическом жидком кристалле немного повернуты друг относительно друга, благодаря чему стопка подобных слоев описывает в пространстве спираль. В силу столь своеобразного строения эти жидкие кристаллы обладают необычными оптическими свойствами. Обычные свет, проходя через такие вещества, распадается на два луча, которые преломляются по-разному. Когда бесцветный, как вода, холестерический жидкий кристалл попадает в зону с меняющейся температурой, он принимает яркую окраску.
Из каждой тысячи новых органических соединений, синтезируемых в лабораториях мира, по крайней мере, пять могут образовывать жидкие кристаллы. Универсальные свойства таких веществ позволили использовать их во многих областях науки и техники, в частности при изготовлении жидкокристаллических дисплеев, плоских
Твердые вещества
Аморфные вещества
Кристаллические вещества
Типы кристаллических решеток
Изоморфизм и полиморфизм
Строение вещества определяется не только взаимным расположением атомов в химических частицах, но и расположением этих химических частиц в пространстве. Наиболее упорядочено размещение атомов, молекул и ионов в кристаллах (от греческого "кристаллос" - лед), где химические частицы (атомы, молекулы, ионы) расположены в определенном порядке, образуя в пространстве кристаллическую решетку. При определенных условиях образования они могут иметь естественную форму правильных симметричных многогранников. Кристаллическое состояние характеризуется наличием дальнего порядка в расположении частиц и симметрией кристаллической решетки.
Для аморфного состояния характерно наличие только ближнего порядка. Структуры аморфных веществ напоминают жидкости, однако обладают гораздо меньшей текучестью. Аморфное состояние обычно неустойчиво. Под действием механических нагрузок или при изменении температуры аморфные тела могут закристаллизоваться. Реакционная способность веществ в аморфном состоянии значительно выше, чем в кристаллическом.
Аморфные вещества
Главный признак аморфного (от греческого "аморфос" - бесформенный) состояние вещества - отсутствие атомной или молекулярной решетки, то есть трехмерной периодичности структуры, характерной для кристаллического состояния.
При охлаждении жидкого вещества не всегда происходит его кристаллизация. при определенных условиях может образоваться неравновесное твердое аморфное (стеклообразное) состояние. В стеклообразном состоянии могут находиться простые вещества (углерод, фосфор мышьяк, сера, селен), оксиды (например, бора, кремния, фосфора), галогениды, халькогениды, многие органические полимеры.
В этом состоянии вещество может быть устойчиво в течение длительного промежутка времени, например, возраст некоторых вулканических стекол исчисляется миллионами лет. Физические и химические свойства вещества в стеклообразном аморфном состоянии могут существенно отличаться от свойств кристаллического вещества. Например, стеклообразный диоксид германия химически более активен, чем кристаллический. Различия в свойствах жидкого и твердого аморфного состояния определятся характером теплового движения частиц: в аморфном состоянии частицы способны лишь к колебательным и вращательным движениям, но не могут перемещаться в толще вещества.
Существуют вещества, которые в твердом виде могут находиться только в аморфном состоянии. Это относится к полимерам с нерегулярной последовательностью звеньев.
Аморфные тела изотропны, то есть их механические, оптические, электрические и другие свойства не зависят от направления. У аморфных тел нет фиксированной температуры плавления: плавление происходит в некотором температурном интервале. Переход аморфного вещества из твердого состояния в жидкое не сопровождается скачкообразным изменением свойств. Физическая модель аморфного состояния до сих пор не создана.
Кристаллические вещества
Твердые кристаллы - трехмерные образования, характеризующиеся строгой повторяемостью одного и того же элемента структуры (элементарной ячейки) во всех направлениях. Элементарная ячейка представляет собой наименьший объем кристалла в виде параллелепипеда, повторяющегося в кристалле бесконечное число раз.
Геометрически правильная форма кристаллов обусловлена, прежде всего, их строго закономерным внутренним строением. Если вместо атомов, ионов или молекул в кристалле изобразить точки как центры тяжести этих частиц, то получится трехмерное регулярное распределение таких точек, называемое кристаллической решеткой. Сами точки называют узлами кристаллической решетки.
Типы кристаллических решеток
В зависимости от того, из каких частицы построена кристаллическая решетка и каков характер химической связи между ними, выделяют различные типы кристаллов.
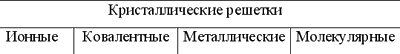
Ионные кристаллы образованы катионами и анионами (например, соли и гидроксиды большинства металлов). В них между частицами имеется ионная связь.
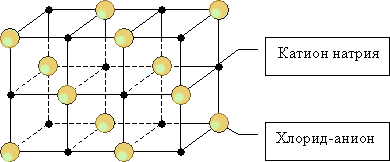 Ионные кристаллы могут состоять из одноатомных ионов. Так построены кристаллы хлорида натрия, иодида калия, фторида кальция.
Ионные кристаллы могут состоять из одноатомных ионов. Так построены кристаллы хлорида натрия, иодида калия, фторида кальция.
В образовании ионных кристаллов многих солей участвуют одноатомные катионы металлов и многоатомные анионы, например, нитрат-ион NO3−, сульфат-ион SO42−, карбонат-ион CO32−.
В ионном кристалле невозможно выделить одиночные молекулы. Каждый катион притягивается к каждому аниону и отталкивается от других катионов. Весь кристалл можно считать огромной молекулой. Размеры такой молекулы не ограничены, поскольку она может расти, присоединяя новые катионы и анионы.
Большинство ионных соединений кристаллизуется по одному из структурных типов, которые отличаются друг от друга значением координационного числа, то есть числом соседей вокруг данного иона (4, 6 или 8). Для ионных соединений с равным числом катионов и анионов известно четыре основных типа кристаллических решеток: хлорида натрия (координационное число обоих ионов равно 6), хлорида цезия (координационное число обоих ионов равно 8), сфалерита и вюрцита (оба структурных типа характеризуются координационном числом катиона и аниона, равным 4). Если число катионов вдвое меньше числа анионов, то координационное число катионов должно быть вдвое больше координационного числа анионов. В этом случае реализуются структурные типы флюорита (координационные числа 8 и 4), рутила (координационные числа 6 и 3), кристобалита (координационные числа 4 и 2).
Обычно ионные кристаллы твердые, но хрупкие. Их хрупкость обусловлена тем, что даже при небольшой деформации кристалла катионы и анионы смещаются таким образом, что силы отталкивания между одноименными ионами начинают преобладать над силами притяжения между катионами и анионами, и кристалл разрушается.
Ионные кристаллы отличаются высокими температурами плавления. В расплавленном состоянии вещества, образующие ионные кристаллы, электропроводны. При растворении в воде эти вещества диссоциируют на катионы и анионы, и образующиеся растворы проводят электрический ток.
Высокая растворимость в полярных растворителях, сопровождающаяся электролитической диссоциацией обусловлена тем, что в среде растворителя с высокой диэлектрической проницаемостью ε уменьшается энергия притяжения между ионами. Диэлектрическая проницаемость воды в 82 раза выше, чем вакуума (условно существующего в ионном кристалле), во столько же раз уменьшается притяжение между ионами в водном растворе. Эффект усиливается за счет сольватации ионов.
Атомные кристаллы состоят из отдельных атомов, объединенных ковалентными связями. Из простых веществ только бор и элементы IVA-группы имеют такие кристаллические решетки. Нередко соединения неметаллов друг с другом (например, диоксид кремния) также образуют атомные кристаллы.
Так же как и ионные, атомные кристаллы можно считать гигантскими молекулами. Они очень прочные и твердые, плохо проводят теплоту и электричество. Вещества, имеющие атомные кристаллические решетки, плавятся при высоких температурах. Они практически нерастворимы в каких-либо растворителях. Для них характерна низкая реакционная способность.
Молекулярные кристаллы построены из отдельных молекул, внутри которых атомы соединены ковалентными связями. Между молекулами действуют более слабые межмолекулярные силы. Они легко разрушаются, поэтому молекулярные кристаллы имеют низкие температуры плавления, малую твердость, высокую летучесть. Вещества, образующие молекулярные кристаллические решетки, не обладают электрической проводимостью, их растворы и расплавы также не проводят электрический ток.
Межмолекулярные силы возникают за счет электростатического взаимодействия отрицательно заряженных электронов одной молекулы с положительно заряженными ядрами соседних молекул. На силу межмолекулярного взаимодействия влияет много факторов. Важнейшими среди них является наличие полярных связей, то есть смещения электронной плотности от одних атомов к другим. Кроме того, межмолекулярное взаимодействие проявляется сильнее между молекулами с большим числом электронов.
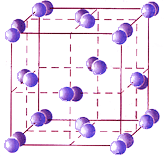 Большинство неметаллов в виде простых веществ (например, иод I2, аргон Ar, сера S8) и соединений друг с другом (например, вода, диоксид углерода, хлороводород), а также практически все твердые органические вещества образуют молекулярные кристаллы.
Большинство неметаллов в виде простых веществ (например, иод I2, аргон Ar, сера S8) и соединений друг с другом (например, вода, диоксид углерода, хлороводород), а также практически все твердые органические вещества образуют молекулярные кристаллы.
Для металлов характерна металлическая кристаллическая решетка. В ней имеется металлическая связь между атомами. В металлических кристаллах ядра атомов расположены таким образом, чтобы их упаковка была как можно более плотной. Связь в таких кристаллах является делокализованной и распространяется на весь кристалл. Металлические кристаллы обладают высокой электрической проводимостью и теплопроводностью, металлическим блеском и непрозрачностью, легкой деформируемостью.
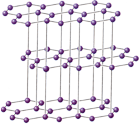 Классификация кристаллических решеток отвечает предельным случаям. Большинство кристаллов неорганических веществ принадлежит к промежуточным типам - ковалентно-ионным, молекулярно-ковалентным и т.д. Например, в кристалле графита внутри каждого слоя связи ковалентно-металлические, а между слоями - межмолекулярные.
Классификация кристаллических решеток отвечает предельным случаям. Большинство кристаллов неорганических веществ принадлежит к промежуточным типам - ковалентно-ионным, молекулярно-ковалентным и т.д. Например, в кристалле графита внутри каждого слоя связи ковалентно-металлические, а между слоями - межмолекулярные.
Изоморфизм и полиморфизм
Многие кристаллические вещества имеют одинаковые структуры. В то же время одно и то же вещество может образовывать разные кристаллические структуры. Это находит отражение в явлениях изоморфизма и полиморфизма.
Изоморфизм заключается в способности атомов, ионов или молекул замещать друг друга в кристаллических структурах. Этот термин (от греческих "изос" - равный и "морфе" - форма) был предложен Э. Мичерлихом в 1819 г. Закон изоморфизма бы сформулирован Э. Мичерлихом в 1821 г. таким образом: "Одинаковые количества атомов, соединенные одинаковым способом, дают одинаковые кристаллические формы; при этом кристаллическая форма не зависит от химической природы атомов, а определяется только их числом и относительным положением".
Работая в химической лаборатории Берлинского университета, Мичерлих обратил внимание на полное сходство кристаллов сульфатов свинца, бария и стронция и близость кристаллических форм многих других веществ. Его наблюдения привлекли внимание известного шведского химика Й.-Я. Берцелиуса, который предложил Мичерлиху подтвердить замеченные закономерности на примере соединений фосфорной и мышьяковой кислот. В результате проведенного исследования был сделан вывод, что "две серии солей различаются лишь тем, что в одной в качестве радикала кислоты присутствует мышьяк, а в другой - фосфор". Открытие Мичерлиха очень скоро привлекло внимание минералогов, начавших исследования по проблеме изоморфного замещения элементов в минералах.
При совместной кристаллизации веществ, склонных к изоморфизму (изоморфных веществ), образуются смешанные кристаллы (изоморфные смеси). Это возможно лишь в том случае, если замещающие друг друга частицы мало различаются по размерам (не более 15%). Кроме того, изоморфные вещества должны иметь сходное пространственное расположение атомов или ионов и, значит, сходные по внешней форме кристаллы. К таким веществам относятся, например, квасцы. В кристаллах алюмокалиевых квасцов KAl(SO4)2 . 12H2O катионы калия могут быть частично или полностью заменены катионами рубидия или аммония, а катионы алюминия - катионами хрома(III) или железа(III).
Изоморфизм широко распространен в природе. Большинство минералов представляет собой изоморфные смеси сложного переменного состава. Например, в минерале сфалерите ZnS до 20% атомов цинка могут быть замещены атомами железа (при этом ZnS и FeS имеют разные кристаллические структуры). С изоморфизмом связано геохимическое поведение редких и рассеянных элементов, их распространение в горных породах и рудах, где они содержатся в виде изоморфных примесей.
Изоморфное замещение определяет многие полезные свойства искусственных материалов современной техники - полупроводников, ферромагнетиков, лазерных материалов.
Многие вещества могут образовывать кристаллические формы, имеющие различные структуру и свойства, но одинаковый состав (полиморфные модификации). Полиморфизм - способность твердых веществ и жидких кристаллов существовать в двух или нескольких формах с различной кристаллической структурой и свойствами при одном и том же химическом составе. Это слово происходит от греческого "полиморфос" - многообразный. Явление полиморфизма было открыто М. Клапротом, который в 1798 г. обнаружил, что два разных минерала - кальцит и арагонит - имеют одинаковый химический состав СаСО3.
Полиморфизм простых веществ обычно называют аллотропией, в то же время понятие полиморфизма не относится к некристаллическим аллотропным формам (например, газообразным О2 и О3). Типичный пример полиморфных форм - модификации углерода (алмаз, лонсдейлит,
Лонсдейлит
