Микросомальная система гидроксилирования
Классификация ферментов.
Микросомальная система гидроксилирования
Сычева И.М., Хидирова Л.Д.
(сокращенная форма методического пособия - ЭНЗИМОЛОГИЯ)
для студентов 2-го курса лечебного, педиатрического и стоматологического факультетов.
Новосибирск – 2012
Классификация ферментов
В зависимости от типа катализируемой реакции выделяют 6 классов ферментов.
Рабочее название фермента строится так: название субстрата + подкласс фермента.
| Класс | Тип катализируемой реакции |
| Оксидоредуктазы | Окислительно-восстановительные реакции. |
| Трансферазы | Перенос отдельных групп атомов от донорной молекулы к акцепторной молекуле. |
| Гидролазы | Гидролитическое (с участием воды) расщепление связей. |
| Лиазы | Расщепление связей способом, отличным от гидролиза или окисления. |
| Изомеразы | Взаимопревращение различных изомеров. |
| Лигазы (синтетазы) | Образование связей в реакции конденсации двух различных соединений (используется энергия АТР). |
Класс – оксидоредуктазы
- катализируют окислительно-восстановительные реакции.
Подклассы оксидоредуктаз:
а) дегидрогеназы
б) цитохромы
в) оксидазы
г) пероксидазы
а) Дегидрогеназы отщепляют водород от молекулы субстрата.
SH2 + НАД+↔ S + НАДНН+
Дегидрогеназы разделяют на пиридиновые и флавиновые.
Пиридиновые дегидрогеназы, в качестве кофермента содержат НАД+ (NAD+) или НАДФ+(NADP+). НАД – никотинамид аденин динуклеотид.
Пример: реакция окисления этилового спирта:
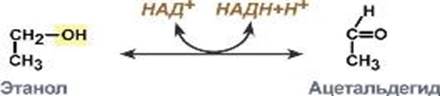
Алкогольдегидрогеназа
Пример: реакция окисления соли яблочной кислоты (малата):
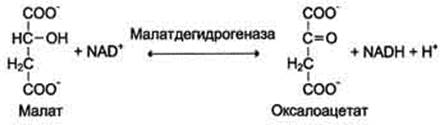
Рабочее название дегидрогеназ строится так: название субстрата (восстановленная форма) + дегидрогеназа.
Флавиновые дегидрогеназы в качестве простетической группы содержат ФАД.
(ФАД-флавинадениннуклеотид).
Пример: реакция окисления соли янтарной кислоты (сукцината):
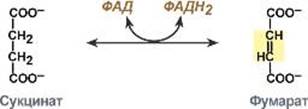
сукцинатдегидрогенназа
Дегидрогеназы бывают аэробные и анаэробные. Аэробные дегидрогеназы отдают атомы водорода кислороду с образованием перекиси водорода:
ФАДН2 + О2 →ФАД+ Н2О2
Пиридиновые дегидрогеназы, как правило, анаэробные, а флавиновые бывают и аэробные и анаэробные. Дегидрогеназы бывают первичные и вторичные . Первичные окисляют небелковый субстрат. Вторичные – белковый. Обычно они окисляют другую дегидрогеназу. Реакция выглядит так: НАДНН++ФАД→ФАДН2+НАД+
б) Цитохромы - это гемсодержащие ферменты, они переносят электроны. Цитохромы участвуют в тканевом дыхании и микросомальном окислении. Они бывают аэробные и анаэробные. В качестве аэробных цитохромов можно привести пример цитохрома Р450 микросомальной системы гидроксилирования.
в) оксидазы (гидроксилазы)
Пример: реакция окисления дофамина до норадреналина
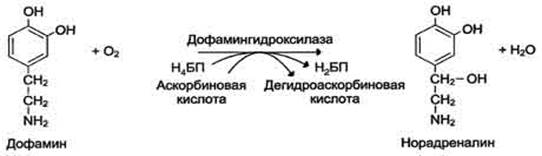
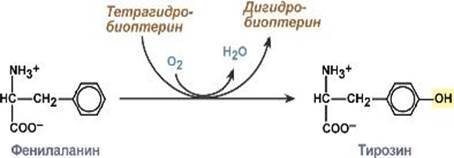
Пример: :реакция окисления фенилаланина до тирозина
г) Пероксидазы расщепляют перекиси. В качестве примера можно привести:
2Н2О2→2Н2О+ О2
каталаза
RH+ Н2О2→ RОH+ Н2О
Пероксидаза
Эти ферменты защищают наш организм от токсичных форм кислорода.
Класс – трансферазы
-переносят группы с одного субстрата на другой или обмен группами между субстратами. В зависимости от того, какие группы переносят трансферазы их разделяют на подклассы:
а) аминотрансферазы
б) ацилтрансферазы,
в) метилтранс-феразы,
г) гликозилтрансферазы,
д)фосфо-трансферазы (киназы).
В качестве примера приведем:
Аминатрансферазу : обмен амино- группы на кето- группу (реакция трансаминирования)
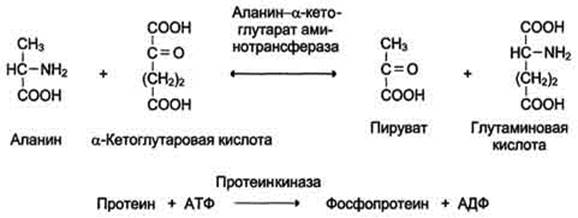
Фосфотрансфераза (киназа). Фосфатная группа переносится с АТФ на субстрат.
Класс – гидролазы
- катализируют реакции гидролиза (распада веществ под действием воды). В зависимости от вида связи гидролазы подразделяются на подклассы.
а) эстеразы –гидролиз сложноэфирных связей
б) фосфоэстеразы – гидролиз фосфоэфирных связей
в) пептидазы – гидролиз пептидных связей.
г) гликозидазы –гидролиз гликозидных связей между молекулами углеводов.
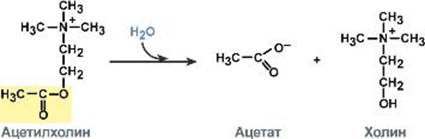
В качестве примера приведем ацетилхолинэстеразу .
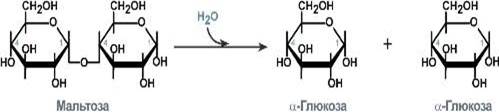
гликозидазу (мальтазу)
Класс –лиазы
- катализируют реакции распада веществ без участия воды). В зависимости от вида связи гидролазы подразделяются на подклассы.
а) С-С лиазы
б) С-N лиазы
в) C-О лиазы
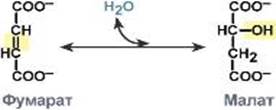
Фумаратгидротаза
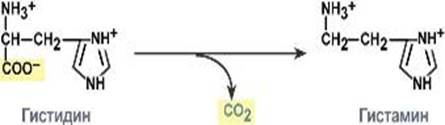
Гистидиндекарбоксилаза
Класс – изомеразы
- катализируют реакции изомеризации.
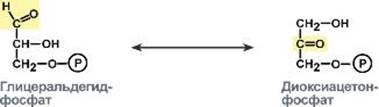
Фосфоглицеральдегидизомераза
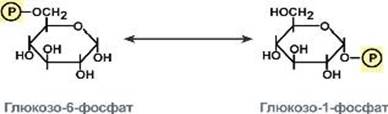
изомераза глюкоза-6- фосфат
Класс – синтетазы
- катализируют реакции синтеза веществ с затратой АТФ.
Синтетаза щавелевоуксусной кислоты
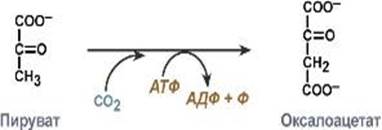
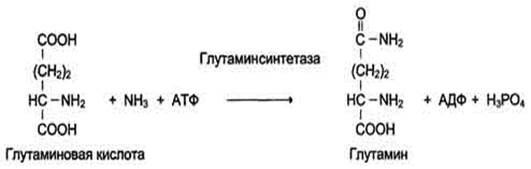
Название синтетаз строится так: Синтезируемое соединение +синтетаза.
Микросомальная система гидроксилирования
Микросомальная система работает в эндоплазматической сети. Она представляет из себя мультиферментный комплекс в состав, которого входят
3 фермента :
1- флавопротеид,
2- цитохром b5
3- цитохром Р450.
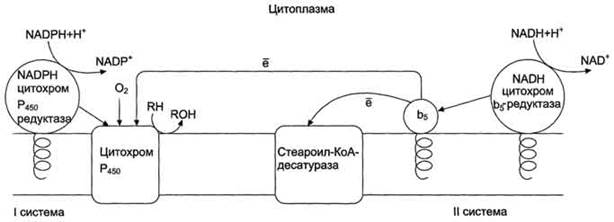
Суммарная реакция окисления может быть записана:
RH + НАДФН2+ О2 → ROH + Н2О + НАДФ
Реакция идет в 3 этапа:
1. Сначала с НАДФН2 атомы водорода переносятся на флавопротеид.
2. С флавопотеида электроны переносятся на цитохром b5 и далее на
цитохром Р450. Атом железа в цитохроме восстанавливается Fe3+→ Fe2+
3. Двухвалентное железо связывает молекулу кислорода. Один атом кислорода встраивается в окисляемую молекулу, а второй взаимодействует с двумя протонами, образуя воду.
НАДФН2 образуется при окислении глюкозы в пентозном цикле и при окислении яблочной кислоты яблочным ферментом.:
яблочная кислота +НАДФ → ПВК +СО2+ НАДФН2
Роль микросомальной системы гидроксилирования:
1. Участвует в синтезе холестерина
2. Участвует в синтезе желчных кислот
3. Участие в синтезе стероидных гормонов
4. Обезвреживание токсинов.
При окислении токсичных гидрофобных веществ встраивается ОН группа. Из-за этого возрастает полярность соединения
· увеличивается растворимость в воде
· облегчается выведение в мочу и желчь
· ухудшается их транспорт в клетку через мембрану
· появление ОН группы также позволяет далее обезвреживать токсины путем их взаимодействия с серной или глюкуроновой кислотами
