Теория абсолютных скоростей реакций
Обычно данные о скоростях реакций и энергиях активации получают экспери-ментальным путем. При помощи экстратермодинамических соотношений, в частности принципа линейности свободных энергий, удается рассчитать скорость одной реакции, зная скорость сходной реакции, т. е. относительные значения скоростей. Однако принципиальный интерес представляет расчет абсолютных скоростей реакций исходя из свойств атомов и молекул. Этот раздел химической кинетики называется теорией абсо-лютных скоростей реакций. Основными задачами теории абсолютных скоростей являются: расчет уравнения поверхности потенциальной энергии и выяснение связи скорости реакции с формой потенциальной поверхности.
Уравнение поверхности потенциальной энергии можно теоретически рассчитать на основании уравнения Шредингера, однако ввиду математических сложностей возможен лишь приближенный расчет с помощью современных компьютеров.
В последнее время, в связи с развитием неэмпирических квантово-химических мето-дов расчета электронных оболочек (методов ab initio) и расширением возможностей вычислительной техники все шире применяются расчетные методы, рассматривающие молекулы вместе с сольватными оболочками.
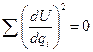 Поскольку для седловой точки tповерхности потенциальной энергии выполняется условие минимума энергии дU/дqi=0, д2U/дq2>0 для Зn-7 координат и д2U/дq2<0 (условие максимума энергии) по координате реакции, структуру переходного состояния нельзя определить минимизацией полной энергии системы. Поэтому расчет переходного состояния проводится методом минимизации нормы градиента потенциальной энергии системы, т. е. суммы квадратов первых производных по кooрдинaтaм:
Поскольку для седловой точки tповерхности потенциальной энергии выполняется условие минимума энергии дU/дqi=0, д2U/дq2>0 для Зn-7 координат и д2U/дq2<0 (условие максимума энергии) по координате реакции, структуру переходного состояния нельзя определить минимизацией полной энергии системы. Поэтому расчет переходного состояния проводится методом минимизации нормы градиента потенциальной энергии системы, т. е. суммы квадратов первых производных по кooрдинaтaм:
При этом матрица силовых постоянных связей системы ║д2U/дqi2║ должна иметь только одно отрицательное собственное значение, соответствующее координате реакции.
Для ограничения объема расчетной работы вначале исходят из общетеоретических предположений, таких как постулат Хэммонда и принцип наименьшего движения (который утверждает, чего наиболее вероятный путь реакции, или путь наименьшего движения, соответствует сохранению в переходном состоянии максимального числа элементов симметрии, имеющихся в конечном продукте). При этом надо выбрать координату реакции (т. е. направление сближения реагентов), рассчитать величины энергии системы для разных значений координаты реакции (через определенные интервалы), минимизируя потенциальную энергию реагирующей системы относительно других естественных координат. Найденная при этом структура с максимальным уровнем энергии соответствует переходному состоянию в пространстве естественных координат.
Задача соотнесения скорости реакции с формой потенциальной поверхности была решена еще до развития квантово-химических расчетных методов Эйрингом и независимо Эвансом и Поляни, которые предложили метод активированного комплекса. Этот метод позволяет рассчитать скорость реакции, если из опыта известны некоторые параметры, характеризующие потенциальную поверхность.
Из рисунка 2.5 видно, что δ - область состояний вблизи вершины потенциального барьера, которую можно рассматривать как переходное состояние. Поскольку максимум на кривой потенциальной энергии является математической точкой, то число систем, точно локализованных в максимуме, равно нулю. Поэтому принимается, что в переходном состоянии находятся системы, для которых координаты реакции располагаются в узком интервале δ, включающем максимум. При достаточно малой длине отрезка δ число систем, находящихся в переходном состоянии, будет пропорционально δ. Очевидно, что если система достигла переходного состояния, то она неизбежно перевалит через потенциальный барьер. Таким образом, переходному состоянию приписывается конечная протяженность δ, которую система проходит за время τ. Если в единице объема имеется с≠ активированных комплексов, то скорость прохождения через потенциальный барьер определяется следующим выражением
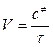
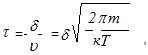 Время прохождения активированного комплекса через потенциальный барьер (τ), в соответствии с кинетической теорией газов, составляет
Время прохождения активированного комплекса через потенциальный барьер (τ), в соответствии с кинетической теорией газов, составляет
(2.1)
где т-масса частицы;
υ - средняя скорость частиц;
Т - абсолютная температура;
к - постоянная Больцмана.
Для определения величины с≠ исходят из допущения, что потребление активированных комплексов не нарушает статистическое распределение Максвелла-Больцмана, т.е. рас-пределение достигает равновесия быстрее, чем происходит химическое превращение. Тогда можно выразить с≠ через концентрации исходных реагентов АВ и С, рассматривая активированный комплекс как квазичастицу, составленную из АВ и С. Активированный комплекс отличается от обычных молекул только тем, что перемещение его вдоль одной степени свободы (координаты реакции) соответствуют максимуму энергии, тогда как по всем остальным координатам - минимуму.
Привлекая математический аппарат статистической физики, можно записать:
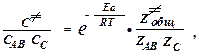 (2.2)
(2.2)
где САВ, Cc, C ≠ - концентрации частиц АВ,
С, Х ≠; Еа - разность нулевых колебательных энергий активированного
комплекса (Х ≠) и исходных частиц,
z- статистические суммы состояний частиц для всех степеней свободы.
Выделяя для активированного комплекса степень свободы вдоль координаты реакции (X), можно записать
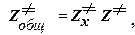
где z≠х- статистическая сумма состояний активированного комплекса для движения
вдоль координаты реакции,
z≠-статистическая сумма состояний активированного комплекса для всех остальных
степеней свободы.
Если перемещение по координате реакции есть поступательное движение на отрезке δ
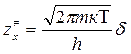 (см. рисунок 2.5), то
(см. рисунок 2.5), то
Тогда выражение (2.2) можно записать как
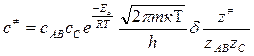
В этом случае с учетом уравнения (2.1) выражение для скорости химической реакции принимает вид:
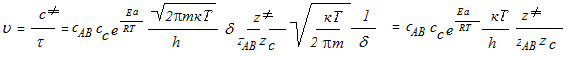
В соответствии с законом действия масс υ=k cAB cс, тогда
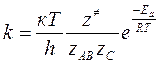 (2.3)
(2.3)
где k - константа скорости;
к - постоянная Больцмана,
остальные обозначения приведены выше.
Это основная формула теории активированного комплекса.
При выводе выражения (2.3) предполагалось, что система, пройдя активационный барьер, уже не возвращается обратно. На самом деле существует некоторая вероятность χ возврата в исходное состояние, т. к. для необратимого перехода необходима дезактивация системы в результате соударений.
В этом случае выражение для константы скорости реакции принимает вид:
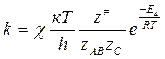 (2.4)
(2.4)
где χ- так называемый трансмиссионный коэффициент.
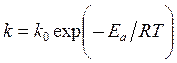 Обычно для реакций в газовой фазе χ <1, однако в некоторых случаях, в частности для реакций переноса протона в растворах, он может превышать единицу. В этом случае говорят о туннельном эффекте (или подбарьерном переходе), который вытекает из квантовой теории и является следствием волновой природы частиц, в частности наиболее легкого из ядер - протона. Выражение (2.4) может быть преобразовано в следующее:
Обычно для реакций в газовой фазе χ <1, однако в некоторых случаях, в частности для реакций переноса протона в растворах, он может превышать единицу. В этом случае говорят о туннельном эффекте (или подбарьерном переходе), который вытекает из квантовой теории и является следствием волновой природы частиц, в частности наиболее легкого из ядер - протона. Выражение (2.4) может быть преобразовано в следующее:
где 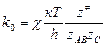 - предэкспоненциальный множитель уравнения Аррениуса.
- предэкспоненциальный множитель уравнения Аррениуса.
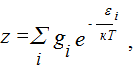 Суть расчета константы скорости реакции по уравнениям (2.3), (2.4) сводится к определению статистических сумм, т. к. для того, чтобы рассчитать k, необходимо знать высоту потенциального барьера Еaи статистические суммы состояний исходных реагентов и активированного комплекса. В общем статистическая сумма z находится из выражения
Суть расчета константы скорости реакции по уравнениям (2.3), (2.4) сводится к определению статистических сумм, т. к. для того, чтобы рассчитать k, необходимо знать высоту потенциального барьера Еaи статистические суммы состояний исходных реагентов и активированного комплекса. В общем статистическая сумма z находится из выражения
(2.5)
где εi - энергия данного энергетического уровня;
gi - число состояний, отвечающих данному уровню, т. н. вырождение уровня.
Статистическая сумма состояний частицы определяется вкладом различных видов движения - поступательного, вращательного, колебательного и электронного:
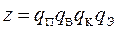 .
.
Наибольший вклад в значение z вносят поступательные и вращательные статистические суммы, а колебательные и электронные в соответствии с уравнением (2.5) при обычных температурах близки к единице, т. е. практически все частицы располагаются на нулевом колебательном и основном электронном уровнях энергии. Вклады поступательных и вращательных статистических сумм можно рассчитать, если известны массы и моменты инерции реагентов и активированного комплекса:
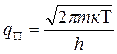 (2.6)
(2.6)
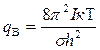
где I- момент инерции;
m - масса;
σ- число симметрии частицы.
В соответствии с уравнением (2.6) для частицы с m =100 при 300оК qпдля одной степени свободы составляет 770; qВколеблется в пределах l01÷l02. Таким образом, для расчета статистических сумм состояний активированного комплекса необходимо иметь хотя бы приближенное представлениео его геометрии.
