Корозія металів. Електрохімічна корозія
Під дією навколишнього середовища метали руйнуються, перетворюючись в оксиди, гідрати оксидів та інші сполуки, руйнування металів під дією навколишнього середовища називають корозією.
Розрізняють два види корозії: хімічну та електрохімічну. Під хімічною корозією розуміють руйнування металу при взаємодії його сухими газами, або рідинами, які не проводять електричного струму. При нагріванні металів на повітрі більшість з них окислюються. У деяких металів, особливо у заліза та його сплавів (чавун, сталь) оксиди утворюються у вигляді пористого шару, який не захищає поверхні металу від дальшого окислення. Особливо великої шкоди завдає електрохімічна корозія. Вона спостерігається при контакті двох металів різної активності з водою чи іншим електролітом.
Теорію електрохімічної корозії розробили російські вчені В. O. Кістяківський, В. Г. Акимов та інші. Згідно з цією теорією, найлегше руйнуються метали за наявності електролітів та інертних домішок (карбіди, метали з вищими значеннями стандартних потенціалів). У цих випадках створюються умови для виникнення гальванічного елемента.
Внаслідок електрохімічної корозії активніша складова частина руйнується, перетворюючись на оксид, гідроксид або розчинний електроліт, а на поверхні інертної домішки виділяється водень чи кисень.
Метал, або та частина його поверхні де проходить перехід йонів в розчин називається анодом (метал піддається корозії), а метал або поверхня на якому проходить відновлення - катодом.
Наприклад, якщо в розчин HCI опустити цинкову і міцну пластинку та з’єднати їх провідником, то електрони з більш активного металу будуть переходити на менш активний метал. В цьому випадку можливе відновлення йонів водню, по схемі, (рис.13.10 )
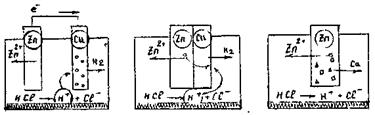
Рисунок 13.10 – Виникнення і робота мікрогальванічних елементів
Електрони будуть переходити, якщо поверхні металів дотикаються, або якщо в структурі одного металу є домішки іншого металу, що відрізняється за хімічною активністю.
Розглянемо корозійну поведінку стальних конструкцій, (сталь має домішки або вуглецю (С), або цементиту Fe3C) у вологому середовищі (атмосферні опади, підземна корозія, морська корозія тощо) (рис.13.11).
Попадаючи у вологе середовище проходить окиснення заліза по схемі:
Fe0 - 2ē → Fe2+,
відповідно в області залізної пластини будуть виділятися катіони заліза.
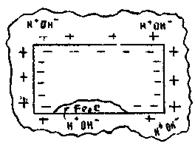
Рисунок 13.11 – Виникнення і робота гальванічної пари за рахунок включення цементиту
У воді є йони Гідрогену, здатні до відновлення:
2H++ 2ē = H2
Крім того, у воді є також розчинений кисень, який теж здатний до відновлення:
O2 + 2H2О + 4ē = 4 ОН–
В області цементиту, маючи високу електропровідність, виділення катіонів не буде, тобто катіони в розчин не переходять.
Йони водню чи молекули кисню підходять до поверхні цементиту і відновлюються згідно вищезазначених рівнянь. Виникає гальванічний елемент, внаслідок чого метал руйнується. Як бачимо, в основі процесу лежать електрохімічні процеси. В даному випадку мирозглянули механізм корозії (тобто виникнення гальванічної пари, за рахунок включення цементиту). В даній парі цементит є катодом, залізо - анодом.
Отже, найважливішими окисниками, що спричинюють електрохімічну корозію, є розчинений кисень та йони Гідрогену.
Оскільки потенціал, що відповідає електродному процесу 2H++ 2ē = H2 в нейтральному середовищі дорівнює -0,41 В, то йони Гідрогену, що містяться у воді або в нейтральному водному середовищі, можуть окиснювати тільки ті метали, значення потенціалів яких менші за
-0,41 В, тобто метали від початку ряду електрохімічних потенціалів до Кадмію.
Розчинений у воді кисень здатний окиснювати ті метали, потенціал яких менший за 0,8 В, оскільки потенціал, що відповідає електродному процесу O2 + 2H2О + 4ē = 4 ОН– у нейтральному середовищі дорівнює 0,8 В.
Отже, розчинений у воді кисень може окиснювати метали, розміщені від початку ряду електрохімічних потенціалів до Аргентуму.
Чисті метали стійкіші проти зовнішніх впливів, ніж сплави.
Якщо метал містить домішки, то корозія його в розчинах електролітів виникає як результат дії невеликих місцевих (локальних) гальванічних елементів (пар). Анодом гальванічного елемента стає активніший метал, який руйнується.
Подібні процеси проходять при контакті заліза та його сплавів з менш активними металами (рис. 13.12).
При контакті Fe з Cu, які знаходяться у вологому повітрі чи іншому нейтральному електроліті, виникає гальванічний елемент, в якому негативним електродом служить залізо, а позитивним - мідь (рис.13.12).
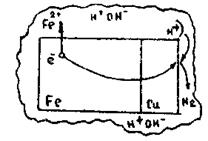
Рисунок 13.12 – Виникнення і робота Fe/Cu гальванічного елементу
В результаті роботи такого гальванічного елемента залізоокислюється, так як воно безпосередньо віддає свої електрони міді. В розчині електроліту йони заліза (ІІ) з’єднуються з йонами OH−, утворюючи Fe(OH)2, який окислюється киснем повітря в гідроксид заліза (ІІІ). Схема процесу:
Fe0 – 2 ē → Fe2+
O2 + 2H2О + 4е = 4 ОН–,
Fe2+ + 2 ОН- = Fe(OH)2
4Fe(OH)2 + 2H2O + O2 → 4Fe(OH)3
В результаті продукти корозії складаються із суміші ферум (ІІ) та ферум (ІІІ) оксидів та їх гідратів: xFenOm ∙ yH2O
Великої шкоди завдають так звані „,блукаючі струми”. Джерелом їх служить електротранспорт, лінії електропередач тощо. Струм величиною в 1 А протягом року знищує біля 10 кг заліза, 37 кг свинцю.
Розрізняють речовини - пасиватори та активатори корозії. Пасиватори - речовини за допомогою яких утворюються оксидні плівки на металах (конц. HNO3, сильні окисники K2Cr2O7). Активатори - речовини, які сприяють руйнуванню оксидної плівки (Cl-) в морській воді, де вміст їх значний.
Приклад 18. Наведіть приклади, зарисуйте схеми, запишіть електрохімічні рівняння, що мають місце при захисті металів від корозії.
Відповідь:
