Классификация и номенклатура
Глава 10
ГИДРОКСИЛПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
Гидроксилпроизводные содержат в молекуле одну или несколько ОН-групп. Гидроксилпроизводные, содержащие связь 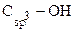 , называют спиртами. Соединения, в которых группа ОН связана с ненасыщенным атомом углерода, называют енолами, с атомом углерода ароматического кольца – фенолами.
, называют спиртами. Соединения, в которых группа ОН связана с ненасыщенным атомом углерода, называют енолами, с атомом углерода ароматического кольца – фенолами.
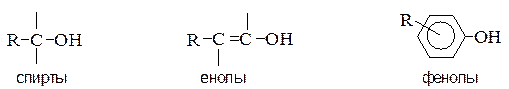
Спирты
Классификация и номенклатура
В зависимости от типа атома углерода, с которым связана гидроксильная группа, различают первичные, вторичные и третичные спирты.
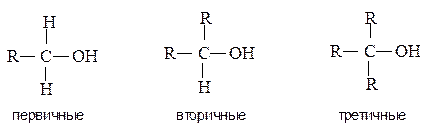
В заместительной номенклатуре гидроксильная группа как старшая характеристическая группа обозначается суффиксом “-ол”. Если в молекуле имеются группы, превосходящие ее по старшинству, то гидроксильную группу обозначают префиксом “гидрокси-“. Согласно радикально-функциональной номенклатуре алканолы называются спиртами.
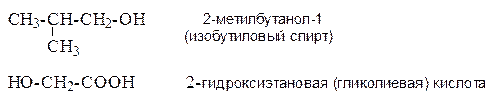
Методы получения
1) Гидролиз галогенпроизводных:
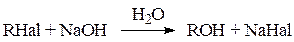
Hal = Cl, Br
2) Гидратация алкенов:
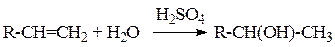
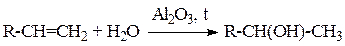
3) Восстановление карбонильных соединений:
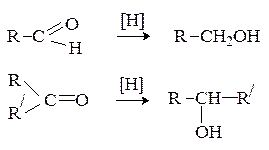
[H]: 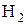 /кат., кат. – Ni, Pt, Pd;
/кат., кат. – Ni, Pt, Pd;
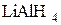 ;
; 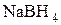 .
.
Физические свойства
Спирты являются бесцветными жидкостями или кристаллическими веществами с характерным запахом. Первые члены ряда имеют приятный запах, у бутанолов и пентанолов запах становится неприятным («сивушным»).
Отличительная черта алканолов - аномально высокая температура кипения, что обусловлено сильными межмолекулярными взаимодействиями в спиртах за счет образования водородных связей.
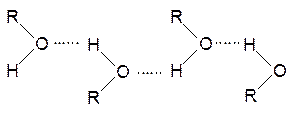
Низшие спирты С1-С4 хорошо растворимы в воде, что связано с их способностью к образованию водородных связей с молекулами растворителя.
Биологическая роль и применение в медицине
Большинство спиртов являются физиологически активными соединениями. Они обладают токсическим и наркотическим действием, которое возрастает с увеличением длины цепи, проходя через максимум при 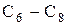 .
.
Первый член гомологического ряда - метанол – сильный яд с кумулятивным действием. При приеме внутрь даже в небольших количествах (5 -10 г) вызывает слепоту, большие дозы (30 г) смертельны.
Этанол действует опьяняюще, а в больших дозах вызывает состояние, близкое к наркозу. Используется в медицине как наружное антисептическое средство, а также для приготовления настоек и экстрактов лекарственных веществ.
Бутиловые и амиловые спирты известны как компоненты сивушных масел, образующихся в качестве побочных продуктов при производстве этанола сбраживанием углеводов.
К одноатомным спиртам алициклического ряда относятся такие биологически активные соединения, как ментол, ретинол (см. 18.2.1), холестерин (см. 18.2.2).
Химические свойства
Реакции спиртов определяются присутствием группы ОН и протекают по следующим основным направлениям.
1) Замещение водорода ОН группы под действием оснований (кислотные свойства).
2) Взаимодействие с электрофильными реагентами по атому кислорода с неподеленной парой электронов (основные и нуклеофильные свойства).
3) Взаимодействие с нуклеофильными реагентами по a-углеродному атому, несущему частичный положительный заряд (реакции нуклеофильного замещения ОН группы).
4) Дегидратация (участвуют связь С-Н в b-положении и связь С-О).
5) Окисление (участвуют связь С-Н в a-положении и связь О-Н).
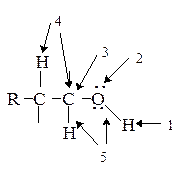
Кислотные свойства.Спирты взаимодействуют с активными металлами (Na, K, Mg, Al и др.) с образованием алкоголятов.
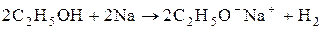

этилат натрия
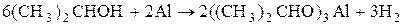
изопропилат алюминия
Алкоголяты образуются также при действии на спирты сильных оснований.
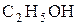 | + | 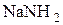 | D | 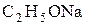 | + | 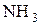 |
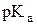 =15,9 =15,9 | 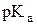 =33 =33 |
При взаимодействии спиртов со щелочами равновесие сдвинуто в сторону гидролиза алкоголятов, так как спирты являются более слабыми кислотами, чем вода:
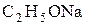 | + | 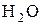 | D | 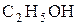 | + | NaOH |
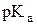 =15,7 =15,7 | 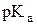 =15,9 =15,9 |
Кислотность спиртов в водных растворах уменьшается в ряду с увеличением длины и разветвленности радикала:
| CH3OH | первичный | вторичный | третичный | |
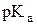 | 15,2 | ~16 | ~16,5 | ~17 |
Нуклеофильные свойства.Нуклеофильные свойства спиртов проявляются в их реакциях с карбоновыми и неорганическими кислотами и их производными, которые приводят к образованию сложных эфиров.
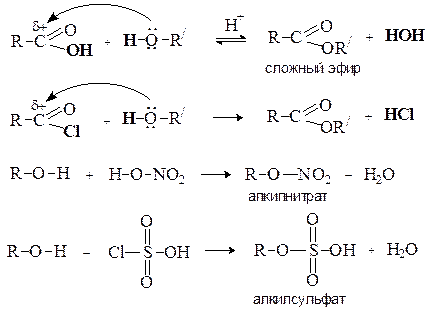
Для увеличения нуклеофильности спирты превращают в алкоголяты, которые способны взаимодействовать с галогенпроизводными с образованием простых эфиров:
R-Hal + R/ONa ® R-OR/ + NaHal
Однако алкоголят-ионы не только сильные нуклеофилы, но и сильные основания. Поэтому их взаимодействие с алкилгалогенидами может привести как к замещению, так и к элиминированию в зависимости от температуры и структуры алкилгалогенида и алкоголята. Например, для получения метилизопропилового эфира необходимо использовать метилиодид и изопропилат-анион, а не изопропилиодид и метилат-анион, так как в последнем случае будет доминировать реакция отщепления:
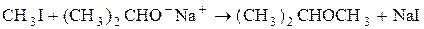 (
( 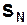 )
)
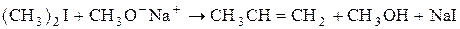 (E)
(E)
Основные свойства и реакции нуклеофильного замещения.Протекание реакции по схеме: R-OH + Y ® R-Y + OH-
невозможно, поскольку гидроксид-анион – это сильное основание и плохая уходящая группа. Для проведения 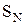 -реакций необходимо предварительно модифицировать ОН группу, превратив ее в хорошую уходящую группу. Для этого спирты переводят в оксониевые соединения или эфиры неорганических кислот:
-реакций необходимо предварительно модифицировать ОН группу, превратив ее в хорошую уходящую группу. Для этого спирты переводят в оксониевые соединения или эфиры неорганических кислот:
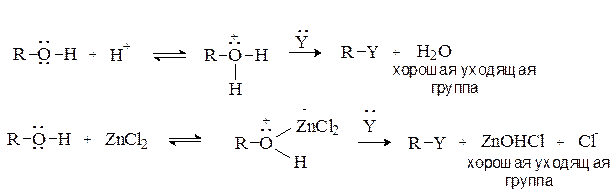
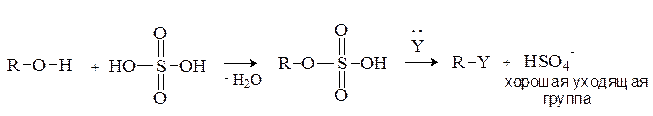
В биохимических процессах замещение ОН группы протекает через стадию превращения спиртов в эфиры фосфорной, дифосфорной и трифосфорной кислот, анионы которых являются легко уходящими группами:
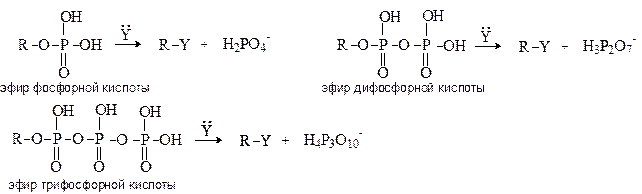
Замещение ОН группы на галоген.Спирты взаимодействуют с галогеноводородами и галогенидами фосфора и серы с образованием галогенпроизводных.
1) Действие галогеноводородов
R-OH + HHal ® R-Hal + 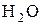
Реакция протекает через стадию протонирования ОН-группы с последующим нуклеофильным замещением по механизму 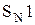 или
или 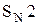 .
.
R-OH + HHal D 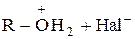 ® R-Hal +
® R-Hal + 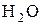
Первичные спирты реагируют по механизму 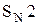 . Реакция идет медленно, так как в протонных растворителях (вода, спирты) галогенид-ионы – слабые нуклеофилы. Вторичные и третичные спирты реагируют по механизму
. Реакция идет медленно, так как в протонных растворителях (вода, спирты) галогенид-ионы – слабые нуклеофилы. Вторичные и третичные спирты реагируют по механизму 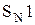 . Таким образом, реакционная способность спиртов возрастает в ряду:
. Таким образом, реакционная способность спиртов возрастает в ряду:
первичный < вторичный < третичный
Реакционная способность галогеноводородов увеличивается в ряду:
HCl < HBr < HI
параллельно с возрастанием силы кислот и нуклеофильности галогенид-анионов. Однако HI не может быть использована, так как легко восстанавливает спирты до углеводородов. HBr реагирует с первичными, вторичными и третичными спиртами. HCl при обычных условиях действует только на третичные спирты.
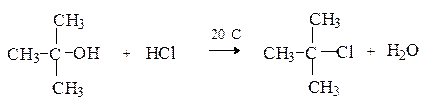
Для вторичных и первичных спиртов требуется присутствие катализатора – кислоты Льюиса.
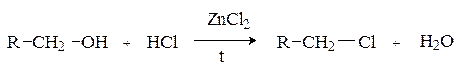
2) Действие галогенидов фосфора и серы
Замещение ОН группы действием 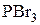 ,
, 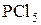 ,
, 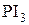 ,
, 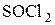 основано на предварительном превращении спирта в эфиры кислот фосфора и серы, которые затем атакуются галогенид-анионом.
основано на предварительном превращении спирта в эфиры кислот фосфора и серы, которые затем атакуются галогенид-анионом.
ROH + 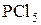 ® RCl +
® RCl + 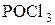 + HCl
+ HCl
ROH + 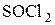 ® RCl +
® RCl + 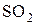 + HCl
+ HCl
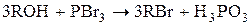
Образование простых эфиров.При нагревании спиртов в присутствии серной кислоты происходит замещение ОН группы на группу OR и образуются простые эфиры.
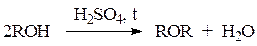
Реакция протекает через стадию протонирования спирта с последующим нуклеофильным замещением, в котором одна молекула спирта (протонированная) выполняет роль субстрата, а вторая – нуклеофила.
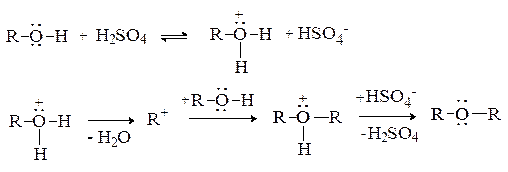
Дегидратация спиртов.При нагревании в присутствии кислотных катализаторов спирты отщепляют воду с образованием алкенов.
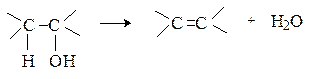
В случае вторичных и третичных спиртов процесс протекает по правилу Зайцева.
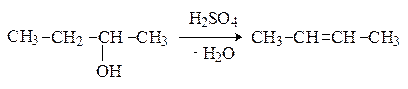
Дегидратация протекает преимущественно по механизму Е1 в соответствии со схемой:
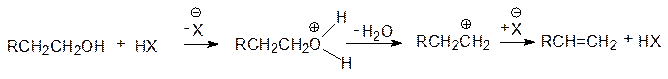
Х= 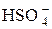
Атака аниона на промежуточно образующийся карбокатион может завершиться как отщеплением протона, так и присоединением к карбокатионному центру. Поэтому реакции дегидратации (элиминирования) протекают параллельно с образованием простых эфиров (нуклеофильным замещением). Склонность спиртов к дегидратации возрастает в ряду:
первичный < вторичный < третичный
Дегидратации способствует также высокая температура, например:
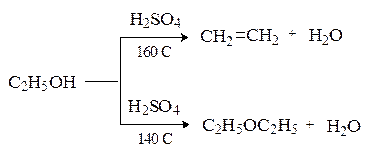
Окисление спиртов.Под окислением в органической химии понимают процессы, приводящие к обеднению субстрата водородом (дегидрирование) или к обогащению его кислородом. Окисление спиртов осуществляют при помощи двух основных приемов – дегидрирования и действия окислителей.
Дегидрирование
Первичные и вторичные спирты отщепляют водород при нагревании в присутствии медно-серебряного катализатора с образованием карбонильных соединений.
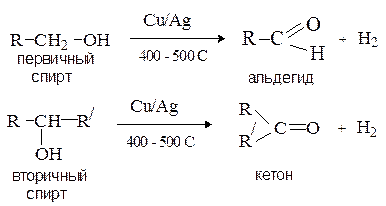
Третичные спирты в таких условиях не реагируют, а в более жестких – разрушаются.
Действие окислителей
Для окисления спиртов используют 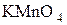 ,
, 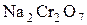 ,
, 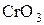 .
.
Первичные спирты окисляются до альдегидов, которые далее легко окисляются до карбоновых кислот.
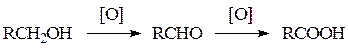
Реакцию можно остановить на стадии альдегида, если использовать кислый раствор дихромата натрия и отгонять образующийся альдегид из реакционной смеси:
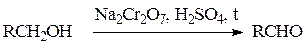
Вторичные спирты окисляются до кетонов под действием 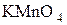 или
или 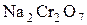 .
.
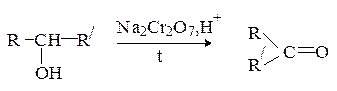
Окисление третичных спиртов протекает в жестких условиях и сопровождается деструкцией углеродного скелета.
Многоатомные спирты
Атомность спиртов определяется количеством гидроксильных групп. Двухатомные спирты содержат две гидроксильные группы и носят общее название диолы или гликоли. Трехатомные спирты называют триолами или глицеринами. Простейшие и наиболее важные представители диолов и триолов – этиленгликоль и глицерин.
Этиленгликоль (этандиол-1,2).
Этиленгликоль получают из этилена по следующим схемам:
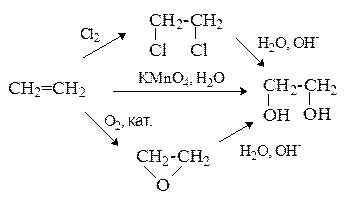
Химические свойства этиленгликоля аналогичны свойствам одноатомных спиртов. Однако есть ряд специфических свойств, обусловленных присутствием двух гидроксильных групп.
Этиленгликоль ( 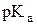 =15,1) является более сильной кислотой, чем одноатомные спирты и образует в водных растворах комплексные алкоголяты с ионами тяжелых металлов.
=15,1) является более сильной кислотой, чем одноатомные спирты и образует в водных растворах комплексные алкоголяты с ионами тяжелых металлов.
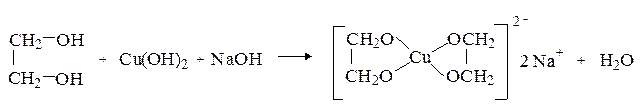
Появляющееся при этом ярко-синее окрашивание позволяет использовать реакцию как качественную на виц-диольный фрагмент.
При дегидратации этиленгликоля в зависимости от условий реакции образуются разные продукты. При нагревании в присутствии серной кислоты происходит межмолекулярная дегидратация с образованием циклического простого эфира – диоксана. Нагревание с хлоридом цинка дает продукт внутримолекулярной дегидратации – ацетальдегид.
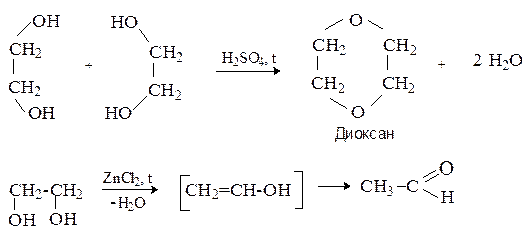
Этиленгликоль легко окисляется. В зависимости от природы окислителя могут образоваться гликолевый альдегид, глиоксаль, глиоксиловая кислота, щавелевая кислота.
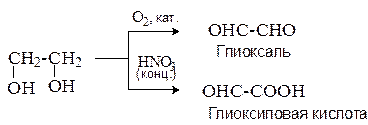
Этиленгликоль используется для приготовления антифризов; для получения растворителей (простые эфиры этиленгликоля, диоксан) и полимеров (полиэфиров).
Глицерин (1,2,3- пропантриол).
Глицерин ранее получали гидролизом жиров, но в настоящее время его получают синтетическим путем из пропилена.
Глицерин дает все реакции, известные для спиртов. Наличие трех гидроксильных групп обусловливает некоторые специфические свойства.
Глицерин ( 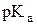 =14) является более сильной кислотой, чем одноатомные спирты и, подобно этиленгликолю, образует хелатные комплексы с ионами металлов.
=14) является более сильной кислотой, чем одноатомные спирты и, подобно этиленгликолю, образует хелатные комплексы с ионами металлов.
При дегидратации глицерина образуется ненасыщенный альдегид акролеин.
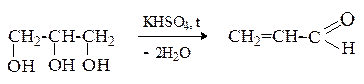
Мягкое окисление глицерина дает смесь глицеринового альдегида и дигидроксиацетона.
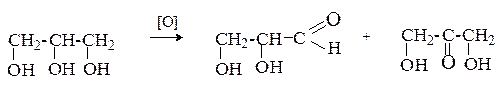
Важное значение имеют сложные эфиры глицерина. При действии на глицерин азотной кислоты в присутствии серной кислоты образуется тринитрат глицерина (нитроглицерин).
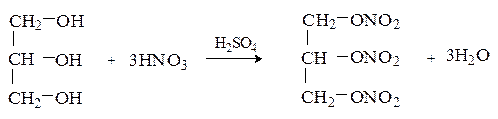
Нитроглицерин используется в производстве взрывчатых веществ. В малых концентрациях нитроглицерин применяется как сосудорасширяющее средство.
При действии на глицерин фосфорной кислоты образуется смесь a- и b-глицерофосфатов.
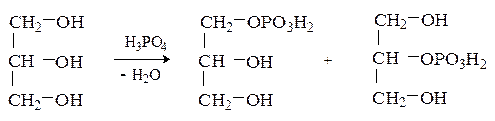
Глицерофосфаты являются структурными компонентами фосфолипидов (см.18.1.3) .
Сложные эфиры глицерина и высших жирных кислот – основная составная часть природных жиров и масел (см. 18.1.2).
Примерами многоатомных спиртов, содержащих четыре, пять и шесть гидроксильных групп, могут служить соответственно эритриты, пентиты и гекситы, которые образуются при восстановлении моносахаридов(см.17.1.5).
Фенолы
Классификация и номенклатура
По количеству ароматических ядер в молекуле различают собственно фенолы, а также нафтолы, антролы, фенантролы и др. По числу гидроксильных групп различают одно-, двух-, трех-, многоатомные фенолы.
Названия фенолов образуют от названий соответствующих аренов с добавлением суффикса –ол. Простейший фенол – гидроксибензол 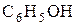 называют просто фенол. При наличии нескольких заместителей начало нумерации определяет гидроксильная группа и эти соединения рассматриваются как производные фенола. Иногда в соединениях сложного строения наличие гидроксильной группы обозначают префиксом гидрокси-. Многие фенолы имеют тривиальные названия.
называют просто фенол. При наличии нескольких заместителей начало нумерации определяет гидроксильная группа и эти соединения рассматриваются как производные фенола. Иногда в соединениях сложного строения наличие гидроксильной группы обозначают префиксом гидрокси-. Многие фенолы имеют тривиальные названия.
. 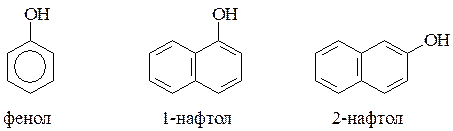
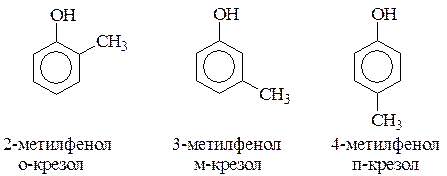
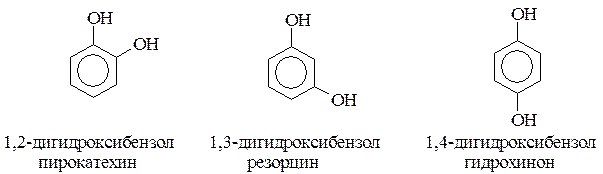
Методы получения
1) Сплавление солей сульфоновых кислот со щелочами.
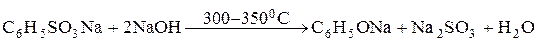
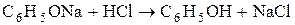
2) Щелочной гидролиз хлорбензола.
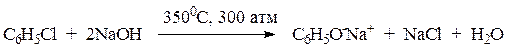
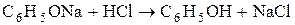
3)Кумольный метод.
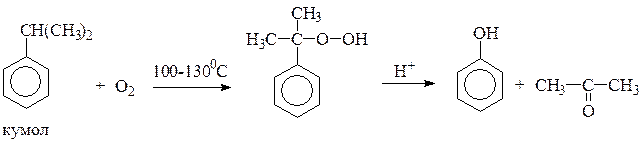
Физические свойства
Фенолы – жидкие или кристаллические вещества с сильным характерным запахом. При хранении на воздухе быстро темнеют из-за окисления. Ограниченно растворимы в воде.
