Лекция: поверхностные явления и адсорбция
ПРИРОДА ПОВЕРХНОСТНОЙ ЭНЕРГИИ
К поверхностным явлениям относят те эффекты и особенности поведения веществ, которые наблюдаются на поверхностях раздела фаз. Причиной поверхностных явлений служит особое состояние молекул в слоях жидкостей и твёрдых тел, непосредственно прилегающих к поверхностям раздела фаз.
Рассмотрим систему, состоящую из жидкости и газа. Силы межмолекулярного взаимодействия внутри жидкости F1,1 больше сил взаимодействия между молекулами газа F2,2.
Если молекула А находится внутри жидкости, то на неё со всех сторон действуют силы взаимодействия таких же молекул. Эти силы уравновешивают друг друга.
Если же, например, молекула В находится на поверхности жидкости, т.е. на межфазной поверхности, то с одной стороны на неё действуют силы взаимодействия таких же молекул, а с другой – молекул газа. Поскольку силы F1,1 › F2,2, возникает результирующая сила Р, направленная в глубь жидкости. Эта сила вталкивает молекулу “В” в глубь жидкости. Эту силу часто называют ВНУТРЕННИМ ДАВЛЕНИЕМ. Под внутренним давлением жидкости понимают силу притяжения между молекулами жидкости в её объёме. Для этой силы можно записать:
Р = F1,1 - F2,2
Чем сильнее различаются силы F1,1 и F2,2 , тем больше Р. Величина внутреннего давления жидкостей, особенно полярных, очень велика, порядка 10 8 Па.
Для создания единицы площади поверхности жидкости надо совершить работу, преодолеть силу внутреннего давления и совершить работу. Если увеличение площади поверхности производится при постоянных давлении и температуре (изобарно-изотермический процесс) или при постоянных давлении и температуре (изохорно-изотермический процесс), то такое увеличение площади поверхности сопровождается увеличением поверхностной энергии системы (энергии Гиббса).
Бесконечно малое изменение поверхностной энергии Гиббса с изменением величины поверхности при постоянных р и Т равно
dG = σdS
где dS – бесконечно малое изменение площади поверхности; σ – коэффициент поверхностного натяжения.
ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ (σ) является важной характеристикой поверхности. Оно характеризует избыток поверхностной энергии, приходящейся на 1 м2 межфазной поверхности.
ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ (σ) РАВНО ТЕРМОДИНАМИЧЕСКИ ОБРАТИМОЙ, ИЗОТЕРМИЧЕСКОЙ РАБОТЕ, КОТОРУЮ НАДО СОВЕРШИТЬ, ЧТОБЫ УВЕЛИЧИТЬ ПЛОЩАДЬ МЕЖФАЗНОЙ ПОВЕРХНОСТИ НА ЕДИНИЦУ
σ = - ∆А/∆S
∆А – это термодинамически обратимая работа, затраченная на образование поверхности площадью ∆S. Так как работа совершается над системой, то она является отрицательной.
Поверхностное натяжение (или коэффициент поверхностного натяжения) является важной характеристикой любой жидкости. Физический смысл поверхностного натяжения может иметь энергетическое и силовое выражения.
Согласно энергетическому выражению, поверхностное натяжение σ есть поверхностная энергия Гиббса единицы поверхности (т.е. удельная поверхностная энергия Гиббса). В таком случае σ равна работе, затраченной на образование единицы поверхности. Энергетической единицей σ является Дж/м2.
Силовое определение поверхностного натяжения формулируется следующим образом: σ – это сила, действующая на поверхности по касательной к ней и стремящаяся сократить свободную поверхность тела до наименьших возможных пределов при данном объёме. В этом случае единицей измерения σ является Н/м.
Поверхностное натяжение характеризует различия в интенсивности межмолекулярных взаимодействий на границе раздела фаз. Чем больше это различие, тем больше σ. Для границы жидкая фаза – воздух можно пренебречь межмолекулярным взаимодействием в воздухе (Fгаз-газ = 0), поэтому поверхностное натяжение характеризует интенсивность межмолекулярных взаимодействий в конденсированной фазе.
Поверхностное натяжение индивидуальных веществ на границе с газом понижается с повышением температуры: dσ/dt ‹ 0. Температурный коэффициент dσ/dt имеет практически постоянное отрицательное значение вплоть до температур близких к критическим. При критической температуре исчезают различия между граничащими фазами и поверностное натяжение становится равным 0 (σ = 0).
Для многих неполярных жидкостей температурная зависимость σ от Т линейна и в первом приближении может быть представлена формулой:
σ = σ0 – а(Т – Т0),
где σ и σ0 – поверхностное натяжение при Т и Т0, а – постоянная, равная температурному коэффициенту поверхностного натяжения, взятому с обратным знаком.
САМОПРОИЗВОЛЬНЫЕ ПРОЦЕССЫ В ПОВЕРХНОСТНОМ СЛОЕ
Для индивидуальных веществ поверхностное натяжение постоянно (σ = Const, dσ = 0). В этих случаях самопроизвольно могут протекать процессы, сопровождающиеся уменьшением площади межфазной поверхности (dS1,2 ‹ 0). К таким явлениям относят:
ü Стремление капель жидкости или пузырьков газа принять сферическую форму (сферические частицы имеют самую маленькую удельную поверхность);
ü Слипание твердых частицу дисперсной фазы (коагуляция);
ü Слипание капель в эмульсиях или пузырьков газа в пенах (коалесценция);
ü Рост кристаллов.
Если площадь межфазной поверхности остается постоянной (S1,2 = const, dS1,2 = 0), то могут протекать самопроизвольно процессы за счёт уменьшения поверхностного натяжения (d σ ‹ 0), которые могут быть обусловлены процессом адсорбции.
АДСОРБЦИЯ, ОСНОВНЫЕ ТЕРМИНЫ
АДСОРБЦИЕЙ НАЗЫВАЕТСЯ САМОПРОИЗВОЛЬНОЕ ИЗМЕНЕНИЕ КОНЦЕНТРАЦИИ КОМПОНЕНТА В ПОВЕРХНОСТНОМ СЛОЕ ПО СРАВНЕНИЮ С ЕГО КОНЦЕНТРАЦИЕЙ В ОБЪЕМЕ
Введем основные термины:
Ø АДСОРБЕНТОМ называется вещество, на котором адсорбируются молекулы других веществ;
Ø АДСОРБТИВОМ называется вещество, молекулы которого адсорбируются на адсорбенте;
Ø АДСОРБАТОМ называется уже адсорбированное вещество;
Ø ДЕСОРБЦИЕЙ называется процесс, обратный адсорбции.
В зависимости от природы сил, действующих между адсорбентом и адсорбатом различают физическую и химическую адсорбции.
ХИМИЧЕСКАЯ АДСОРБЦИЯ осуществляется при взаимодействии адсорбента с адсорбатом с образованием химической связи. Энергия возникающих при этом связей 40 – 400 кДж/моль. Хемсорбция практически необратима, специфична и локализована. Повышение температуры усиливает адсорбцию.
ФИЗИЧЕСКАЯ АДСОРБЦИЯ обусловлена межмолекулярным взаимодействием за счёт сил Ван-дер-Ваальса (ориентационных, индукционных и дисперсионных) или водородной связью. Поэтому для этого вида адсорбции характерны: обратимость, неспецефичность, экзотермичность.
ЗАВИСИМОСТЬ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ ОТ ПРИРОДЫ И КОНЦЕНТРАЦИИ РАСТВОРЁННОГО ВЕЩЕСТВА
Эксперимент показал, что различные растворённые вещества по-разному влияют на поверхностное натяжение растворов.
1. Вещества, понижающие поверхностное натяжение называют поверхностно-активными (ПАВ). По отношению к водным растворам ПАВ являются спирты, жирные кислоты и их соли, амины и другие вещества, имеющие дифильное строение молекул, т.е. полярную часть (функциональные группы) и неполярную часть (углеводородный радикал). Молекулы ПАВ принято изображать так:
---------------------------------О
Неполярная часть полярная часть
Поверхностно-активными по отношению к воде являются вещества менее полярные, чем вода. Они взаимодействуют с водой слабее, чем молекулы воды между собой, значит, попадая на поверхность, они уменьшают поверхностное натяжение.
2. Вещества, повышающие поверхностное натяжение, называются поверхностно-инактивными (ПИВ). К ним относятся сильные электролиты: соли, кислоты, щёлочи. Ионы, образующиеся в результате диссоциации, взаимодействуют с водой сильнее, чем молекулы воды между собой. Поэтому значительная часть ионов увлекается молекулами воды в объём раствора. Однако немногие оставшиеся на поверхности ионы создают вблизи поверхности силовое поле, тем самым повышая поверностное натяжение.
3. Существуют вещества, растворение которых практически не приводит к изменению поверностного натяжения. Такие вещества являются поверхностно-неактивными. К ним относятся вещества, имеющие много полярных групп, например, сахароза С12Н22О11.
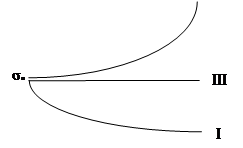
Всё многообразие зависимостей поверхностного натяжения от концентрации может быть представлено кривыми трёх типов:
| |||
| |||
|
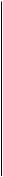
 |
|
| |
 |
Рис. 1. Зависимость поверхностного натяжения водного раствора от концентрации ПАВ (1); ПИВ (2) и не влияющих на величину поверхностного натяжения веществ ПНВ (3).
Из графика видно, что для ПАВ 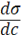 < 0, для ПИВ
< 0, для ПИВ 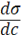 > 0, а для ПНВ
> 0, а для ПНВ 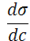 = 0. На графике σ0 – поверхностное натяжение воды. Отметим, что для ПАВ характерно резкое снижение σ даже при малых концентрациях. По мере роста концентрации ПАВ график становится более пологим и, наконец, переходит в горизонтальную прямую, что означает, что поверхностное натяжение достигло своего минимального значения. Увеличение σ под влиянием ПИВ происходит незначительно, что связано с тем, что концентрация ионов в поверхностном слое незначительна и по составу он близок к чистому растворителю.
= 0. На графике σ0 – поверхностное натяжение воды. Отметим, что для ПАВ характерно резкое снижение σ даже при малых концентрациях. По мере роста концентрации ПАВ график становится более пологим и, наконец, переходит в горизонтальную прямую, что означает, что поверхностное натяжение достигло своего минимального значения. Увеличение σ под влиянием ПИВ происходит незначительно, что связано с тем, что концентрация ионов в поверхностном слое незначительна и по составу он близок к чистому растворителю.
Отметим, что понятия ПАВ и ПИВ не носят абсолютный характер, они определяются выбранным растворителем, его поверхностным натяжением.
АДСОРБЦИЯ НА ПОВЕРХНОСТИ РАСТВОРОВ. УРАВНЕНИЕ ГИББСА
Изменение концентрации растворённого вещества в поверхностном слое раствора (или вообще на границе раздела фаз) называется адсорбцией.
Дж. Гиббс на основе второго закона термодинамики в 70-х гг. XIX в. вывел важное уравнение, связывающее величину адсорбции со способностью растворённого вещества изменять поверхностное натяжение раствора:
Г = 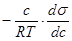
где Г – количество адсорбированного вещества, моль/м2; с – молярная концентрация растворённого вещества, моль/дм3, Т – температура, при которой происходит адсорбция, R – газовая постоянная, 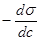 – поверхностная активность.
– поверхностная активность.
Уравнение Гиббса отражает следующую зависимость: чем сильнее уменьшается поверхностное натяжение с увеличением концентрации адсорбируемого вещества, тем больше его поверхностная активность. Это свидетельствует о том, что знак «минус» указывает на обратную зависимость между величиной адсорбции Г и поверхностным натяжением σ.
Если 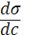 < 0, то Г > 0, т.е. адсорбция положительна (вещество накапливается на поверхности раздела фаз), это характерно для ПАВ. Если же
< 0, то Г > 0, т.е. адсорбция положительна (вещество накапливается на поверхности раздела фаз), это характерно для ПАВ. Если же 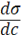 > 0, то Г < 0, т.е. адсорбция отрицательна (вещество накапливается в объёме), это характерно для ПИВ.
> 0, то Г < 0, т.е. адсорбция отрицательна (вещество накапливается в объёме), это характерно для ПИВ.
Адсорбция вещества – обратимый процесс, заканчивающийся установлением адсорбционного равновесия, при котором скорость адсорбции равна скорости обратного процесса – десорбции.
Рассмотрим изотерму адсорбции Гиббса (Рис. 2):
|
 |
 |
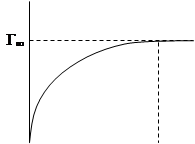
Рис. 2. Изотерма адсорбции Гиббса.
Из графика видно, что по мере увеличения концентрации вещества адсорбция возрастает вначале резко, а затем всё медленнее и медленнее, асимптотически приближаясь к некоторой величине предельной адсорбции Г∞. Существование предельного значения адсорбции понятно, так как поверхность раствора имеет определённую площадь и при достижении определённой концентрации ПАВ в растворе (С∞) она оказывается полностью занятой молекулами ПАВ. Поскольку адсорбция мономолекулярна (однослойна), дальнейшее увеличение концентрации ПАВ в растворе ничего не может изменить в поверхностном слое.
ПОВЕРХНОСТНАЯ АКТИВНОСТЬ
Из уравнения Гиббса следует, что характеристикой поведения вещества при адсорбции является величина производной dσ/dc, однако её значение изменяется при изменении концентрации. Советский академик П.А. Ребиндер, чтобы придать этой величине вид характеристической постоянной, предложил брать предельное значение величины dσ/dc (при с → 0). Это предельное значение он назвал поверхностной активностью g:
g = -( dσ/dc)c → 0
Размерность: Дж∙м3/м2∙моль = Дж∙м/моль или Н∙м2/моль
Чем в большей степени уменьшается поверхностное натяжение с увеличением концентрации адсорбируемого вещества, тем больше поверхностная активность этого вещества, и тем больше его гиббсовая адсорбция.
В честь Гиббса величину - dσ/dc обозначают буквой G и называют гибсом. В этом случае уравнение Гиббса принимает более простую форму:
Г = с/RT∙G
Откуда: G = - dσ/dc = RTГ/c (эрг ∙ см/моль)
ПРАВИЛО ДЮКЛО-ТРАУБЕ
Адсорбция одного ПАВ и того же гомологического ряда меняется в соответствии с правилом Дюкло-Траубе:
С РОСТОМ ДЛИНЫ УГЛЕВОДОРОДНОГО РАДИКАЛА МОЛЕКУЛ ПАВ НА ГРУППУ –СН2- АДСОРБЦИЯ ВЕЩЕСТВА УВЕЛИЧИВАЕТСЯ В 3 – 3,5 РАЗА
ОРИЕНТАЦИЯ МОЛЕКУЛ ПАВ В ПОВЕРХНОСТНОМ СЛОЕ
В 1915 г Ленгмюр ввел понятие об ориентации молекул ПАВ в поверхностном слое.
[Ленгмюр Ирвинг (1881-1957), американский физик и физико-химик. Труды по электрическим разрядам в газах, термоэлектронной эмиссии, вакуумной технике и др. Исследовал поверхностные явления (адсорбция, мономолекурные слои и др.). Нобелевская премия (1932).]
Исходя из строения молекул ПАВ, Ленгмюр сформулировал принцип независимости поверхностного действия, заключающийся в том, что при адсорбции полярная группа молекулы, обладающая большим сродством к полярной фазе, втягивается в воду, в то время как неполярный радикал выталкивается в неполярную фазу. Происходящее при этом уменьшение свободной поверхностной энергии ограничивает размеры поверхностного слоя толщиной в одну молекулу. Образуется мономолекулярный слой.
При малых концентрациях ПАВ углеводородные радикалы «лежат» на поверхности полярной жидкости, а полярные группировки погружены в неё. Затем по мере роста концентрации ПАВ, они (неполярные радикалы) начинают подниматься. В насыщенном адсорбционном слое поверхность воды оказывается сплошь покрытой «частоколом Ленгмюра» из вертикально ориентированных молекул ПАВ. Значение поверхностного натяжения в этом случае приближается к значению, характерному для чистого ПАВ на границе с воздухом.
 |  |  |  |  |  |  |  |  | |||||||||||||
 | |||||||||||||||||||||
 | |||||||||||||||||||||




















А) малые концентрации ПАВ Б) умеренные концентрации В) насыщенный адсорбционный слой
Рис. 3. Ориентация молекул ПАВ на поверхности водного раствора.
Из-за вертикальной ориентации ПАВ в поверхностном слое максимальная адсорбция (Г∞) не зависит от длины «хвоста» (длины углеродного радикала), а определяется только размерами поперечного сечения молекулы, которые в гомологическом ряду остаются неизменными. Экспериментально найденная величина Г∞ даёт возможность вычислить поперечный размер молекулы S0:
S0 = 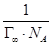
Представления об ориентации молекул ПАВ в насыщенном адсорбционном слое сыграли большую роль в развитии учения о структуре биологических мембран. Клеточные мембраны образованы главным образом молекулами двух типов: липидами и белками.
Липиды не растворимы в воде, но растворимы в органических растворителях. Особенностью мембранных липидов является то, что на одном конце их молекулы есть полярные группы (например –СООН), обладающие гидрофильными свойствами, тогда как другой её конец представляет собой длинную углеводородную цепь с гидрофобными свойствами.
Липиды биомембран расположены двумя слоями. Обычно говорят о двухслойной структуре. Каждый (моно) слой состоит из сложных липидов (и иногда холестерина), расположенных таким образом, что неполярные гидрофобные хвосты молекул находятся в тесном контакте друг с другом; в таком же контакте полярные гидрофильные элементы. Все взаимодействия имеют исключительно нековалентный характер. Два монослоя совмещаются, ориентируясь «хвост к хвосту», так, что образуется структура двойного слоя, имеющая неполярную внутреннюю часть и две полярные поверхности. Толщина липидного слоя примерно 3,5 – 4 нм.
Молекулы белка могут располагаться вблизи внешней и внутренней поверхностей мембраны, а также проникать, частично или полностью, через всю её толщину. Обычно клеточные мембраны весьма прочны и обладают свойствами электрического изолятора.
Биологические мембраны не являются жесткими структурами. Например, во многих случаях белки и липиды внутри мембран находятся в постоянном движении.
| | |||
| | |||
АДСОРБЦИЯ НА НЕПОДВИЖНОЙ ГРАНИЦЕ РАЗДЕЛА ФАЗ
(НА ПОВЕРХНОСТИ ТВЁРДОГО ВЕЩЕСТВА)
УДЕЛЬНАЯ ДСОРБЦИЯ
При адсорбции на поверхности твёрдых адсорбентов изменяется химический состав поверхности адсорбента. Количественной характеристикой этого процесса является величина удельной адсорбции Г.
УДЕЛЬНАЯ АДСОРБЦИЯ – ЭТО РАВНОВЕСНОЕ КОЛИЧЕСТВО ПОГЛОЩАЕМОГО ВЕЩЕСТВА, ПРИХОДЯЩЕЕСЯ НА ЕДИНИЦУ ПОВЕРХНОСТИ ИЛИ МАССЫ ТВЁРДОГО АДСОРБЕНТА
В качестве адсорбентов обычно применяют мелкоизмельчённые вещества или пористые тела, что обеспечивает большую площадь поверхности раздела фаз, которую определить практически невозможно. Поэтому удельная адсорбция для твёрдых адсорбентов преимущественно выражается в молях поглощённого вещества на единицу массы адсорбента:
Г =  (моль/г)
(моль/г)
где n – количество адсорбата, моль; m – масса адсорбента, г.
Адсорбция газов и паров адсорбата на твёрдых адсорбентах – процесс, протекающий за счёт сил Ван-дер-Ваальса и водородных связей. Количество поглощённого газа или пара зависит от следующих факторов.
1. От свободной поверхностной энергии адсорбента. Она весьма велика у адсорбентов с аморфной структурой (активированный уголь) и у кристаллических веществ (оксиды алюминия, кремния). Адсорбент тем эффективнее, чем мельче измельчен.
2. От сродства адсорбтива к поверхности адсорбента. Полярные вещества лучше адсорбируются на полярных адсорбентах, а неполярные на неполярных. Чем больше адсорбент склонен к межмолекулярным взаимодействиям, тем интенсивнее идет адсорбция.
3. При физической адсорбции из смеси газов или паров лучше адсорбируется тот компонент, который легче сжимается, поскольку его молекулы более склонны к межмолекулярным взаимодействиям.
4. От концентрации адсорбата. Зависимость имеет сложный характер, так как с адсорбцией идет одновременно процесс десорбции. При равенстве скоростей этих процессов наступает равновесие.
ТЕОРИЯ МОНОМОЛЕКУЛЯРНОЙ АДСОРБЦИИ ЛЕНГМЮРА. УРАВНЕНИЕ ЛЕНГМЮРА
Изучая адсорбцию на твердых поверхностях Ленгмюр предложил теорию мономолекулярной адсорбции и уравнение адсорбции. Основные положения теории Ленгмюра следующие:
v адсорбция молекул происходит не на всей поверхности адсорбента, а только на адсорбционных центрах, где имеются участки с наиболее нескомпенсированными силовыми полями;
v каждый адсорбционный центр может удерживать только одну молекулу адсорбата, при этом адсорбированные молекулы не взаимодействуют со свободными молекулами, что приводит к образованию мономолекулярного слоя поглощаемого вещества;
v процесс адсорбции обратим и носит динамический характер, т.к. адсорбированные молекулы удерживаются адсорбционными центрами только в течение определенного промежутка времени, после чего происходит десорбция этих молекул и адсорбция такого же числа новых молекул.
Исходя из этих положений, Ленгмюр предложил уравнение адсорбции:
Г = 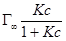
Где Г∞ - значение предельной адсорбции; с – равновесная концентрация адсорбента в системе; К – константа адсорбционного равновесия.
Зависимость адсорбции от концентрации ПАВ (изотерма адсорбции) имеет вид:
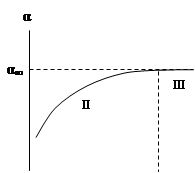 |

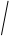
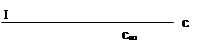 |
Рис. 4. Зависимость адсорбции от концентрации ПАВ
На кривой четко видны три участка:
I - ый участок – это прямая линия, выходящая из начала координат. Действительно, при малых концентрациях, когда с → 0 и (1 + Кс) ≈1, уравнение принимает вид Г = Г∞·Кс, т.е. величина адсорбции прямо пропорциональна концентрации или давлению адсорбата.
III – участок – соответствует прямой, параллельной оси абсцисс, что означает, что адсорбция достигла своего предельного значения. При этом Кс ›› 1 и (1 + Кс) ≈ Кс, тогда Г = Г∞ (произошло насыщение поверхности адсорбента молекулами адсорбата, так как сформировался мономолекулярный слой).
II – ой участок соответствует криволинейной части графика и описывается полным уравнением Ленгмюра.
АДСОРБЦИЯ НА ГРАНИЦЕ ТВЕРДОЕ ТЕЛО – ЖИДКОСТЬ
Существенным отличием адсорбции веществ из растворов является конкуренция между растворенным веществом и растворителем за возможность взаимодействовать с адсорбционными центрами на поверхности твердого адсорбента. Рассматривая этот вид адсорбции остановимся на следующем:
1. При адсорбции из раствора важным фактором является величина удельной поверхности адсорбента и его сродство к поглощаемому веществу. Гидрофильные адсорбенты (силикагель, глины, пористые стекла) хорошо поглощают полярные вещества, а гидрофобные (сажа, активированный уголь) -–неполярные вещества.
2. Природа растворителя:
Чем хуже данный растворитель смачивает поверхность адсорбента и чем хуже растворяет вещество, тем лучше будет происходить адсорбция растворенного вещества.
Природа поглощаемого вещества:
а) выполняется правило «подобное взаимодействует с подобным», т.е. должно быть сродство между адсорбентом и адсорбтивом; б) Выполняется правило Шилова:
Чем больше растворимость вещества в данном растворителе, тем хуже оно адсорбируется на поверхности твердого адсорбента.
в) правило Ребиндера:
На поверхности раздела фаз прежде всего адсорбируются те вещества, при адсорбции которых происходит выравнивание полярностей соприкасающихся фаз, причём с увеличением разности полярности фаз способность к адсорбции этих веществ возрастае
Эффективней всего адсорбируются молекулы веществ, имеющих дифильное строение. В этом случае идёт эффективная адсорбция на твердом адсорбенте с самопроизвольной четкой ориентацией их молекул на границе раздела, выравнивающей полярности фаз. Полярный фрагмент молекулы обращен всегда к полярной фазе – к воде, силикагелю, а неполярный фрагмент – к неполярной (гидрофобной) фазе – активированному углю, маслу.
3. Влияние концентрации растворенного вещества на процесс адсорбции при постоянной Т описывается уравнением Ленгмюра.
4. Повышение температуры снижает эффективность адсорбции. Объясняется это ослаблением взаимодействия между адсорбентом и адсорбатом.
Молекулярная адсорбция из растворов на твердом адсорбенте широко используется в медицинской практике. Активированный уголь хорошо адсорбирует газы, алкалоиды, барбитураты, токсины из пищеварительной системы. Одна таблетка активированного угля массой 0,25 г имеет адсорбционную поверхность около 100 м2.
АДСОРБЦИЯ РАСТВОРЁННОГО В ЖИДКОСТИ ВЕЩЕСТВА НА ТВЁРДОМ АДСОРБЕНТЕ
Различают молекулярную и ионную адсорбцию.
Молекулярная адсорбция – это адсорбция из растворов неэлектролитов (или очень слабых электролитов). При молекулярной адсорбции вещество адсорбируется на поверхности твёрдого тела в виде молекул.
Особенности молекулярной адсорбции: наряду с растворённым веществом адсорбируются молекулы растворителя. Поэтому для адсорбции растворённого вещества его молекулы должны вытеснять с поверхности молекулы растворителя.
Экспериментально величину адсорбции «а» изучают измеряя молярную концентрацию раствора до контакта с адсорбентом (с0) и после наступления адсорбционного равновесия (сs):
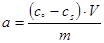 моль/г,
моль/г,
а – количество адсорбированного вещества, приходящееся на 1 г адсорбента; m – масса адсорбента, г: V – объём раствора, из которого идёт адсорбция, л.
На молекулярную адсорбцию влияют:
ü равновесная концентрация растворённого вещества;
ü природа растворителя;
ü природа адсорбента;
ü природа растворённого вещества;
ü температура, время адсорбции.
Ионная адсорбция – это адсорбция из растворов сильных электролитов; в этом случае адсорбируется растворённое вещество на поверхности твёрдого адсорбента в виде ионов.
Ионная адсорбция – процесс более сложный, так как в растворе присутствуют уже частицы как минимум 3 видов: катионы, анионы растворённого вещества и молекулы растворителя.
Особенности ионной адсорбции:
1. Адсорбируются заряженные частицы (ионы), а не молекулы.
2. Адсорбция происходит только на полярных адсорбентах, поэтому её часто называют полярной адсорбцией.
3. Адсорбция сопровождается образованием двойного электрического слоя (ДЭС).
4. Адсорбция является избирательной, т.е. на каждом данном адсорбенте катионы и анионы адсорбируются неодинаково.
5. В основе ионной адсорбции лежат химические силы, и она чаще всего кинетически необратима.
6. Для ионной адсорбции характерно явление обменной адсорбции.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ИОННУЮ АДСОРБЦИЮ
1. Химическая природа адсорбента
Чем более полярным является адсорбент, тем лучше он адсорбирует ионы из водных растворов. На активных центрах, несущих положительный заряд, адсорбируются анионы, на отрицательных - катионы.
2. Химическая природа ионов
а) На адсорбцию ионов большое влияние оказывает величина радиуса иона. Чем больше кристаллический радиус иона при одинаковом заряде, тем лучше он адсорбируется, так как с увеличением кристаллического радиуса иона возрастает его поляризуемость, а следовательно, способность притягиваться к полярной поверхности – адсорбироваться на ней. Одновременно увеличение кристаллического радиуса приводит к уменьшению гидратации иона, а это облегчает адсорбцию. В соответствии с этим ионы можно расположить в ряды по возрастающей способности к адсорбции. Эти ряды называют лиотропными рядами или рядами Гофмейстера:
Li+ ‹ Na + ‹ K + ‹ Rb + ‹ Cs +
Mg 2+ ‹ Са 2+ ‹ Sr 2+ ‹ Ва 2+
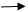 Cl ‾ ‹ Br ‾ ‹ NO3 ‾ ‹ I ‾ ‹ NCS ‾
Cl ‾ ‹ Br ‾ ‹ NO3 ‾ ‹ I ‾ ‹ NCS ‾
Адсорбционная способность возрастает
б) Чем больше заряд иона, тем сильнее ион притягивается противоположно заряженной поверхностью твердого тела, тем сильнее адсорбция:
K + ‹‹ Са 2+ ‹‹ Al 3+
 Усиление адсорбции
Усиление адсорбции
Особый интерес представляет адсорбция ионов поверхностью кристалла, в состав которого входят такие же ионы или родственные ионы. В этом случае адсорбцию можно рассматривать как кристаллизацию, т.е. достройку кристаллической решетки способными адсорбироваться на ней ионами. Это позволило Панету и Фаянсу сформулировать следующее правило:
На кристаллической поверхности адсорбента адсорбируются те ионы, которые способны достраивать кристаллическую решетку и дают труднорастворимое соединение с ионами, входящими в состав кристалла.
Пример:
 | |||
 | |||
|
|
 nAgCl + K+ + Cl- → nAgCl
nAgCl + K+ + Cl- → nAgCl [Панет Фридрих Адольф (1887 – 1958), немецкий химик. Первым исследовал абсолютный возраст метеоритов, один из авторов правила Фаянса-Панета.
Фаянс Казимир (1887-1975), американский физико-химик, иностранный член-корреспондент АН СССР с 1924 года, труды в области радиохимии. Установил вместе с Ф. Панетом праило Фаянса-Панета).]
ИОНООБМЕННАЯ АДСОРБЦИЯ
Ионообменная адсорбция – это процесс, при котором твёрдый адсорбент обменивает свои ионы на ионы такого же знака заряда, находящиеся в растворе.
Для ионообменной адсорбции характерно следующее:
¨ эта адсорбция специфична, т.е. к обмену способны только определённые ионы, по своей природе этот процесс приближается к химическим явлениям;
¨ ионообменная адсорбция не всегда обратима;
¨ протекает медленнее, чем молекулярная адсорбция;
¨ при ионообменной адсорбции может меняться рН среды.
Вещества, проявляющие способность к ионному обмену при контакте с растворами электролитов, называются ионитами. Большинство ионитов – твёрдые, нерастворимые, ограниченно набухающие вещества. Иониты состоят из каркаса, несущего положительный или отрицательный заряд, и подвижных противоионов, которые компенсируют своими зарядами заряд каркаса и стехиометрически обмениваются на противоионы раствора электролита.
По знаку заряда обменивающихся ионов иониты делят на катиониты, аниониты и амфолиты.
По химической природе каркаса – на неорганические, органические и минерально-органические. Неорганические и органические иониты могут быть природными (целлюлоза, древесина, торф) и синтетическими (силикагель, Al2O3, наиболее важны ионообменные смолы). Минерально-органические состоят из органического полиэлектролита на минеральном носителе.
Иониты применяются для очистки, разделения и концентрирования веществ из водных органических и газообразных сред. Например: очистка сточных вод, лекарственных веществ, сахара, выделение ценных металлов и т. д.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
(по теме «Поверхностная энергия. Адсорбция»)
1. Какова причина возникновения избыточной поверхностной энергии?
2. Что называется поверхностным натяжением? От чего зависит величина поверхностного натяжения?
3. В чём заключаются причины самопроизвольных поверхностных явлений?
4. Какие поверхностные явления связаны с уменьшением величины межфазной поверхности?
5. Что называется адсорбцией? Чем она обусловлена?
6. Чем можно объяснить, что деревянную палочку диаметром 1 см сломать легко, а стальной стержень такого же диаметра – практически невозможно?
7. Какие вещества называются поверхностно-активными, поверхностно-инактивными?
8. В чём состоят особенности строения молекул ПАВ и ПИВ и их адсорбции?
9. Как зависит поверхностное натяжение от концентрации ПАВ в растворе?
10. Уравнение Гиббса, его анализ. Ориентация молекул в поверхностном слое; структура липидного биослоя.
11. Чем отличается физическая адсорбция от хемосорбции?
12. Что называется поверхностной активностью? Как её можно определить графически и аналитически?
13. В чём заключается правило Дюкло-Траубе?
14. Как графически можно определить предельную адсорбцию?
15. В чём состоят особенности газов и паров на твёрдых поверхностях?
16. Какие участки есть на изотерме Ленгмюра? Какие математические уравнения характеризуют каждый участок?
17. Перечислите основные положения теории Ленгмюра.
18. Как с помощью теории Ленгмюра можно объяснить ступенчатую адсорбцию?
19. От каких факторов зависит адсорбция на пористых адсорбентах?
20. Какие свойства газов влияют на их адсорбцию.
21. Что является причиной адсорбции растворённых веществ на поверхности твёрдых тел?
22. Какая адсорбция является молекулярной, от каких факторов она зависит?
23. Как зависит молекулярная адсорбция от природы растворённого вещества, растворителя и адсорбента?
24. Перечислите особенности ионной адсорбции. Как она зависит от размеров и зарядов ионов?
25. Сформулируйте правило Панета –Фаянса.
26. В чём сущность ионообменной адсорбции? Какое состояние называется ионообменным равновесием? Какая величина его характеризует?
27. Какие поверхности называются гидрофильными, гидрофобными?
