Производство черных и цветных металлов
18.4.1 Получение чугуна
Исходными материалами для получения чугуна служат железные руды, топливо и флюсы. В железных рудах основной составляющей частью являются оксиды железа. Кроме них руды содержат пустую породу, состоящую из других оксидов металлов, а также неметаллических включений – глинозема, известняка, песка.
Для выплавки чугуна применяют магнитный железняк Fe3O4 с содержанием железа до 70 %, красный железняк Fe2O3 с содержанием железа 50–60 %, бурый железняк Fе2Оз Н2О c содержанием железа около 30 % ∙ и шпатовый железняк с содержанием железа до 30–40 % в виде FeCO3.
Топливом служит кокс, получаемый сухой перегонкой (без доступа воздуха) отдельных видов каменных углей. Он же является восстановителем железа.
В качестве флюсов (плавней) применяются известняк, доломит, кварцевый песок. Их назначение – понизить температуру плавления пустой породы и для перевода ее и золы топлива в шлак.
Восстановление железа из оксидов и отделение руды от пустой породы выполняется в доменной печи (рисунок 18.10)
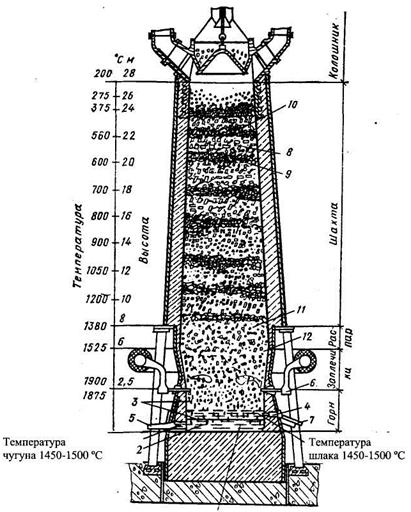
Рисунок18.10 – Схема доменной печи: 1 – жидкий чугун; 2 – чугунная летка; 3 – жидкий шлак; 4 – шлаковая летка; 5 – желоб для выпуска чугуна; 6 – фурмы; 7 – желоб для выпуска шлака; 8 – топливо; 9 – руда; 10 – флюс; 11 – капли чугуна; 12 – капли шлака
Руду, флюс и топливо загружают сверху чередующимися слоями. Снизу через фурмы подается нагретый до 600–900 °С воздух.
Топливо горит в верхней части горна. Образующийся оксид углерода восстанавливает железо по схеме:
3Fe2O3 + СО ® 2Fe3O4 + СО2;
Fe3O4 + СО ® 3FeO + СО2;
FeO + СО ® Fe + СО2.
После восстановления железа образуется карбид железа (цементит)
3Fe + 2СО ® Fe3C + СО2.
При температуре выше 900 °С происходит науглероживание железа, выше 1147 °С образуется жидкий чугун и плавится пустая порода с флюсом, а затем и с золой кокса, и образуется шлак. Они собираются в нижней части горна, чугун – внизу, шлак, как более легкий, - над чугуном. Периодически чугун и шлак выпускаются через летки. На 1 т чугуна получается 0,6 т шлака. Он используется при изготовлении портландцементов, шлако-щелочных вяжущих, щебня и пр.
Чугуны подразделяются на литейные, применяемые для труб, санитар-ных деталей; передельные, используемые для производства стали; специальные – сплавы железа с марганцем (ферромарганец), с кремнием (ферросилиций) и другими, которые служат раскислителями или легирующими добавками при получении стали.
Получение стали
Сталь отличается от чугуна меньшим содержанием углерода (до 2,14 %) и других примесей. Она имеет более высокую пластичность, лучше обрабатывается. Получение стали из чугуна заключается в уменьшении примесей до допускаемого количества. Основными примесями в стали являются сера, фосфор, марганец, кремний.
В обычной стали содержание серы допускается до 0,04–0,06 %. Это вредная примесь. При повышенном ее содержании сталь становится красноломкой.
Содержание фосфора в стали составляет 0,04–0,085 %. Это также вредная примесь, которая увеличивает хрупкость стали, особенно при низких температурах.
Содержание марганца в стали обычно составляет 0,3–0,8 %. Он вводится как раскислитель, повышает прокаливаемость стали и ослабляет вредное действие серы.
Содержание кремния в обычной стали не превышает 0,3–0,4 %. Он явля- ется раскислителем, повышает плотность слитка.
Основными способами производства стали являются конверторный мартеновский и электроплавка.
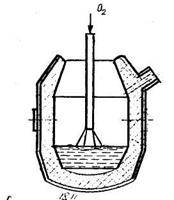 Конверторныйспособ получения стали заключается в продувке воздухе или кислорода через расплавленный чугун. Процесс осуществляется в специальных печах – конверторах. Различают кислый (бессемеровский), основной (томасовский) и кислородно-конверторный способы. Первые два имеют ограниченное применение из-за низкого качества стали. Основным способом является кислородно-конверторный, при котором окисление чугуна осуществляется технически чистым кислородом. Схема кислородного конвертора приведена на рисунке 18.11.
Конверторныйспособ получения стали заключается в продувке воздухе или кислорода через расплавленный чугун. Процесс осуществляется в специальных печах – конверторах. Различают кислый (бессемеровский), основной (томасовский) и кислородно-конверторный способы. Первые два имеют ограниченное применение из-за низкого качества стали. Основным способом является кислородно-конверторный, при котором окисление чугуна осуществляется технически чистым кислородом. Схема кислородного конвертора приведена на рисунке 18.11.
Материалами для получения стали служат расплавленный чугун, лом, окислители.
 Перед загрузкой конвертор нак-лоняют, загружают лом, затем заливают чугун. Далее конвертор ставят в вер-тикальное положение, опускают фурму и начинают продувать кислород. Одно-временно загружают известь, железную руду и флюсы (боксит, плавиковый шпат).
Перед загрузкой конвертор нак-лоняют, загружают лом, затем заливают чугун. Далее конвертор ставят в вер-тикальное положение, опускают фурму и начинают продувать кислород. Одно-временно загружают известь, железную руду и флюсы (боксит, плавиковый шпат).
В начале процесса кислород окисляет железо, образуя оксид железа, который начинает реагировать с кремнием, марганцем, фосфором и углеродом:
2Fe + О2 = 2FeО + Q;
2FeO + Si = 2Fe + SiO2 + Qi;
FeO + Mn = Fe + MnO + Q2;
5FeO + 2P = 5Fe + P2O5 + Q3;
FeO + С = Fe + CO - Q.
После окисления углерода снова начинает окисляться железо. В металле содержится незначительное количество углерода и много оксида железа. Такой металл красноломкий, непригоден по механическим свойствам. Поэтому после прекращения дутья в конвертор вводят раскислители: марганец, кремний в виде ферросплавов и алюминий в чистом виде.
SiO2 и МпО уходят в шлак, а СО частично сгорает и удаляется с пламенем.
После окончания продувки конвертор поворачивают в горизонтальное положение, и сталь выпускают в ковш.
По степени раскисленности стали разделяют на кипящие, полуспокойные и спокойные. Кипящие стали раскисляют ферромарганцем. В них частично остается растворенный FeO и при кристаллизации продолжается процесс кипения по реакции
FeO + С = Fe + СО.
Сталь содержит в своем составе пузыри. Ее стоимость самая низкая.
Спокойную сталь раскисляют ферромарганцем, ферросилицием и алюминием. В металле нет FeO. Кипение прекращается, сталь «ускоряется». Это наиболее дорогая сталь.
Полуспокойную сталь раскисляют ферромарганцем и в меньшем количестве ферросилицием. Она занимает среднее положение между кипящей и спокойной.
После раскисления сталь разливают в изложницы для получения стальных слитков.
Мартеновский способ выплавки стали осуществляется на поду мартеновской печи (рисунок 18.12).
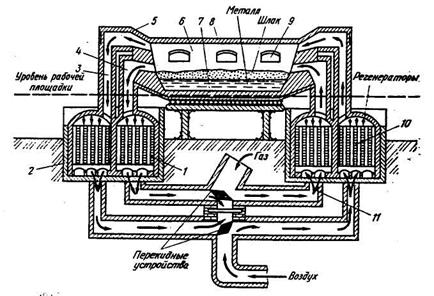
Рисунок 18.12 – Схема мартеновской печи: 1 – газовые регенераторы; 2 – воздушные регенераторы; 3, 4 – воздушные и газовые вертикальные каналы; 5 – головки; 6 – рабочее пространство печи; 7 – подина печи; 8 – свод; 9 – рабочие окна; 10 – насадка регенератора; 11 – борова
Мартеновская печь является пламенной печью, в рабочем пространстве которой сжигается газообразное или жидкое топливо. Высокая температура создается за счет регенерации тепла отходящих газов. Сырьем служат стальной лом, флюсы и чугун, которые последовательно загружают в печь. Образующийся FeO вступает во взаимодействие с вредными примесями и переводит их в шлак. Шлак всплывает и находится на поверхности стали. Окисляясь, FeO переходит в железо.
Мартеновским способом получают высококачественные стали необходимого состава. Их применяют для изготовления мостов, ферм, рельсов.
Электроплавкаосуществляется в дуговых и индукционных печах. Наиболее распространены электродуговые печи вместимостью от 0,5 до 360 т (рисунок 18.13). Тепло образуется электрической дугой, возбуждаемой графитовыми электродами и металлической шихтой.
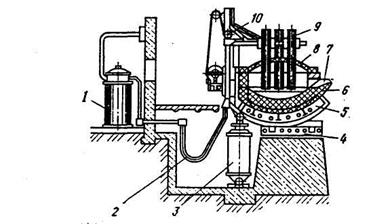
Рисунок 18.13 – Схема дуговой электропечи: 1 – понижающий трансформатор; 2 – токоподводящие кабели; 3 – гидравлический привод для наклона печи;
4, 5 – опора сектора и сектор для наклона печи; 6 – подина печи;
7 – желоб для выпуска металла; 8 – свод печи; 9 – электроды;
10 – механизм для подъема и опускания электродов
В электропечах получают стали заданного химического состава. Это высококачественные конструкционные, инструментальные, коррозионностойкие, жаростойкие и другие специальные стали. Однако стоимость их выше конверторной и мартеновской. Выплавленную сталь выпускают в ковш, представляющий металлический сосуд (рисунок 18.14), выложенный изнутри огнеупорным материалом, из которого затем разливают в металлические формы (изложницы), где она затвердевает и образует слитки массой от 10 кг до 300 т. Крупные слитки разливают сверху (рисунок 18.15), мелкие –сифоном снизу (рисунок 18.16).
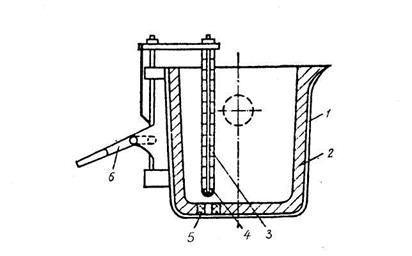
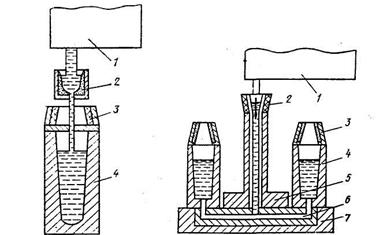 Рисунок 18.14 – Сталеразливочный ковш: 1 – кожух; 2 – футеровка ковша; 3 – стопор; 4 –огнеупорная пробка; 5 – стакан с отверстием для выпуска стали; 6 – рычажный механизм стопора
Рисунок 18.14 – Сталеразливочный ковш: 1 – кожух; 2 – футеровка ковша; 3 – стопор; 4 –огнеупорная пробка; 5 – стакан с отверстием для выпуска стали; 6 – рычажный механизм стопора
|
|
При затвердевании объем стали уменьшается на 3 %. Образуются раковины и усадочная пористость. В спокойной стали все пустоты из слитка должны быть выведены в его прибыльную часть, составляющую 12–20 %, которая затем отрезается и идет в переплав.
Наиболее прогрессивным является непрерывный способ разливки стали (рисунок 18.17). Сталь поступает в кристаллизатор, где затвердевает в виде одного непрерывного слитка необходимого профиля и неограниченной длины. Затем его разрезают на мерные длины и используют при производстве листа и сортового проката.
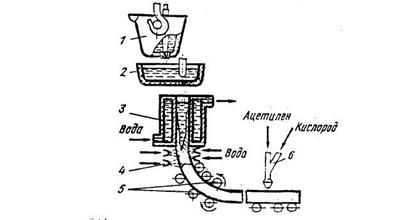
Рисунок 18.17 – Схема непрерывной разливки стали: 1 – сталеразливочный
ковш; 2 – промежуточный ковш; 3 – водоохлаждаемый кристаллизатор; 4 – зона
вторичного охлаждения; 5 - тянущие валки; 6 — ацетилено-кислородный резак
Непрерывное литье сокращает отходы, повышает производительность труда, улучшает качество металла.
18.4.3 Получение меди
Сырьем для выплавки меди служат сульфидные руды – медный колчедан или халькопирит Cu2S и другие с содержанием меди 1–2 %. Медь получают чаще всего пирометаллургическим способом, который включает обогащение руд для получения концентрата, его обжига, плавку на медный штейн, получение черновой меди и ее рафинирование. Обогащение осуществляют флотацией, после чего медный концентрат содержит до 30 % меди. Затем его обжигают для частичного удаления серы (до 50 %) и получают огарок. Плавка на штейн производится в пламенных отражательных или
электропечах при температуре до 1600 °С, затем штейн заливают в конвертор (рисунок 18.18) и перерабатывают в черновую медь. Для шлакования оксидов железа на поверхность штейна загружают кварцевый песок. Затем производят продувку воздухом в два периода.
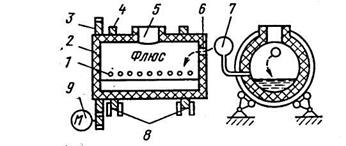
Рисунок 18.18 –Медеплавильный конвертор: 1 – фурмы воздушного дутья;
2 – футеровочный корпус; 3 – зубчатая передача; 4 – обод;
5 – горловина для заливки штейна; 6 – отверстие для загрузки флюса;
7 – воздухопровод; 8–опорные ролики; 9 – электродвигатель с редуктором
В первый период сульфиды железа окисляются кислородом воздуха. FeO, взаимодействуя с SiO2, переходит в шлак, a SO2 направляется на изготовление серной кислоты:
2FeS + ЗО2 = 2FeO + 2SO2 + Q;
2FeO + SiO2 = SiO2 ∙ 2FeO + Q.
Шлак направляют на повторную переработку для извлечения меди. Оставшийся штейн белого цвета продувают вторично воздухом и получают черновую медь:
2Cu2S + ЗО2 = 2Cu2O + 2SO2;
Cu2S + 2Cu2O = 6Cu + SO2.
Она содержит в своем составе до 2 % железа, серы, цинка, никеля, свинца, алюминия и других примесей. Ее рафинируют огневым и электролитическим способами. Огневое рафинирование черновой меди осуществляется в пламенных 400-тонных печах, где ее расплавляют и продувают воздухом. В результате чего образуется 4Сu + О2 = 2Сu2О, который окисляет примеси Al, Si, Mn, Zn, Fe, Ni и др. Не окисляются только золото и серебро. После скачивания шлака медь раскисляют, перемешивая природным газом. Это происходит по реакции
4Сu2О + СН4 = 8Сu + СО2 + 2Н2О.
Расплав с содержанием 99,5–99,7 % меди разливают в слитки или анодные пластины для электролитического рафинирования.
Электролиз осуществляют в ваннах. Электролитом является 15%-ный раствор медного купороса (CuSO4 · 5Н2О) и серной кислоты (H2SO4). В электролит погружают анодные пластины из черновой меди и катоды, изготовленные из чистой электролитической меди. Их подвешивают на анодной и катодной шинах и включают постоянный ток. Металл анодов растворяется и переходит в раствор, а на катодах выделяется металлическая медь чистотой 99,98 %. Ее переплавляют в слитки, из которых получают лист, проволоку, трубы, используют для выплавки латуней и бронз.
Получение алюминия
Алюминий производят из руд, богатых глиноземом. Чаще всего используют бокситы. Состав их следующий, %: AI2O3 – 40–60, Fe2О3 – 15–30, SiO2– 5–15, TiO2 – 2–4 и гидратная вода – 10–15. Процесс получения алюминия включает три этапа: извлечение глинозема из руды, электролиз расплавленного глинозема и получение первичного алюминия, его рафинирование.
Глинозем извлекают мокрым или сухим способами. При мокром – бокситы дробят, измельчают в шаровых мельницах, а затем выдерживают в автоклавах 2–3 часа с концентрированной щелочью при температуре 150–250 °С и давлении до 3 МПа. Происходит взаимодействие между глиноземом и щелочью:
А12О3 + ЗН2О + 2NaOH = Na2O × А12О3 + 4 Н2О.
Раствор алюмината натрия в виде пульпы, после фильтрации и разбавления водой, выдерживается в отстойнике, в котором выпадает в осадок гидроксид алюминия,
Na2O ∙ А12О3 + 4 Н2О = 2NaOH + 2А1(ОН)3¯,
который фильтруют, прокаливают при температуре 1200-1300 °С во вращающихся печах и получают глинозем:
2А1(ОН)3 = А12О3 + 3Н2О.
При сухом способе смесь боксита, соды и известняка спекают во вращающихся печах при температуре 1200 °С. Образуется спек с водорастворимым алюминатом натрия
А12О3 + Na2 CO3 = Na2O · А12О3 + СО2
и нерастворимый в воде силикат кальция CaO · SiO2, в образовании которого участвует известь.
Алюминат натрия извлекают из спека горячей водой и продувают газообразным СО2:
Na2O ∙ А12О3 + 3Н2О + СО2 = 2А1(ОН)3 + Na2 CO3.
Осадок промывают, прокаливают и затем получают глинозем, как при мокром способе.
Глинозем растворяют в расплавленном криолите Na3AlF6, из которого электролизом получают алюминий. Процесс осуществляется в алюминиевой ванне-электролизере (рисунок18.19). Внутренняя поверхность ванны облицована угольными блоками, которые являются катодом. Анодами служат угольные электроды, погруженные в расплав.
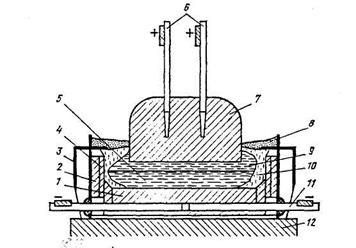
Рисунок 18.19 – Схема электролизера для производства алюминия:
1 – катодные угольные блоки; 2 – огнеупорная футеровка; 3 – стальной кожух;
4 – угольные плиты; 5 – жидкий алюминий; 6 – металлические стержни с шинами;
7 – угольный анод; 8 – глинозем; 9 – жидкий электролит; 10 – корка затвердевшего
электролита; 11 – катодная токоподводящая шина; 12 – фундамент
При температуре 930–950 °С глинозем электролита диссоциирует на ионы:
А12О3 ® 2 А13+ + 3О2-
На поверхности угольной подины, которая служит катодом, ионы восстанавливаются до металла:
2А13+ + 6е = 2А1.
По мере накопления жидкий алюминий периодически удаляется.
Очистка алюминия от примесей А12Оз, Fe, Si, С, Н2 и др. осуществляется чаще всего электролитическим рафинированием, где электролитом являются безводные хлористые и фтористые соли. Получают алюминий чистотой 99,996 %.
Получение магния
Магний получают из магнезита MgCО3, доломита MgCО3 · СаСО3, карналлита MgCl2 ∙ КС1 · 6Н2О двумя способами – электролитическим и термическим. Наиболее распространенным является электролитический. Исходным сырьем в этом случае служит обезвоженный хлорид магния или обезвоженный карналлит. Хлорид магния получают обжигом магнезита и хлорированием оксида магния:
MgCO3 = MgO + СО2;
MgO + Cl2 + С = MgCl2 + CO.
Электролиз расплавленного хлорида магния MgCl2 осуществляют в электролизерах. Аноды изготавливают из графита, катоды – из стали. После электролиза для удаления примесей его подвергают рафинированию.
Магний применяют для раскисления и обессеривания некоторых металлов и сплавов, для производства сверхлегких сплавов.
18.5 ПРОИЗВОДСТВО МЕТАЛЛИЧЕСКИХ ИЗДЕЛИЙ
Металлические изделия изготавливают методами литья, давлением, с применением сварки и пайки. Для улучшения свойств металл подвергают термической обработке.
Получение изделий литьем
Литьем называется способ получения заготовки или изделий (отливок) заполнением форм заданной конфигурации жидким металлом. Отливки изготавливают литьем в обычные песчаные формы и специальными способами.
Литейные формы изготавливают из формовочных и стержневых смесей, состоящих из кварцевого песка, являющегося огнеупорной основой, и связующих: глины, жидкого стекла, полимеров. В литейные формы из вагра-нок, электропечей или раздаточных ковшей заливают расплав.
Специальными способами литья получают изделия высокой точности с лучшим качеством поверхности. Это литье в кокиль, когда литейная форма изготавливается из металла (чугун, алюминиевые и другие сплавы), литье под давлением, литье в керамические формы.
Для строительства отливают из чугуна тюбинги. трубы, опорные части колонн, архитектурно-художественные детали.
