Процесс взаимодействия ионов соли с водой, приводящий к образованию слабого электролита, называется гидролизом
Гидролиз представляет собой обменное взаимодействие ионов соли с молекулами воды, в результате которого смещается равновесие электролитической диссоциации воды. Сущность этого процесса заключается в том, что катион соли (слабое основание) или ее анион (слабая кислота) связывает соответственно ОН- или Н+ с образованием слабого электролита (основания или кислоты).
Если соли рассматривать как продукт взаимодействия кислоты с основанием, то в зависимости от этого их можно разделить на четыре типа: соли, образованные сильным основанием и сильной кислотой; соли, образованные сильным основанием и слабой кислотой; соли, образованные слабым основанием и сильной кислотой; соли, образованные слабым основанием и слабой кислотой.
Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются, так как при их взаимодействии с водой не могут быть получены слабые электролиты. Вследствие этого равновесие Н+- и ОН--ионов в воде не нарушается, поэтому в растворах таких солей среда остается нейтральной (рН=7).
Гидролиз соли, образованной сильным основанием и слабой кислотой, иначе называется гидролизом по аниону. Рассмотрим в качестве примера гидролиз Na2CO3. При растворении этой соли в воде CO32- -ионы связываются с водородными ионами воды, образуя недиссоциирующие НСО3--ионы:
2Na+ +CO32- + HOH↔Na++НCO3- + ОН- (I ступень)
СО32- + НОН ↔ HCO3- + OН-
Na++HCO3- +H2O↔H2CO3+Na++OH- (II ступень)
HCO3- + НОН ↔ Н2СО3+ОН-
В молекулярной форме уравнение гидролиза выглядит так:
Na2CO3+HOH↔NaHCO3+NaOH
Таким образом, каждый ион водорода нейтрализует одну единицу отрицательного заряда иона кислотного остатка СО32-, а из молекулы воды освобождается ОН--ион. Этот ион, будучи в избытке, придает щелочную реакцию, так как первая ступень гидролиза соли сильно выражена (рН > 7). Следовательно, растворы солей, образованных сильным основанием и слабой кислотой, имеют щелочную реакцию.
Гидролиз соли, образованной слабым основанием и сильной кислотой, иначе называют гидролизом по катиону. Рассмотрим гидролиз СuС12. Течение гидролиза обусловлено образованием очень слабо диссоциирующих ионов ОH-:
Сu2++2С1-+Н2О↔Сu(ОН)++С1- + Н++С1- (I ступень)
Сu2+ + Н2О = Сu(ОН)+ + Н+
Сu(0Н)++С1-+Н2О↔Сu(ОН)2 + H++ С1- (II ступень)
Сu(ОН)+ + Н2О ↔ Cu(OH)2 + H+ В молекулярной форме уравнение гидролиза выглядит так:
CuCl2+HOH↔Cu(OH)Cl+HCl
ионное уравнение:
Сu2+ + НОН ↔ Сu(ОН)+ + Н+
В этой реакции гидролиза первая ступень более выражена, вследствие чего в растворе наблюдается избыток ионов водорода. Следовательно, растворы солей, образованных слабым основанием и сильной кислотой, имеют кислую реакцию (рН < 7).
Гидролиз соли, образованной слабым основанием и слабой кислотой , называют гидролизом по катиону и аниону. В полностью ионизированной соли слабого основания и слабой кислоты, например в карбонате алюминия Аl2(CO3)3, катион ведет себя как кислота, а анион — как основание. Следовательно,
2А13+ + ЗСО32- + 6Н0Н ↔ 2А1(ОН)з + ЗСО2 + 3Н2О
При кипячении раствора гидролиз усиливается, и реакция практически идет до конца; рН среды определяется относительной силой оснований и кислот и может быть либо нейтральной, либо незначительно смещенной в ту или иную сторону, т. е. слабокислой или слабощелочной.
Количественно гидролиз характеризуется степенью гидролиза αГ и константой гидролиза Кг.
Доля вещества, подвергающаяся гидролизу, называется степенью гидролиза:
αг = Сг/С, где Сг — концентрация гидролизованной части вещества; С — общая концентрация растворенного вещества.
В растворах умеренной концентрации αг при комнатной температуре невелика. Для солей, образованных сильным основанием и сильной кислотой, она практически равна нулю. Если соль образована слабым основанием и сильной кислотой или сильным основанием и слабой кислотой, то αг составляет около 1 %.
Если представить в общем виде уравнение гидролиза
МеА + Н2О ↔НА + МеОН, то для этого равновесия константа равна:
К= [НА] [MeOH]/[MeA][H2O].
Учитывая, что в разбавленных растворах концентрация_воды является практически постоянной величиной, то, обозначив К [Н2О] = Кг, получим выражение для константы гидролиза соли:
Кг= [НА] [MeOH]/[MeA].
Чем больше значение Кг , тем в большей степени протекает гидролиз. Константа гидролиза связана с константами диссоциации кислоты и основания следующим образом: Кг= Кw/Kk, Кг= Кw/Kосн
Следовательно, значения Кг тем больше, чем меньше константа ионизации кислоты или основания соответственно, поэтому, чем слабее кислота, тем в большей степени подвергаются гидролизу ее соли; чем слабее основание, тем в большей степени подвергаются гидролизу образованные им соли.
На процесс гидролиза значительное влияние оказывают концентрация и температура. В соответствии с принципом Ле Шателье рассмотрим влияние этих факторов на положение гидролитического расщепления. Разбавление раствора равноценно увеличению концентрации одного из реагирующих веществ (в данном случае воды). Следовательно, равновесие смещается вправо, т. е. гидролиз усиливается. Наоборот, гидролиз концентрированных растворов протекает значительно слабее.
Изменение температуры влияет на гидролиз вследствие резкой температурной зависимости степени диссоциации воды. С повышением температуры концентрация Н+ и ОН~-ионов в растворе резко возрастает, вследствие чего увеличивается вероятность связывания их с образованием малодиссоциированной кислоты или основания. Поэтому с повышением температуры гидролиз протекает полнее. Данный вывод подтверждается тем, что реакция нейтрализации экзотермична. Так как гидролиз является противоположным ей процессом, т. е. эндотермичен, то в соответствии с принципом Ле Шателье нагревание вызывает, усиление гидролиза.
Сильные электролиты.
В водных растворах сильные электролиты обычно полностью диссоциированы. Поэтому число ионов в них больше, чем в растворах слабых электролитов той же концентрации. И если в растворах слабых электролитов концентрация ионов мала, расстояния между ними велики и взаимодействие ионов друг с другом незначительно, то в не очень разбавленных растворах сильных электролитов среднее расстояние между ионами вследствие значительной концентрации сравнительно мало. Например, в насыщенном растворе хлорида натрия среднее расстояние между ионами всего только в 2 раза больше, чем в кристаллах NaCl. При этом силы межионного притяжения и отталкивания довольно велики. В таких растворах ионы не вполне свободны, движение их стеснено взаимным притяжением друг к другу. Благодаря этому притяжению каждый ион как бы окружен шарообразным роем противоположно заряженных ионов, получившим название «ионной атмосферы».
В отсутствие внешнего электрического поля ионная атмосфера симметрична и силы, действующие на центральный ион, взаимно уравновешиваются. Если же приложить к раствору постоянное электрическое поле, то разноименно заряженные ионы будут перемещаться в противоположных направлениях. При этом каждый ион стремится двигаться в одну сторону, а окружающая его ионная атмосфера — в противоположную, вследствие чего направленное перемещение иона замедляется, а следовательно, уменьшается число ионов, проходящих через раствор в единицу времени, т. е. сила тока. Чем больше концентрация раствора, тем сильнее проявляется тормозящее действие ионной атмосферы на электрическую проводимость раствора. Значения степени диссоциации хлорида калия, вычисленные при 18 °С по электрической проводимости его растворов, показывают, что с ростом концентрации ее падает:
Концентрация КС1, См 0,01 0,1 1 2
а, % 94,2 86,2 75,6 71,2
Однако падение степени диссоциации объясняется не образованием молекул, а увеличением тормозящего действия ионной атмосферы. В связи с этим, определяемое по электрической проводимости (или другими методами) значение степени диссоциации сильных электролитов называется кажущейся степенью диссоциации.
Аналвгично силы межионного притяжения и отталкивания влияют и на величину осмотического давления, которая, несмотря на полную диссоциацию, все же меньше, чем следовало бы ожидать при удвоенном, утроенном и большем числе частиц. Следовав телыго, все еввйетва раствора электролита, зависящие от концентрации ионов, проявляются так, как если бы число ионов в растворе
было меньше, чем это соответствует полной диссоциации электро-
лита.
Для оценки состояния ионов в растворе пользуются величиной, называемой активностью.
Под активностью иона понимают ту эффективную, условную концентрацию его, соответственно которой он действует при химических реакциях. Активность иона а равна его концентрации С, умноженной на коэффициент активности/:
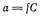
Коэффициенты активности различных ионов различны. Кроме того, они изменяются при изменении условий, в частности при изменении концентрации раствора. В концентрированных растворах коэффициент активности обычно меньше единицы, а с разбавлением раствора он приближается к единице. Значение /, меньшее единицы, указывает на взаимодействие между ионами, приводящее к их взаимному связыванию. Если же коэффициент активности близок к единице, то это свидетельствует о слабом межионном взаимодействии. Действительно, в очень разбавленных растворах средние расстояния ионов друг от друга настолько велики, что действие межионных сил почти не проявляется.

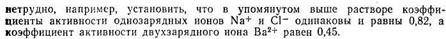
Если пользоваться значениями активности, то законы химического равновесия можно применять и к сильным электролитам. В частности, при этом можно получить значения констант диссоциации сильных кислот. В выражении константы диссоциации вместо концентраций ионов и недиссоциированных молекул будут стоять их активности. Несмотря на некоторую формальность такого рода констант, они полезны, так как дают возможность сравнивать друг с другом свойства сильных кислот.
Лекция 7.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ И ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
Окислительно-восстановительные реакции составляют особый класс химических процессов. Их характерной особенностью является изменение степени окисления, по крайней мере, пары атомов: окисление одного (потеря электронов) и восстановление другого (присоединение электронов). Окисление и восстановление, следовательно, такие два полупроцесса, самостоятельное существование каждого из которых невозможно, однако их одновременное протекание обеспечивает реализацию единого окислительно-восстановительного процесса. Хотя главную роль в последнем играют атомы, изменяющие свои степени окисления, окислителями и восстановителями при рассмотрении соответствующих реакций принято называть не отдельные атомы, а вещества, содержащие эти атомы.
Вещества, содержащие атомы, которые понижают свою степень окисления, называют окислителями, а вещества, содержащие атомы, которые повышают степень окисления, - восстановителями.
Рассмотрим основные типы окислительно-восстановительных реакций.
1. Межмолекулярные (межатомные) окислительно-восстановительные реакции характеризуются тем, что атомы, изменяющие свои степени окисления, находятся в разных по своей химической природе атомных или молекулярных частицах. Другими словами, одни вещества (простые или сложные), вступающие в химические реакции, являются окислителями, а другие - восстановителями. Межмолекулярные процессы составляют наиболее обширную группу окислительно-восстановительных реакций. Примерами могут служить реакции с участием простых и сложных веществ, а также различных атомных и молекулярных частиц (радикалов, ионов и т.п.):
0 0 + 4-2
S + О2 = SО 2
2NaBr + Cl2 = 2NaCl + Br2
2CrO3 + 3МnО = Cr2O3 + 3MnO2
Fe(NO3)2 + AgNO3 = Ag + Fe(NO3)3
2. Внутримолекулярные окислительно-восстановительные реакции характеризуются тем, что атомы, изменяющие свои степени окисления, находятся в одной и той же молекулярной частице:
-3 +6 О +3
(NH4)2Cr2O7 = N2 + Cr2O3 + 4Н2О
В этом случае атомы хрома, изменяющие степень окисления от + 6 до + 3, принимают электроны, а атомы азота, степень окисления которых меняется от — 3 до 0, их отдают.
Среди внутримолекулярных окислительно-восстановительных реакций выделяют реакции диспропорционирования (самоокисления-самовосстановления). Они сопровождаются одновременным увеличением и уменьшением степени окисления атомов одного и того же элемента, первоначально находящихся в одном определенном состоянии. Например, при термическом разложении бертолетовой соли одни атомы хлора восстанавливаются, изменяя степень окисления от + 5 до — 1, а другие окисляются от + 5 до +7:
+5 +7 -1
4КСlO3 = 3КСlO4 + КС1
Среди внутримолекулярных окислительно-восстановительных реакций выделяют и реакции конпропорционирования - процессы, в результате которых происходит выравнивание степени окисления атомов одного и того же элемента, находящегося в исходном веществе в различных состояниях. Например:
-3 +3 О
NH4NO2 = N2 + 2H2O
В этом случае происходит выравнивание степени окисления атомов азота: в исходном веществе существуют два атома со степенями окисления - 3 и + 3, а в образующейся в результате реакции молекуле N2 атомы азота имеют нулевую степень окисления. В аналогичной реакции конпропорционирования, протекающей при нагревании нитрата аммония, два атома азота со степенями окисления - 3 и +5 образуют в результате реакции молекулу N2O, в которой оба атома азота имеют степень окисления +1.
