Роль глутатиона в процессах детоксикации
Биосинтез глутатиона происходит во всех клетках, а катаболизм преимущественно в клетках почек. Внутриклеточный пул включает его восстановленную и окисленную формы, смешанные дисульфиды, тиоэфиры.
Глутатион поддерживает функциональную активность биологических мембран; участвует в механизмах передачи нервного импульса, синтезе белка и ДНК, в синтезе простагландинов, в модулировании конформационного состояния белковых молекул, за счет этого участвует в регуляции активности ферментов и в механизмах транспорта аминокислот. Однако наиболее существенной функцией глутатиона является участие его в процессах детоксикации ксенобиотиков. Этот трипептид прямо или косвенно участвует в функционировании всех звеньев системы детоксикации.
В первой фазе детоксикации уровень глутатиона имеет существенное значение для действия цитохрома Р-450. Взаимосвязь их реализуется на уровне восстановленных эквивалентов НАДФН, необходимых как для глутатионредуктазы, так и для цитохрома Р-450.
Важную роль во взаимодействии цитохрома Р-450 и глутатиона играют процессы перекисного окисления. Глутатион устраняет избыток перекисных соединений при действии Se-зависимой или Se-независимой Глутатион-пероксидаз. Таким образом, осуществляется защита цитохрома Р-450 от пов-реждающего действия активных форм кислорода и перекисных соединений.
Между глутатионом и цитохромом существуют двойные взаимосвязи: конкурентные – через общий фонд НАДФН, который расходуется редуктазами глутатиона и цитохрома, и пополняется в глюкозо-6-фосфатдегидрогеназной реакции пентозофосфатного цикла, и реципроктные – через продукты восстановления молекулярного кислорода, побочно продуцирующиеся при функционировании цитохрома Р-450.
Помимо прямого взаимодействия глутатиона и цитохрома существует и опосредованное влияние глутатиона на действие микросомальных монооксигеназ. Метаболизм ксенобиотиков при определенных уровнях их воздействия на организм сопровождается активацией микросомальных монооксигеназ за счет индукции. В процессах интенсификации синтеза белка принимает участие глутатион, поддерживая оптимальный уровень внутри-клеточного пула аминокислот, обеспечивая их транспорт через клеточную мембрану, восстанавливая дисульфидные связи в белковых молекулах и участвуя в синтезе предшественников ДНК.
Во второй фазе детоксикации ксенобиотиков глутатион участвует в образовании конъюгатов. Эти реакции катализируется глутатион-S-трансферазами. Глутатион участвует в реакциях дегалогенизации, замещения лабильных нитрогрупп или сульфатов. Он взаимодействует с эпоксидами, веществами с ненасыщенными связями, с органическими фосфатами, тиоцианатами, поли- и гетероциклическими соединениями и т. д. Принципиально важно присутствие глутатион-S-трансферазы в эритроцитах. Это открывает возможности детоксикации экзогенных гидрофильных соединений уже на первых этапах их проникновения в организм. Конъюгаты глутатиона активно транспортируются через мембрану эритроцитов.
Глутатион занимает центральное место и в третьем звене системы детоксикации – в антирадикальной и антиперекисной защите.
Следует отметить участие глутатиона и во внемикросомальной биотрансформации ксенобиотиков (например, метилртути, формальдегида).
Металлотионеины
Это низкомолекулярные белки, содержащие до 30% цистеина и способные связывать ионы тяжелых металлов. Обладают уникальной структурой – молекула содержит 23-33% цистеина без дисульфидных мостиков, остатков ароматических аминокислот и гистидина. Содержат ионы цинка. Образуя меркаптиды, металлотионеины способны связывать до семи ионов тяжелых металлов на одну молекулу. Участвуют в регуляции гомеос-таза цинка и меди. Индуцируются металлами (например, цинком), а также глюкокортикоидами и веществами типа интерферона, интерлейкина и др.
Также участвуют в иннактивации свободных радикалов (цистеин в составе металлотионеинов в 770 раз более активен, чем цистеин глутатиона). Способны связывать ионы железа, являющиеся активаторами свободно-радикального окисления (хелатированные белками ионы железа не активны для реакции Фентона). Активируют ферменты антиоксидантной системы. Также способны замещать глутатион в глутатионпероксидазной системе. За счет этого металлотионеины оказывают радиозащитное действие.
Тестовый контроль по теме: “Адаптация. Биохимические механизмы детоксикации эндогенных и экзогенных соединений”
Тест 1
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Реакции, за счет которых протекает первая фаза детоксикации ксенобиотиков:
а) митохондриального окисления
б) окислительного фосфорилирования
в) микросомального окисления
г) окислительного декарбоксилирования
д) бета-окисления
Тест 2
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Цитохром Р-450 представляет собой белок, содержащий в порфириновом кольце ионы:
а) меди
б) хрома
в) цинка
г) железа
д) селена
Тест 3
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Глутатион является:
а) биогенным амином
б) стероидным гормоном
в) водорастворимым антиоксидантом
г) жирорастворимым витамином
д) жирорастворимым антиоксидантом
Тест 4
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Реакции, за счет которых протекает вторая фаза детоксикации ксенобиотиков:
а) перекисного окисления
б) декарбоксилирования
в) конъюгации
г) деакилирования
д) дезаминирования
Тест 5
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Источником НАДФН для антиоксидантной системы является:
а) гликолиз
б) бета-окисление
в) глюконеогенез
г) пентозофосфатный цикл
д) цикл трикарбоновых кислот
Тест 6
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Приспособительным механизмом в условиях разнообразных химических воздействий является:
а) разобщение окисления и фосфорилирования
б) индукция множественных форм ферментов детоксикации
в) увеличение перекисного окисления липидов
г) ингибирование анаэробного окисления глюкозы
д) усиление процессов фильтрации в почках
Тест 7
ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ
Локализация ферментов монооксигеназной системы печени:
а) митохондриях
б) ядре
в) рибосомах
г) ЭПР
д) пероксисомах
Тест 8
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Виды реакций конъюгации:
а) декарбоксилирование
б) метилирование
в) ацетилирование
г) дезаминирование
д) фосфорилирование
Тест 9
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Цитохромы микросомального окисления:
| а) в б) с г) аа3 в) Р-450 д) в5 |
Тест 10
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Биотрансформация ксенобиотиков интенсивно протекает в:
а) коже
б) головном мозге
в) сердечной мышце
г) печени
д) легкие
Тест 11
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Реакции, катализируемые монооксигеназной системой:
а) гидроксилирования
б) деалкилирования
в) фосфорилирования
г) декабоксилирования
д) эпоксидирования
Тест 12
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Эндогенные вещества, метаболизируемые микросомальными оксигеназами:
а) стероидные гормоны
б) глутамин г) холестерин
в) жирные кислоты д) глюкагон
Тест 13
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Ферментами монооксигеназной системы являются:
а) цитохром Р-450
б) глутатионредуктаза
в) НАДФН-зависимая-цитохром-Р450-редуктаза
г) цитохром с
д) цитохром в5
Тест 14
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Индукторами цитохрома Р-450 являются:
а) инсулин
б) метилхолантрен
в) прегненалон
г) витамин РР
д) фенобарбитал
Тест 15
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Микросомальные оксигеназы участвуют в:
а) превращении индола в индоксил
б) синтезе желчных кислот из холестерина
в) образовании АТФ
г) активации витамина Д
д) обмене метионина
Тест 16
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Цитохром Р-450 в обмене женских половых гормонов катализирует превращение эстрадиола в:
а) 4-гидроксиэстрадиол
б) 2-гидроксиэстрадиол
в) 6-гидроксиэстрадиол
г) 16-гидроксиэстрадиол
д) 8-гидроксиэстрадиол
Тест 17
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Ферментами второй фазы детоксикации являются:
а) глутатионредуктаза
б) глутатионтрансфераза
в) аминотрансфераза
г) метилтрансфераза
д) глутатионпероксидаза
Тест 18
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Феномен «токсификации» наблюдается при метаболизме:
а) нифедипина
б) никотина
в) парацетамола
г) варфарина
д) четыреххлористого углерода
Тест 19
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Металлотионеины – это белки, которые:
а) содержат SH-группы
б) имеют в своем составе железо
в) связывают тяжелые металлы
г) индуцируются цинком
д) ингибируются цинком
Тест 20
ВЫБЕРИТЕ ВСЕ ПРАВИЛЬНЫЕ ОТВЕТЫ
Аминокислоты, используемые для детоксикации ксенобиотиков:
а) аланин
б) глицин
в) метионин
г) тирозин
д) фенилаланин
Тест 21
УСТАНОВИТЕ СТРОГОЕ СООТВЕТСТВИЕ
| Реакции конъюгации: | Кофермент: |
| 1) глюкуронидная 2) сульфатная 3) метилирования 4) ацетилирования | а) глутатион б) S-аденозил-метионин в) УДФ-глюкуроновая кислота г) ФАФС д) ацетил-коА |
Тест 22
УСТАНОВИТЕ СООТВЕТСТВИЕ
«каждому вопросу соответствует несколько ответов, каждый ответ может быть использован один раз или не использован совсем»
| Фазы детоксикации: | Компоненты: |
| 1) первая 2) вторая | а) цитохром Р-450 б) глутатионтрансфераза в) цитохром аа3 г) глутатионредуктаза д) глюкуронилтрансфераза |
Тест 23
УСТАНОВИТЕ СООТВЕТСТВИЕ
«каждому вопросу может соответствовать несколько ответов, каждый ответ может быть использован один или несколько раз, не использован совсем»
| Цитохром: | Особенности: |
| 1) Р-450 2) в5 | а) взаимодействует с кислородом б) принимает электроны от НАДФН в) принимает электроны от НАДН г) является гемсодержащим белком д) участвует в окислительном фосфорилировании |
Тест 24
УСТАНОВИТЕ СООТВЕТСТВИЕ
«каждому вопросу может соответствовать несколько ответов, каждый ответ может быть использован один раз или не использован совсем»
| Влияние на цитохром Р-450: | Вещество: |
| 1) индуктор 2) ингибитор | а) флавоноиды грейпфрута б) этанол в) четыреххлористый углерод г) дексаметазон д) адреналин |
Тест 25
ДОПОЛНИТЕ
Коферментом в реакциях сульфатной конъюгации является____________.
Тест 26
ДОПОЛНИТЕ
Коферментом в реакции метилирования является __________________.
Тест 27
ДОПОЛНИТЕ
Коферментом в реакции глюкуронидной конъюгации является______________.
Тест 28
ДОПОЛНИТЕ
Ферменты, катализирующие реакции конъюгации относятся к классу ______________.
Тест 29
ДОПОЛНИТЕ
Увеличение токсичности ксенобиотика при метаболизме на цитохроме Р-450 называется ___________ ______________.
Тест 30
УСТАНОВИТЕ ПРАВИЛЬНУЮ ПОСЛЕДОВАТЕЛЬНОСТЬ
Последовательность стадий в механизме действия цитохрома Р-450:
а) образование тройного комплекса RH-Р-450(Fe+2)-О2
б) восстановление комплекса RH-Р-450(Fe+3) за счет НАДФН
в) распад комплекса с высвобождением воды и гидроксилированного субстрата
г) взаимодействие субстрата (RH) с окисленной формой цитохрома Р-450
д) восстановление комплекса RH-Р-450(Fe+2)-О2 за счет НАДН и цитохрома в5
Ответы по теме: “ Адаптация. Биохимические механизмы детоксикации эндогенных и экзогенных соединений”
| Тест 1 — в Тест 2 — г Тест 3 — в Тест 4 — в Тест 5 — г Тест 6 — б Тест 7 — г Тест 8 — б, в Тест 9 — в, д Тест 10 — а, г, д Тест 11 — а, б, д Тест 12 — а, в, г Тест 13 — а, в, д Тест 14 — б, в, д Тест 15 — а, б, г | Тест 16 — а, б, г Тест 17 — б, г Тест 18 — б, в, д Тест 19 — а, в, г Тест 20 – б, в Тест 21 — 1 в, 2 г, 3 б, 4 д Тест 22 — 1 а, 2 б, д Тест 23 — 1 а, б, г, 2 б, в, г Тест 24 — 1 б, г, 2 а, в Тест 25 – фосфоаденозилфосфосульфат (ФАФС) Тест 26 — S-аденозилметионин Тест 27 — УДФ-глюкуроновая кислота Тест 28 — трансферазы Тест 29 — феномен токсификации Тест 30 — г б а д в (последов-ть) |
1. Тема 30. ²Физико-химические свойства, нормальные и патологические компоненты мочи, качественный и количественный анализ патологических компонентов мочи².
Место проведения - кафедра биохимии.
Продолжительность занятия– 180 минут.
2. Цель занятия:
Учебная: систематизировать знания о происхождении всех выделяемых с мочой компонентов, их роли и значении в оценке функционального состояния различных органов и использовании в клинической практике.
Развивающая цель: развитие логического мышления, умения видеть
причинно-следственные связи, формирование восприятия организма человека как единое целое.
Воспитательная цель:развитие деловых качеств, воспитание
ответственности.
3. Конкретные задачи:
3.1. Студент должен знать:
3.1.1. Роль почек в поддержании гомеостаза и строение нефрона.
3.1.2. Общие механизмы образования мочи.
3.1.3. Происхождение азотсодержащих и некоторых других компонентов мочи в норме (мочевина, мочевая кислота, аминокислоты, креатинин, гип-пуровая кислота, животный индикан, соли аммония, органические кислоты) и патологии (глюкоза, кетоновые тела, белок, гемоглобин, желчные пигменты).
3.1.4. Ферменты, находящиеся в моче, и их диагностическую роль.
3.1.5. Общие свойства мочи.
3.1.6. Физико-химические показатели мочи в норме и патологии.
3.1.7. Значение исследования мочи в клинической практике.
3.1.8. Методы обнаружения некоторых компонентов мочи.
3.2. Студент должен уметь:
3.2.1. Анализировать и объяснять причины отклонения от нормы и появле-ние патологических компонентов в моче при различных ситуациях: воспали-тельный процесс, травма, недостаток продуцирования гормонов, белковое голодание, избыток белка в пище, патология печени, патология почек, сахарный диабет, наследственные заболевания и т.д.).
3.2.2. Обнаружить в моче патологические компоненты: белок, кетоновые тела и глюкозу с помощью качественных реакций.
3.2.3. Определить количественное содержание в моче белка и глюкозы современными методами анализа.
3.2.4.Решить самостоятельную работу на исследование патологических компонентов в предложенной пробе мочи (качественный и количественный анализ).
4. Мотивация: знания, полученные на занятии, могут быть использованы в практической работе врача для выявления патологии различных органов и для контроля состояния здоровья людей.
Межпредметные связи.


 Физиология Анатомия
Физиология Анатомия
 |  |




 Органическая Моча Гистология
Органическая Моча Гистология
химия
 |  | ||||
 | |||||


 Клиническая
Клиническая
Патофизиология Терапия практика
Внутрипредметные связи.



Белковый Липидный Углеводный
 обмен обмен обмен
обмен обмен обмен
 |  | ||


Биохимия Биохимия мышечной

 почек ткани
почек ткани


 Биохимия Моча
Биохимия Моча
 печени
печени
 | |||
 |


Биохимия Гормональная
крови регуляция


Биохимическая оценка Биохимическая оценка
состояния функции почек состояния функции печени
5. Вопросы для самоподготовки:
5.1. Роль почек в поддержании гомеостаза.
5.2. Роль почек в промежуточном обмене.
5.3. Роль почек в регуляции водно-солевого обмена.
5.4. Экскреторная функция почек.
5.5. Строение нефрона и общие механизмы образования мочи.
5.6. Физико-химические свойства мочи: объем, относительная плотность, реакция мочи (РН), цвет; причины их изменения при патологии.
5.7.Азотсодержащие компоненты мочи: мочевина, мочевая кислота, гиппуровая кислота, креатинин, индикан; их происхождение; причины повышения и понижения их содержания в моче.
5.8. Протеинурия, виды и причины возникновения.
5.9. Глюкозурия. Механизмы ее развития и виды.
5.10. Кетонурия. Механизмы развития.
5.11. Гемоглобинурия и гематурия. Причины их появления.
5.12. Причины появления желчных пигментов в моче.
5.13. Креатинурия, механизмы ее развития и виды.
5.14. Ферменты мочи и значение их определения.
5.15. Значение исследования мочи в клинической практике.
6. Задания для самоподготовки:
6.1. Изучить рекомендуемую литературу, используя вопросы для самоподготовки.
6.2. Написать в рабочей тетради физико-химические показатели мочи и их изменения при патологии.
6.3. Написать в рабочей тетради все нормальные и патологические компоненты мочи, их происхождение, причины повышения и понижения их содержания в моче.
Литература:
Основная литература:
1. Березов Т.Т., Коровкин Б.Ф. «Биологическая химия», М., Медицина, 1998, раздел «Почки и моча», с. – 608-624.
2. Учебно-методическое пособие к практическим занятиям по биологичес-кой химии под редакцией проф. В. А. Дадали, доц. М.Н. Смертиной, СПб, 2007, часть 4, тема «Физико - химические свойства, нормальные и патологические компоненты мочи, качественный и количественный анализ патологических компонентов мочи».
3. Северин Е.С. «Биохимия» М., ГЭОТАР-МЕД, 2003, с. 597-606.
Дополнительная литература:
1. Цыганенко А.Я., Жуков В.И., Мясоедов В.В. и др. «Клиническая биохимия», Учебное пособие, М., «Триада-Х», 2002, с. 49-71.
2. Лифшиц В.М., Сидельникова В.И. «Медицинские лабораторные анализы», Справочник, М., «Триада – Х», 2003, с. 33-44, 141-144.
7. Этапы занятия, контроль их усвоения и распределение учебного
времени.
| Этапы проведения занятия | Форма и методы проведения каждого этапа | Форма контроля и усвоения знаний | Время (мин) |
| 7.1. Вводный этап: Организацион-ный момент, представление цели занятия и мотивации. 7.2. Контроль исходного уровня знаний. 7.3. Основной этап: 7.3.1. Формирование знаний о роли почек и многообразии их функций. Формирование знаний об общих механизмах образования мочи. Формирование знаний об общих свойствах мочи. Формирование знаний о нормальных и патологи-ческих компонентах мочи, их происхождении и причинах появления и изменения. 7.3.5. Формирование умений по определению и оценке некоторых патологических компонентов мочи (глюкоза, кетоновые тела, белок). 7.4. Заключительный этап: 7.4.1. Подведение итогов. Оформление и проверка протоколов. 7.4.2. Домашнее задание. | Излагает преподаватель письменно устный опрос дискуссия лабораторная работа представление результатов исследований, оформление протоколов Формулировка следующей темы. | Проверочная работа проверка решения задачи, проверка протоколов |
Пример билета проверочного контроля: см. Тестовый контроль.
Лабораторная работа № 15
²Физико-химические свойства, нормальные и патологические компоненты мочи, качественный и количественный анализ патологических компонентов мочи².
Химическое исследование мочи имеет большое диагностическое значение т.к. состав мочи отражает состояние обмена веществ в организме и функции ряда органов: печени, почек, поджелудочной железы и т.д. Исследование мочи на наличие тех или иных компонентов дает возможность следить за течением патологических процессов и за эффективностью терапевтических мероприятий. Общие свойства мочи: цвет, прозрачность, относительная плотность, реакция мочи (РН), суточный диурез также являются информативными показателями состояния организма.
Обычно для исследования собирают всю порцию утренней мочи. Для количественного анализа необходимо собирать мочу в течение суток, добавляя в качестве антисептика тимол. Анализ проводят с пересчетом на суточное содержание.
Общие свойства мочи.
Реактивы и оборудование.
1.Штатив для пробирок. 2.Водяная баня. 3.Пробирки. 4. Стеклянные трубоч-ки. 5. Стеклянные воронки. 6. Бумажные фильтры или вата. 7. Раствор сульфата меди II- 1%. 8. Раствор гидроксида натрия-10%. 9. Раствор Люголя (раствор иода в иодистом калии). 10.Раствор азотной кислоты –50%. 11.Набор реагентов для определения белка в моче колориметрическим методом с пирогаллоловым красным. 12.Набор реактивов для определения глюкозы в крови и моче глюкозо-оксидазным методом НОВОГЛЮК-К,М (200). 13. Универсальные индикаторные бумажки, футляр со шкалой РН.
Удельный вес мочи (относительная плотность). Для определения удельного веса используются специальные ареометры, которые называются урометрами.
Ход работы: мочу наливают в цилиндр, в нее погружают урометр и по шкале урометра определяют удельный вес мочи (демонстрация).
Реакция мочи, РН мочи. На предметное стекло помещают кусочек универсальной индикаторной бумажки и стеклянной палочкой наносят каплю мочи. Окраску бумажки сравнивают со шкалой РН.
Качественные реакции на патологические компоненты мочи.
Определение глюкозы.
Реакция Троммера.
Принцип метода: основан на окислении глюкозы гидроксидом меди при нагревании с образованием желтого осадка гидрата закиси меди CuOH или красного осадка закиси меди Cu2O.
 Схема реакции: CuSO4 + 2 NaOH Cu(OH)2 + Na2SO4
Схема реакции: CuSO4 + 2 NaOH Cu(OH)2 + Na2SO4
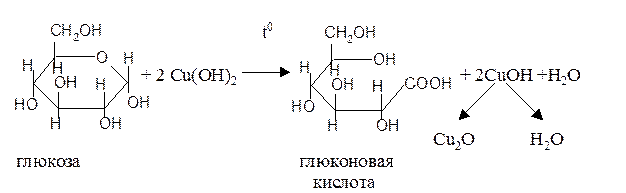 Ход работы: в пробирку вносят 4 капли исследуемой мочи и 4 капли раствора гидроксида натрия, прибавляют 1 каплю раствора сульфата меди и нагревают на кипящей водяной бане. При наличии сахара появляется зеленая, желтая или красная окраска с последующим осадком на дне пробирки. При зеленой окраске без осадка проба отрицательна. При отсутствии глюкозы в моче чаще всего образуется черный осадок окиси меди CuO.
Ход работы: в пробирку вносят 4 капли исследуемой мочи и 4 капли раствора гидроксида натрия, прибавляют 1 каплю раствора сульфата меди и нагревают на кипящей водяной бане. При наличии сахара появляется зеленая, желтая или красная окраска с последующим осадком на дне пробирки. При зеленой окраске без осадка проба отрицательна. При отсутствии глюкозы в моче чаще всего образуется черный осадок окиси меди CuO.
