Упрощенная теория нормального распространения пламени
Скорость нормального распространения пламени теоретически может быть определена из решения уравнения теплопроводности, если известно кинетическое уравнение реакции. Решение для Un впервые было получено в 1938 году Зельдовичем Я.Б. и Франк-Каменецким Д.А., которые разработали тепловую теорию ламинарного распространения пламени. На основе физической модели тепловой теории устанавливаются простые соотношения, связывающие нормальную скорость сгорания с размерами зоны горения и характеристиками пламени.
Поток тепла, отнесенный к единице поверхности в единицу времени, пропорционален градиенту температуры (закон теплопроводности Фурье):
q = - λм 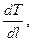
где λм – коэффициент молекулярной теплопроводности, Дж/с·м·град. Знак "-" учитывает то, что тепловой поток имеет направление, обратное направлению повышения температуры.
Рассмотрим элемент фронта пламени. Если принять, что изменение температуры подчиняется линейному закону (пунктир на рис.3.8), то можем написать:

Рис.3.8. Структура ламинарного фронта пламени
Этот тепловой поток воспринимается несгоревшей смесью и идет на повышение её температуры от Т0 до ТГ .
q2 = W·ρ0·cp·(TГ – T0);
Так как q1 = q2 и W = Un, то
Un·ρ0· cp·(TГ – T0) = λм 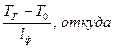 Un = λм/cp· ρ0·
Un = λм/cp· ρ0· 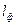 .
.
Здесь ам = λм / cp · ρ0 - коэффициент молекулярной температуропроводности, см2/с
Химическая ширина зоны горения составляет долю от физической
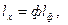 где ф < 1
где ф < 1
Это функция, зависящая от скорости химической реакции, поэтому
Un = ф 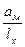 (3.4)
(3.4)
Последнее выражение показывает, что чем меньше толщина зоны горения, тем больше нормальная скорость горения Un.
Фронт пламени, движущийся со скоростью Un, будет проходить расстояние ℓх, за время сгорания τх .
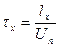 (3.5)
(3.5)
Подставляя значение ℓх= Un· τх в (3.4), получим:

Un2 = ф 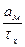 /
/
Считая, что ℓх ≈ ℓф получим окончательно:
Un 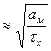 (3.6)
(3.6)
или τх ≈ ам/ Un2;
подставляя последнее выражение в (3.5), получаем:
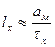 (3.7)
(3.7)
Полученное выражение дает возможность лишь качественно оценивать влияние различных величин на Un.
Нормальную скорость сгорания и ее зависимость от качества и состава смеси, температуры и давления определяют экспериментально. В настоящее время это проще и точнее теоретического расчета.
На рис. 3.9 приведены экспериментальные данные зависимости Un бензо- и керосиновоздушных смесей от коэффициента избытка воздуха при различных начальных температурах. Максимальное значение Un достигается не при стехиометрическом, а при несколько более богатом составе смеси (α ≈ 0,9 - 0,95), и в обе стороны от этого значения величина Un снижается, так как недостаток либо горючего, либо окислителя приводит к снижению температуры сгорания и уменьшению Un. Распространение пламени при умеренной Т0 происходит в диапазоне α от 0,6 до 1,7. Более бедная и более богатая топливная смесь не горит. С увеличением температуры Un возрастает.
Достижение Un мах при α < 1 наблюдается и для других горючих смесей. Объясняется это следующим:
1. В точке, где Un мах достигается максимальная температура сгорания. При некотором обогащении состава смеси топливом от стехиометрического более полно используется кислород воздуха. При стехиометрическом составе смеси появляется большая вероятность того, что не весь кислород воздуха из-за микронеоднородностей смеси будет использован. В результате не сгорит и все топливо, температура окажется несколько меньше, чем теоретическая.
2. При α ≤ 1 несколько возрастает скорость химической реакции, так как на богатой смеси более вероятно образование активных центров ОН и Н ,способствующих возникновении новых цепей, и следовательно, увеличению скорости реакции.
При увеличении начальной температуры топливовоздушной смеси нормальная скорость горения возрастает (рис.3.10), что согласуется с выводами рассмотренной выше тепловой теории - с увеличением начальной температуры возрастает величина коэффициента температуропроводности и уменьшается время химической реакции, так как возрастает ее скорость. Но скорость химической реакции возрастает от температуры по экспоненте, а величина Un по зависимости, близкой к квадратичной.
UnTг = UnT0·(TГ/T0)m, где m = 1,5 – 2,0, Un То - нормальная скорость при Т0 = 288° K.
Зависимость Un от давления различна для разных смесей. Для смеси углеводородного топлива с воздухом
Unp = Un0/pn, где n = 0,2 – 0,3; Un 0 - нормальная скорость при p = 1 кг/см2.
Для топливокислородных смесей по данным некоторых исследователей n = 0, то есть Un не зависит от давления. При разбавлении горючей смеси инертными газами (С02, N2, Не, Аr и др.) нормальная скорость сгорания уменьшается. Это в первую очередь объясняется тем, что при добавлении инертного газа уменьшается концентрация реагирующих веществ и соответственно падает скорость химической реакции. Помимо этого, может изменяться коэффициент температуропроводности.
На рис. 3.11 приведен график, показывающий как будет изменяться нормальная скорость пропано-кислородо-азотной смеси, если между пропаном (С3Н8 ) и кислородом выдерживается стехиометрическое соотношение (α = 1), но будет изменяться мольная доля кислорода ψ. Для воздуха ψ = 0,21. При большой доле кислорода Un растет пропорционально ψ .

Рис.3.9. Зависимость Un от α при различных начальных температурах (бензиновоздушная смесь)

Рис.3.10. Зависимость Un max от t0 для смесей с различными горючими веществами

Рис. 3.11. Зависимость Un от нейтральной примеси (см/с)
