Титриметрическое определение содержания ЛВ
Методы количественного определения ЛВ.
Классификация методов:
1. весовой (гравиметрический) – основан на точном измерении массы определяемого вещества или его составных частей, выделяемых в виде соединения точно известного постоянного состава.
2. объемные (титриметрические) – основаны на измерении объема реагента (титранта) затраченного на реакцию с определяемым веществом.
3. физические и физико-химические:
· оптические методы
а) рефрактометрия – метод анализа, основанный на наличие зависимости показателя преломления света от концентрации раствора исследуемого вещества.
б) поляриметрия – метод анализа, основанный способности вещества вращать плоскость поляризованного света. Эта способность обусловлена наличием ассиметрических атомов углерода.
· Методы основанные на поглощении электромагнитного излучения
а) спектрофотометрия – метод анализа, основанный на измерении оптической плотности раствора вещества в различных областях света (УФ -, ИК - и видимой).
б) фотоколорометрия - метод анализа, основанный на измерении степени поглощения немонохроматического света испытуемым веществом.
· Хроматографические методы
хроматография – процесс разделения смесей веществ, основанный на количественных различиях в поведении разделяемых компонентов при их непрерывном перераспределении между контактирующими фазами, одна из которых неподвижна, а другая имеет постоянное направление движения.
По механизму, лежащему в основе разделения, различают адсорбционную, распределительную, ионнообменную и некоторые другие виды хроматографии.
В настоящее время широко применяют ГЖХ и ВЭЖХ.
а) ГЖХ – основана на распределении компонентов смеси между газовой и жидкой или твердой фазами. Метод применим для анализа летучих веществ или веществ, которые могут быть переведены в газообразное состояние.
б) ВЭЖХ – отличается от ГЖХ тем, что подвижной фазой служит не газ, а жидкость.
· электрометрические методы титрования:
а) определение рН – заключается в сравнении потенциала индикаторного электрода, погруженного в испытуемый раствор, с потенциалом электрода в стандартном буферном растворе с известным значением рН;
б) потенциометрическое титрование – способ определения эквивалентного объема титранта путем измерения в процессе титрования электродвижущей силы специально подобранной электродной парой;
4. биологическая стандартизацияприменяется для препаратов, содержащих сильнодействующие вещества (сердечные гликозиды).
Титриметрическое определение содержания ЛВ
в зависимости от типа реакций, лежащих в основе каждого метода, разделяют на 4 группы:
1. осадительные,
2. кислотно-основные,
3. комплексонометрические
4. окислительно-восстановительные.
Они отличаются друг от друга природой используемых равновесий, индикаторами, стандартными растворами, а также способом определения эквивалентной массы.
Наряду с этой классификацией в практике часто применяют разделение объемных методов в соответствии с типом веществ, используемых в качестве титранта: алкалиметрия, ацидиметрия, аргентометрия, перманганатометрия, йодометрия и т.д. По способу проведения различают методы прямого, обратного и косвенного титрования.
Расчеты при титровании
Титр по определяемому веществу – это масса анализируемого вещества (в г), взаимодействующая с 1 мл титранта. Размерность – г/мл.
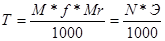 , где
, где
M – молярность титранта;
f – фактор эквивалентности;
Mr – молекулярная масса вещества.
N – нормальность титранта;
Э – эквивалент вещества.
При прямом титровании концентрацию индивидуального лекарственного вещества в процентах рассчитывают по формуле:
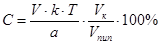 ,
,
где С – концентрация определяемого вещества, %;
V – объем титрованного раствора, мл;
k – коэффициент поправки на титрованный раствор;
T – титр по определяемому веществу, г/мл;
a – навеска, г или мл.
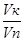 - разведение.
- разведение.
Содержание ингредиентов в граммах рассчитывают по формулам:
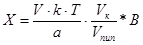 ;
;
где X – масса определяемого лекарственного вещества, г;
V – объем титрованного раствора, мл;
В – объем жидкой лекарственной формы по прописи, мл или общая масса порошка, мази по прописи, г;
a – навеска лекарственной формы, отобранная для анализа, мл или г;
k – поправочный коэффициент титранта.
При обратном титровании используют 2 титрованных раствора. Тогда концентрацию ингредиентов в процентах рассчитывают по формуле:
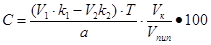 ,
,
где V1 – объем 1-го титранта, взятого в избытке, мл;
k1 – коэффициент поправки на 1-й титрованный раствор;
V2 – объем 2-го титранта, затраченного на титрование избытка 1-го титрованного раствора, мл;
k2 – коэффициент поправки на 2-й титрованный раствор.
Остальные обозначения – см. выше.
Содержание ингредиентов в граммах рассчитывают по формулам:
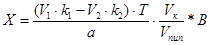 ;
;
где обозначения – см. выше.
В анализе иногда проводят контрольный (холостой) опыт при прямом и обратном способах титрования.
Концентрацию определяемого вещества в процентах и в граммах вычисляют с учетом контрольного опыта по формулам:
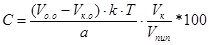 ;
;
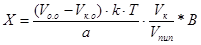 ;
;
где Vо.о – объем титрованного раствора, израсходованный на итрование определяемого вещества, мл;
Vк.о – объем титрованного раствора, израсходованный на титрование контрольного опыта, мл;
Остальные обозначения – см. выше.
При прямом ацидиметрическом титровании некоторых лекарственных веществ (гексаметилентетрамин, калия ацетат, натрия бензоат и др.) контрольный опыт проводится с целью сравнения перехода окраски индикатора в точке эквивалентности в анализируемом и контрольном растворах. В этом случае количество титрованного раствора, израсходованное на титрование в контрольном опыте, при расчетах не учитывается.
В случае обратного титрования концентрацию определяемого вещества в процентах и в граммах вычисляют с учетом контрольного опыта по формулам:
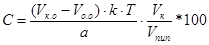 ; ()
; ()
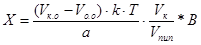 , ()
, ()
где Vк.о – объем 2-го титранта, пошедший на титрование контрольного опыта, мл;
Vо.о – объем 2-го титранта, пошедший на титрование основного опыта, мл;
Остальные обозначения – см. выше.
При заместительном (косвенном) титровании, т.е. титровании вещества, образующегося в результате реакции в количестве, эквивалентном определяемому компоненту, расчет ведут, как при прямом титровании, но титриметрический фактор пересчета определяют не по титруемому заместителю, а по определяемому веществу.
Критерии подхода к разработке методик объемного анализа:
1. навески должны быть для сухих веществ не менее 0,05 г, для жидкостей не менее 1 мл;
2. точность взвешивания навески на аналитических весах 0,0001 г;
3. методика ФС планируется так, чтобы затратить не более 20 мл титранта;
4. расчет навески ведется по формуле:
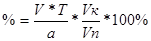 , где
, где
% - процентное содержание ЛВ, %;
V – объем титранта пошедшего на титрование, мл;
T – титр ЛВ, г/мл;
а – навеска ЛВ, г;
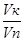 - разведение.
- разведение.
Если мы считаем, что у нас идеальное титрование, то тогда %=100%, разведение = 1 и наша формула приобретает вид:
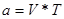 , где а– навеска ЛВ, г;
, где а– навеска ЛВ, г;
V – объем титранта пошедшего на титрование, мл;
T – титр ЛВ, г/мл.
