Дослід 1. Відношення бензолу та скипідару до бромної води
У одну пробірку наливають 1 мл бензолу, у іншу – 1 мл скипідару.
В обидві пробірки доливають по 1 мл бромної води. Струшують.
Спостереження:
Рівняння реакції:
Дослід 2. Взаємодія бензолу з бромом
Дослід виконувати у витяжній шафі у захисних окулярах!
Упробірку поміщають один-два залізних ошурки. Обережно підігрівають. Після охолодження у пробірку спочатку наливають 1мл бензолу, потім додають 1мл розчину брому в CCl4. Суміш обережно підігрівають на водяній бані до початку виділення газу, водночас до отвору пробірки підносять універсальний індикаторний папір, який тримають пінцетом.
Спостереження:
Рівняння реакції:
Дослід 3. Відношення бензолу та скипідару до розчину перманганату калію
У одну пробірку наливають 1 мл бензолу, у іншу–1 мл скипідару.
В обидві пробірки доливають по 2 мл розчину перманганату калію. Струшують.
Спостереження:
Рівняння реакції:
Дослід 4. Відношення бензолу та толуолу до перманганату калію при наявності сульфатної кислоти
У одну пробірку наливають 1 мл бензолу, у іншу – 1 мл толуолу.
У кожну пробірку додають по 1-2 мл 0,1%-го розчину перманганату калію та 1-2 краплі 10%-го розчину сульфатної кислоти. Збовтуючи, обережно підігрівають суміш у пробірках на водяній бані.
Спостереження:
Рівняння реакції:
Дослід 5 Окиснення терпенів киснем повітря
У пробірку поміщають 1 краплю 0,5%-го розчину крохмального клейстеру, 1 краплю 0,5 н розчину КІ і 1 краплю скипідару. Струшують пробірку. Спостерігають за зміною забарвлення суміші.
Спостереження:
Рівняння реакції:
Висновок:
Техніка безпеки
1. Усі досліди проводити у витяжній шафі при опущеному захисному склі.
2. З бромною водою та розчином брому в ССІ4 працювати у захисних окулярах!При попаданні бромної води або розчину брому в ССІ4 на шкіру нейтралізувати розчином аміаку.
3. Після проведення дослідів суміші з пробірок вилити у спеціальний посуд, що знаходиться у витяжній шафі. У раковину не виливати.
4. При попаданні сульфатної кислоти на шкіру змити великою кількістю води і нейтралізувати 1%-ним розчином гідрокарбонату натрію.
Контрольні запитання та завдання
- Наведіть механізм приєднання брому до α-пінену.
- Наведіть механізм бромування бензену, толуену.
- Порівняйте механізм електрофільного приєднання брому до α-пінену з механізмом бромування бензену (електрофільне заміщення ).
- Які речовини відносяться до ароматичних сполук? Наведіть правило Хюккеля.
- Наведіть рівняння реакції окиснення бутилбензену перманганатом калію при наявності сульфатної кислоти.
- Наведіть механізми та рівняння реакцій бромування ізобутилбензену в ядро та в боковий ланцюг.
- Наведіть визначення наступних понять: перехідний стан, проміжна сполука (інтермедіат), π–комплекс, σ –комплекс (як приклад використайте хлорування бензену при наявності AlCl3).
- Визначте електронні ефекти наведених замісників, якщо вони безпосередньо зв,язані з бензольним ядром: - СH2-СН3; - NO2; - CCl3; -CN; -COOH; -NH2 ; -OH; -NH3+ ;
- CH=CH2; -CH2-CH=CH2. Поясніть орієнтуючу здатність наведених замісників у реакціях SE, використавши резонасні структури. Які з цих замісників сприяють реакціям SE?
Завдання для самостійної роботи
Здійснити перетворення:
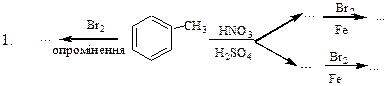
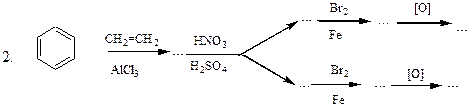
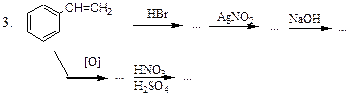
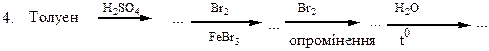
HNO3 Cl2 NaOH
5. Хлорбензен  …
…  …
…  …
…
H2 SO4 AlCl3 нагрівання
Перетворити в декілька стадій:
- Бензен
 2-бромо-6-нітротолуен.
2-бромо-6-нітротолуен. - Бензен
 3,4-дибромонітробензен.
3,4-дибромонітробензен. - Толуен
 3-нітро-4-хлоробензойна кислота.
3-нітро-4-хлоробензойна кислота. - Толуен
 2-нітро-6-хлоротолуен.
2-нітро-6-хлоротолуен. - Хлоробензен
 2-нітро-4-хлорофенол.
2-нітро-4-хлорофенол. - Толуен
 п-нітробензилбромід.
п-нітробензилбромід. - Бензен
 п-нітрофенетол (4-нітроетоксибензен).
п-нітрофенетол (4-нітроетоксибензен).
Виконати завдання: [2],№ 1.6.2, 5, 15, 16, 22, 24, 37 ;2.3.1, 4, 5, 6, 8, 17, 23, 29, 49, 50, 51.; 3.5.16, 17, 21, 24, 25 ,27, 28, 29, 32 ; 6.2.1, 5, ?, 8,16, 18, 27, 32, 33,34-39
Лабораторна робота 3
