Уравнение Нернста
Направление протекания ОВР.
Для того, чтобы узнать, протекает ли ОВР в прямом направлении, нужно сравнить Е0 окислителя и восстановителя. Мысленно компонуют гальванический элемент, состоящий из окислителя и восстановителя, и вычисляют электродвижущую силу химической реакции.
ЭДС = Е0ок – Е0вос
Если ЭДС>0 – протекает в прямом направлении.
ЭДС<0 – не протекает в прямом направлении.
ЭДС = Е0Cu/Cu2+ - Е0Zn/Zn2+
ЭДС = 0,34В – (-0,76В) = 1,1В
Окисление Zn не протекает.
Zn + 2H+ = Zn2+ + H2
восст окисл
ЭДС = Е02Н+/H2 – E0Zn/Zn2+ = 0В – (-0,76В) = 0,76В.
Протекает реакция.
Zn2+ + H2 = Zn0 + 2H+
ЭДС = Е0Zn/Zn2+ - E02H+/H2 = - 0,76В не протекает.
Если в растворе смесь катионов, то их восстановление будет протекать таким образом, что первой будет протекать реакция с наибольшим значением ЭДС.
Сравнивая Е0 металлов друг с другом, был составлен электрохимический ряд напряжения металлов (Бекетов). Согласно ряду: металлы расположены в порядке возрастания стандартного электродного потенциала. Металлы правее – окислители по отношению к металлам, расположенным левее. Левее расположенные металлы вытесняют металлы, стоящие справа из растворов солей – восстанавливают их. Чем дальше друг от друга стоят металлы, тем ЭДС больше.
∆σ0 = - nF∆E0, n – количество перешедших электронов, F – постоянная Фарадея, 96480Кл, ∆Е0 – ЭДС.
F – количество электричества, которое необходимо затратить, чтобы восстановить 1 эквивалент любого вещества.
Е0 металлов до водорода меньше 0. Н+ - окислители, металлы вытесняют водород из кислот. Металлы после водорода – окислители по отношению к водороду.
Электрохимический ряд напряжения металлов составлен для водных растворов, относительно поведения металла и его катиона в растворе.
В растворе ион находится в гидратированном виде. На Е0 сильное влияние оказывает Егидр, на Егидр – q/R.
Егидр (Li+) высока. В результате гидротации Е0 смещается влево.
ЕLi/Li+ = -3,01B.
В расплаве – четкая зависимость.
Кроме того, на реальное поведение металла в растворе оказывает влияние процесс пассивации. Он связан с внедрением молекул кислорода в поверхностный слой металла и изменением его физико-химических параметров. Обусловлен также наличием оксидной пленки, чем она тоньше и чем более плотно прилегает к поверхности металла, тем процесс пассивации выше. Поэтому А1, Сr, Fe в концентрированных H2SO4 и HNO3 не растворяются на холоде.
Е зависит от:
1). Температуры
2). Активности окислителя и восстановителя
3). Концентрации окислителя и восстановителя.
Уравнение Нернста.
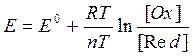
 при t=250С:
при t=250С:
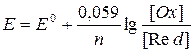
2Ag + 2HJ = 2AgJ + H2
E0Ag/Ag+ = 0,8B
ЭДС = 0В – 0,8В = - 0,8
ПРAgJ ≈ 10-16
EJ-/AgJ
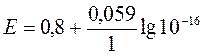
E = -0,14B, ЭДС = 0 - (- 0,14) = 0,14
1. образование труднорастворимого осадка.
2. реакции, идущие с образованием стойких комплексов.
Приводят к тому, что потенциалы смещаются в сторону отрицательных значений.
4Au + 8NaCN + 2H2O + O2 = 4Na[Au(CN)2] + 4NaOH - метод Багратиона.
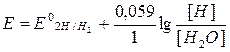
Е = Е0 + 0,059lg[H+]
E = -0,059pH
pH = 7 – вН2О
Е = -0,41В
Металлы, Е которых меньше – 0,41В вытесняют Н2 из воды.
