Аккумуляторы энергии в организме
Энергетический обмен. Цепь переноса протонов и электронов – 5 ферментативных комплексов. Окислительное фосфорилирование. Окислительные процессы, не связанные с запасанием энергии – микросомальное окисление, свободно-радикальное окисление, активные формы кислорода. Антиоксидантная система
Введение в биоэнергетику
Биоэнергетика, или биохимическая термодинамика, занимается изучением энергетических превращений, сопровождающих биохимические реакции.
Изменение свободной энергии (∆G) – это та часть изменения внутренней энергии системы, которая может превращаться в работу. Иначе говоря, это полезная энергия и выражается уравнением
∆G = ∆Н - Т∆S,
где ∆Н – изменение энтальпии (теплоты), Т – абсолютная температура, ∆S – изменение энтропии. Энтропия служит мерой неупорядоченности, хаотичности системы и возрастает при самопроизвольных процессах.
Если значение ∆G отрицательное, то реакция протекает самопроизвольно и сопровождается уменьшением свободной энергии. Такие реакции называют экзэргоническими. Если значение ∆G положительное, то реакция будет протекать только при поступлении свободной энергии извне; такая реакция называется эндэргонической. При ∆G равном нулю система находится в равновесии. Величина ∆G при стандартных условиях протекания химической реакции (концентрация веществ-участников 1,0 М, температура 25 ºС, рН 7,0) обозначается DG0¢ и называется стандартной свободной энергией реакции.
Жизненно важные процессы в организме – реакции синтеза, мышечное сокращение, проведение нервного импульса, транспорт через мембраны – получают энергию путем химического сопряжения с окислительными реакциями, в результате которых происходит высвобождение энергии. Т.е. эндэргонические реакции в организме сопряжены с экзэргоническими (рис.1).
 | |||
| |||
Рис.1. Сопряжение экзэргонических процессов с эндэргоническими.
Для сопряжения эндэргонических реакций с экзэргоническими реакциями необходимы аккумуляторы энергии в организме, в которых запасается примерно 50% энергии.
Аккумуляторы энергии в организме
1. Внутренняя мембрана митохондрий – это промежуточный аккумулятор энергии при получении АТФ. За счет энергии окисления веществ происходит «выталкивание» протонов из матрикса в межмембранное пространство митохондрий. В результате создается электрохимический потенциал (ЭХП) на внутренней мембране митохондрий. При разрядке мембраны энергия электрохимического потенциала трансформируется в энергию АТФ: Еокисл. ® Еэхп ® ЕАТФ. Для реализации этого механизма внутренняя мембрана митохондрий содержит ферментативную цепь переноса электронов на кислород и АТФ-синтазу (протонзависимую синтазу АТФ).
2. АТФ и другие макроэргические соединения. Материальным носителем свободной энергии в органических веществах являются химические связи между атомами. Обычным энергетическим уровнем возникновения или распада химической связи является ~ 12,5 кДж/моль. Однако имеется ряд молекул, при гидролизе связей которых выделяется более 21 кДж/моль энергии (табл.1). К ним относятся соединения с макроэргической фосфоангидридной связью (АТФ), а также ацилфосфаты (ацетил-фосфат, 1,3-бисфосфоглицерат), енол-фосфаты (фосфоенолпируват) и фосфогуанидины (фосфокреатин, фосфоаргинин).
Таблица 1.
Стандартная свободная энергия гидролиза некоторых фосфорилированных соединений
| Соединение | DG0¢ (кДж/моль) |
| Фосфоенолпируват | -61,9 |
| 1,3-Бисфосфоглицерат | -49,4 |
| Ацетил-фосфат | -43,1 |
| Фосфокреатин | -43,1 |
| Пирофосфат (РРн) | -33,5 |
| АТФ (®АМФ+РРн) | -32,2 |
| АТФ (®АДФ+Рн) | -30,5 |
| Глюкозо-1-фосфат | -20,9 |
| Фруктозо-6-фосфат | -13,8 |
| Глюкозо-6-фосфат | -13,8 |
| Глицерол-3-фосфат | -9,2 |
Основным макроэргическим соединением в организме человека является АТФ.
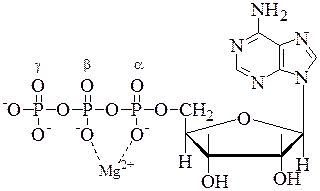
В АТФ цепочка из трех фосфатных остатков связана с 5’-ОН группой аденозина. Фосфатные (фосфорильные) группы обозначаются как a, b и g. Два остатка фосфорной кислоты соединены между собой фосфоангидридными связями, а a-остаток фосфорной кислоты – фосфоэфирной связью. При гидролизе АТФ в стандартных условиях выделяется -30,5 кДж/моль энергии.
При физиологических значениях рН АТФ несет четыре отрицательных заряда. Одной из причин относительной нестабильности фосфоангидридных связей является сильное отталкивание отрицательно заряженных атомов кислорода, которое ослабевает при гидролитическом отщеплении концевой фосфатной группы. Поэтому такие реакции являются высоко экзэргоническими.
В клетках АТФ находится в комплексе с ионами Mg2+ или Mn2+, координационно связанными с a- и b-фосфатом, что увеличивает изменение свободной энергии при гидролизе АТФ до 52,5 кДж/моль.
Центральное место в приведенной шкале (табл. 8.3) занимает цикл АТФ « АДФ + Рн. Это позволяет АТФ быть как универсальным аккумулятором, так и универсальным источником энергии для живых организмов.
В клетках теплокровных АТФ как универсальный аккумулятор энергии возникает двумя путями:
1) аккумулирует энергию более энергоемких соединений, стоящих выше АТФ в термодинамической шкале без участия О2 – субстратноефосфорилирование: S ~ Р + АДФ ® S + АТФ;
2) аккумулирует энергию электрохимического потенциала при разрядке внутренней мембраны митохондрии – окислительное фосфорилирование.
АТФ является универсальным источником энергии для совершения основных видов работы клетки (передача наследственной информации, мышечное сокращение, трансмембранный перенос веществ, биосинтезы): 1) АТФ+Н2О®АДФ+Рн; 2) АTФ + Н2О ® АМФ + РРн.
Во время интенсивных упражнений скорость использования АТФ может достигать 0,5 кг/мин.
Если ферментативная реакция термодинамически невыгодна, то она может осуществиться при сопряжении с реакцией гидролиза АТФ. Гидролиз молекулы АТФ изменяет равновесное отношение субстратов и продуктов в сопряженной реакции в 108 раз.
Для количественной оценки энергетического состояния клетки используют показатель – энергетический заряд. Многие реакции метаболизма контролируются энергетическим обеспечением клеток, который контролируется энергетическим зарядом клетки. Энергетический заряд может колебаться от 0 (все АМФ) до 1 (все АТФ). Согласно Д.Аткинсону, образующие АТФ катаболические пути ингибируются высоким энергетическим зарядом клетки, а утилизирующие АТФ анаболические пути стимулируются высоким энергетическим зарядом клетки. Оба пути функционируют одинаково при энергетическом заряде, близком к 0,9 (точка перекреста на рисунке 8.3). Следовательно, энергетический заряд, подобно рН, является буферным регулятором метаболизма (соотношения катаболизма и анаболизма). В большинстве клеток энергетический заряд колеблется в пределах 0,80-0,95.
Энергетический заряд = 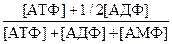
К макроэргическим соединениям относят также нуклеозидтрифосфаты, которые обеспечивают энергией ряд биосинтезов: УТФ – углеводов; ЦТФ – липидов; ГТФ – белков. В биоэнергетике мышц важное место занимает креатинфосфат.
3. НАДФН+Н+ – никотинамидадениндинуклеотидфосфат восстановленный. Это специальный аккумулятор с высокой энергией, который используется в клетке (цитозоль) для биосинтезов. R-CH3 + НАДФН2 + О2 ® R-CH2ОН + Н2О + НАДФ+ (здесь показано создание ОН-группы в молекуле).
Пути потребления кислорода (биологическое окисление)
В основе биологического окисления лежат окислительно-восстановительные процессы, определяемые переносом электронов. Вещество окисляется, если теряет электроны или одновременно электроны и протоны (водородные атомы, дегидрирование) или присоединяет кислород (оксигенирование). Противоположные превращения – восстановление.
Способность молекул отдавать электроны другой молекуле определяется окислительно-восстановительным потенциалом (редокс-потенциалом, Е0¢, или ОВП). Редокс-потенциал определяют путем измерения электродвижущей силы в вольтах. В качестве стандарта принят редокс-потенциал реакции при рН 7,0: Н2 « 2Н+ + 2е-, равный -0,42 В. Чем меньше потенциал окислительно-восстановительной системы, тем легче она отдает электроны и в большей степени является восстановителем. Чем выше потенциал системы, тем сильнее выражены ее окислительные свойства, т.е. способность принимать электроны. Это правило лежит в основе последовательности расположения промежуточных переносчиков электронов от водородов субстратов до кислорода.
При изучении окислительных процессов в клетках целесообразно придерживаться следующей схемы использования кислорода (табл. 2).
Таблица 2
Основные пути использования кислорода в клетках
| ОКИСЛЕНИЕ СУБСТРАТА (R) | ||||
| Дегидрирование | Оксигенирование | Свободно-радикальное окисление | ||
| -2Н | -2Н | +½ О2 | +О2 | О2¯· НО· NО∙ ONOO- озон |
| на ½ О2 | на О2 | |||
| Н2О | Н2О2 | R-OH | RO2 | |
| Тканевое дыхание | Простые окислительные системы | Монооксиге- назный путь | Диоксиге- назный путь | |
| АТФ | Обезвреживание | Обезвреживание | Разрыв ароматических колец | |
| Тепло | Тепло |
Здесь рассматриваются три основных пути: 1) окисление субстрата путем дегидрирования с переносом двух атомов водорода на атом кислорода с образованием Н2О (энергия окисления аккумулируется в форме АТФ, на этот процесс расходуется более 90% кислорода) или молекулу кислорода с образованием Н2О2; 2) присоединение атома кислорода с образованием гидроксильной группы (повышение растворимости субстрата) или молекулы кислорода (метаболизм и обезвреживание устойчивых ароматических молекул); 3) образование кислородных свободных радикалов, служащих как для защиты внутренней среды организма от чужеродных макромолекул, так и для повреждения мембран в механизмах окислительного стресса.
В биохимии и клеточной биологии под тканевым (клеточным) дыханием понимают молекулярные процессы, в результате которых происходит поглощение клеткой кислорода и выделение углекислого газа. Клеточное дыхание включает 3 стадии. На первой стадии органические молекулы – глюкоза, жирные кислоты и некоторые аминокислоты – окисляются с образованием ацетил-КоА. На второй стадии ацетил-КоА вступает в ЦТК, где его ацетильная группа ферментативно окисляется до СО2 и выделяется HS-КоА. Энергия, высвобождающаяся при окислении, накапливается в восстановленных переносчиках электронов НАДН и ФАДН2. На третьей стадии электроны переносятся к О2, как конечному акцептору, через цепь переносчиков электронов, которая называется дыхательная цепь или цепь переноса электронов (ЦПЭ). При переносе электронов по дыхательной цепи выделяется большое количество энергии, которая используется для синтеза АТФ путем окислительного фосфорилирования.
Процесс тканевого дыхания оценивают с помощью дыхательного коэффициента:
RQ = число молей образованного СО2/число молей поглощенного О2.
Этот показатель позволяет оценить тип топливных молекул, используемых организмом: при полном окислении углеводов дыхательный коэффициент равен 1, белков – 0,80, жиров – 0,71; при смешанном питании величина RQ=0,85. Газометрическим методом Варбурга изучают тканевое дыхание в срезах органов: при окислении углеводных субстратов коэффициент СО2/О2 стремится к 1, а при окислении липидных субстратов – 04-07.
ЦПЭ встроена во внутреннюю мембрану митохондрий. Электроны перемещаются по цепи от более электроотрицательных компонентов к более электроположительному кислороду: от НАДН (-0,32 В) до кислорода (+0,82 В).
ЦПЭ – это универсальный конвейер по переносу электронов от субстратов окисления к кислороду, построенный в соответствии с градиентом окислительно-восстановительного потенциала. Главные компоненты дыхательной цепи расположены в порядке возрастания их окислительно-восстановительного потенциала. В процессе переноса электронов по градиенту окислительно-восстановительного потенциала высвобождается свободная энергия.
Строение митохондрий
Митохондрииявляются органеллами клеток.Наружная мембрана проницаема для многих малых молекул и ионов, поскольку содержит много митохондриальных поринов – белков с молекулярной массой 30-35 кДа (называются также VDAC). Электрозависимые анионные каналы VDAC регулируют поток анионов (фосфаты, хлориды, органические анионы и адениловые нуклеотиды) через мембрану. Внутренняя мембрана митохондрий не проницаема для большинства ионов и полярных молекул. Имеется ряд специальных переносчиков для АТФ, пирувата и цитрата через внутреннюю мембрану митохондрий. Во внутренней мембране митохондрий выделяют матриксную (N) поверхность и цитозольную (Р) поверхность.
Митохондрии содержат собственную кольцевую ДНК, которая кодирует синтез ряда РНК и белков. Человеческая митохондриальная ДНК содержит 16569 пар оснований и кодирует 13 белков цепей переноса электронов. Митохондрии также содержат также ряд белков, которые кодируются ядерной ДНК.
