Ионный обмен. Сущность процесса, применение, оборудование
Ионный обмен (ИО)
Ионообменная очистка применяется для извлечения из сточных вод металлов (цинка, меди, хрома, никеля, свинца, ртути, кадмия, ванадия, марганца и др.), а также соединений мышьяка, фосфора, цианистых соединений и радиоактивных веществ. М-од широко примен-ся в пр-сах водоподготовки для удаления солей жесткости. Временная жесткость воды обусловлена гидрокарбонатами Са и Mg. Эта жес-ть удал-ся при кипячении Ca(HCO2)2→CaCO3+CO2+H2O и Mg(HCO3)2. Постоянная жес-ть обусловлена наличием сульфатов Са и Mg. (СаSO4 и MgSO4 – не удал-ся при кипячении)
Сущность метода. Ионный обмен представляет собой процесс взаимодействия раствора с твердой фазой (иониты), обладающей свойствами обменивать ионы, содержащиеся в ней, на другие ионы; присутствующие в растворе. Тв фаза наз ИОНИТ, которые практически нерастворимы в воде.
При ИО ионы Н+и ОН- обмениваются на эквивалентное кол-во ионов того же знака ионита. Катиониты поглащ из растворов положительные ионы (катионы), Аниониты поглащ из растворов отрицательные ионы (анионы). Катиониты облад кислотными св-вами, а аниониты - основными св-вами. Амфотерные иониты обменивают и катионы и анионы. Иониты бывают неорганич (минеральные) и органич. Это природные в-ва или получены искусственно. Неоргаюгч природные иониты: цеолиты, глинистые минералы, полевые шпаты. Катионно-обменные св-ва их обусловлены содержанием алюмосиликатов. Цеолиты образ-ся при нагревании алюмосиликатов, когда требуется вода и получ-ся пористая структура с большой пов-тью. К неорганнч синтетич ионитам относ: силикагели, пермутиты и труднораствор-ые оксиды и гидроксиды некот-х Mе(Al, хром, цирконий). Органич иониты природные: гуминовые кислоты почв и углей. Органич иониты искусственные: ионообменные смолы, кот представл собой высокомолекулярные соединения и кот имеют развитую пов-ть. Органич и неорганич иониты представл собой 3-ех мерный каркас, в кот нах-ся группы атомов, несущие заряд противоионы. Основа ионита(матрица) состоит из пространственно сшитых углеводородных цепей с жестко закрепленными на них активными ионогенными группами(отрицательно заряженными на катионите и + на анионите),заряд которых нейтрализ-ся располож внутри полимера ионами противоп знака( противоионами),способными вступать в реак обмена с ионами того же знака заряда из р-ра.В зависимости от степени диссоциации катионообменные смолы подразделяются на сильно- и слабокислотные,а анионообменные на сильно- и слабоосновные.Сильнокислотные катиониты содержат сулъфогруппы (-SO3H),Н -противоион. Слабокислотные катиониты - карбоксильную группу(-СООН) и фенольную (-С6Н4ОН). Сильноосновные иониты — это четвертичные аммонивые основания, к слабоосновным - аминогруппы различной степени замещения. Реге-нерация ионита: катиониты промывают р-рами кислот 2-8% -растрами, а отраб-ые иониты промывают р-рами щелочей 2-6% растворами. Проц ионного обмена можно разделить на стадии:1- диффузия ионов в рас-ре к пов-сти зерен ионита;2-диффузия их внутри зерна;3-прохождение р-ции обмена ионов;4-диффузия вытесненного противоиона к поверхности зерна; 5-диффузия противоиона от поверхности зерна ионита в объем р-ра.
Скорость ИО определ самой медленной из этих стадий- диффузией в пленке жидкости либо диффузией в зерне ионита. Перенос в-ва из рас-ра ионита м.б. представлен в неск стадий: 1) перенос ионов А из ядра потока жидкости к внешней поверхности пограничной жидкой пленки, окружающей зерно ионита; 2) диффузия ионов через пограничный слой; 3) переход иона через границу раздела фаз в зерно смолы; 4) диффузия ионов А внутри зерна смолы к ионообменным функциональным группам; 5) собственно химическая реакция двойного обмена ионов А и В; 6) диффузия ионов В внутри зерна ионита к границе раздела фаз; 7) переход ионов В через границу раздела фаз на внутреннюю поверхность пленки жидкости; 8) диффузия ионов В через пленку; 9) диффузия ионов В в ядро потока жидкости.
В общем виде- р-ция ионного обмена mА+RmВ=mRmA+B. Реакция ИО идет до уст-го ионного равновесия. МАХ кол-во ионов, кот. поглащ-ся обменным путем 1г ионита назыв емкостью поглощения или обменной емкостью (включ полную ОЕ,равновесную ОЕ,полную динамическую и динамич). Полная емкость ионита - это кол-во, нах-ся в сточной воде г*экв ионов, кот-е м. поглатить 1м3 ионита до начала проскока в фильтрах поглощаемых ионов. ПОЕ опред-ся числом функцион групп,способных к ионному обмену в ед. массы сухого ионита или набухшего ионита(мг экв/г,экв/л),она яв-ся const и указ в паспорте ионита. Она не зависит от концентрили природно обменивающегося иона.
Основой при выборе ионита яв-ся равновесная ОЕ,зависящая от ряда факторов(природа ионита,степень набухаемости,pH среды,концен р-ра и др).
ДОЕ-динамич ОЕ,характер-ая кол-во поглощ-го иона до момента его проскока в фильтрат.ИО сточных вод и обессоливание воды осущ-ся в различ-х аппаратах, наиб применение получили: ионообменные фильтры для фильтрования сточн воды в плотном слое. Для обессоливания водыпримем Н-катионитовые фильтры.
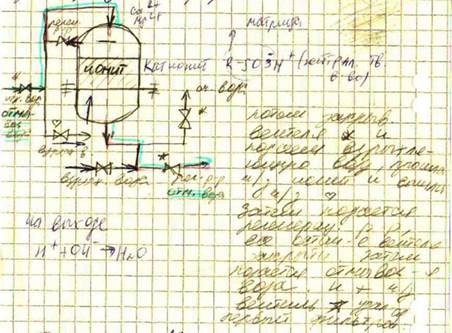
Цикл работы состоит: 1-умягчение;2-взрыхление;3-регенерация;4-отмывка. Взрых нужно для устранения уплотнения ионита,препятств-го доступу регенерац-го р-ра к его зернам. Регенерация катионита для обогащения его ионами H+ (Na) производится р-рами кислот серной или соляной(р-ром NaCl), регенерация анионита-раствором щелочи NaOH.
Фильтр-вертик однокамерный цилиндрич аппарат,состоящ из корпуса,ниж и верх распределит устройств,трубопров,запорной арматуры,пробоотборного устр-ва и фильтрующ загрузки.
Реген р-р и продукты регенерации после отмывки подаются в направлении сверху вниз в //-точных ионитных фил-х; в противот ф-рах реген р-р и обрабатываемая вода пропуск-ся в противоп направлен . при этом обрабатыв вода перед выходом из ф-ра соприкас с хорошо отрегенерирован слоями ионита,благодаря чему обеспечив более глубок ИО и повыш кач-во отработанной воды.
