Метод нейтралізації -кислотно - основне титрування
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
ОДЕСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ ІМ. І.І. МЕЧНИКОВА
ХІМІЧНИЙ ФАКУЛЬТЕТ
КАФЕДРА АНАЛІТИЧНОЇ ХІМІЇ
ТЕРМІНОЛОГІЧНИЙ СЛОВНИК
З
АНАЛІТИЧНОЇ ХІМІЇ
ОДЕСА 2010
А
Автопротоліз – процес перенесення протону від однієї молекули розчинника до іншої.
Адсорбція - процес поглинання речовини на поверхні розподілу фаз.
Активність – ефективна концентрація, яка проявляє себе в хімічних процесах в якості реально діючої на відміну від загальної концентрації речовин в розчині.
Акцептор -частинка з вільною орбітою, яка приймає електронну пару.
Аналіз– метод дослідження, оснований на розкладанні даного обۥєкту на більш прості складові.
Аморфний осад-осад, який не має кристалічної будови.
Аналіз структурний – метод аналізу, який встановлює порядок звۥязків атомів в молекулі.
Аналіт – об’єкт, який підлягає аналізу.
Аналітика - термін, який інколи використовують замість терміна «аналітична хімія»; а також в якості елементу студентського сленгу.
Аналітичні властивості – особистий колір або здатність утворювати забарвлені сполуки, а також осади, гази, кристали певного кольору та форми при взаємодії з певними хімічними реагентами.
Аналітичний контроль – перевірка відповідності речовини або партії матеріалів, яку контролюють, установленим вимогам.
Аналітичні реагенти – реактиви, які використовують для проведення аналітичних реакцій.
Аналітична реакція – це реакція, яка закінчується аналітичним ефектом і дозволяє визначити наявність або кількість певних часток в речовині або в розчині.
Аналітичний сигнал – фізична величина, яка вимірюється на заключній стадії аналізу і залежить від вмісту компоненту, який визначається (сила струму, ЕРС, оптична густина, інтенсивність випромінювання тощо).
Аналітична служба – це сервісна система, яка забезпечує конкретний аналіз певних об`єктів з використанням методів, які рекомендуються аналітичною хімією.
Аналітична хімія – наука, яка розвиває теоретичні основи аналізу хімічного складу речовини і розробляє методи ідентифікації, виявлення, визначення та розділення хімічних елементів і їх сполук, а також методи встановлення хімічної будови речовин.
Ауксохроми- групи атомів, введення яких в молекули барвників підсилює їх колір.
Б
Буферна дія – дія буферних розчинів, яка основана на тому, що компоненти буферних сумішей зв`язують іони гідрогену кислот або гідроксиду основ, які додаються, з утворенням слабких електролітів.
Буферна ємність – визначається кількістю молей сильної кислоти або лугу, додавання яких до 1л буферного розчину змінює його рН на 1.
Буферні розчини – розчини, які здатні зберігати постійне значення рН при додаванні до них невеликих кількостей сильних кислот або лугів, а також при розведенні.
В
Вибірковість – Виявлення або визначення деяких часток (елементів, іонів, тощо) на фоні інших.
Відновник- атом, молекула або іон, який віддає електрони.
Відтворюваність – характеризує ступінь близькості один до одного одиничних визначень, розсіювання одиничних результатів відносно середнього.
Водневий показник – характеризує концентрацію (активність) іонів гідрогену у розчинах. Чисельно дорівнює від`ємному десятичному логарифму концентраціі (активності) водневих іонів [Н+], яка виражена у моль/л: рН= -lg[H+].
Вторинний стандарт – розчин, який не відповідає вимогам для первинних стандартів. Його готують приблизно і встановлюють точну концентрацію в день роботи по первинному стандарту ( HCl, NaOH, KMnO4, AgNO3 )
Г
Гель– желеподібний осад, який утворюється внаслідок злипання колоїдних часток.
Гетерогенна система – система, яка складається з двох чи декількох фаз, відокремлених поверхнею розділу.
Гомогенна система(однорідна, однофазна) – система, хімічний склад та фізичні властивості якої у всіх частинах однакові або змінюються безперервно. Між частинами системами немає поверхні розділу фаз .
Гравіметрія (ваговий аналіз)– метод кількісного аналізу, оснований на точному вимірюванні маси продукту хімічної реакції.
Групи аналітико-активні (ААГ) – групи атомів, які змінюють аналітичні властивості продукту реакції (розчинність, колір тощо).
Групи функціонально-аналітичні (ФАГ)– це групи атомів органічного реагенту, які обумовлюють його взаємодію з певним іоном металу.
Д
Дентатність – кількість координаційних зв`язків, які ліганд може утворювати з комплексоутворювачем. Визначається кількістю донорних атомів лігандів.
Десорбція - процес видалення речовин, які адсорбовані, з поверхні сорбенту.
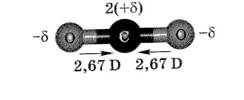 Диполь – полярні молекули, які мають два рівних за величиною і протилежних за знаком зарядів, що знаходяться на деякій відстані один від одного.
Диполь – полярні молекули, які мають два рівних за величиною і протилежних за знаком зарядів, що знаходяться на деякій відстані один від одного.
Дистиляція – перехід речовини із рідкого стану в газоподібне з наступною конденсацією у вигляді рідинної фази.
Дистильована вода – це вода, яка не містить неорганічних і органічних домішок, її одержують методом дистиляції.
Добуток розчинності – добуток концентрацій іонів малорозчинного електроліта в його насиченому розчині.
Донор– частинка, яка представляє для зв`язку електронну пару.
Е
Еквівалент –кількість хімічного елементу (речовини), яка взаємодіє з 1 молем (еквівалентом) атомів гідрогену.
Екстракція– розподіл речовин між двома рідинними фазами, які не змішуються.
Електродний потенціал (Е) редокс-пари (окилювально - відновний, електрохімічний, редокс-потенціал) – це електрорушійна сила (ЕРС) гальванічного ланцюгу, який складається з окислювально-відновного електроду (електроду ІІІ роду) та стандартного водневого електроду.
З
Золі (колоїдні розчини) – високодисперсні мікрогетерогенні (неоднорідні) системи, які зберігають поверхню розділу фаз між дисперсною фазою та дисперсійним середовищем.
І
Ідентифікація – ототожнення, тобто визнання однаковим, подібним.
Ізоморфізм (Утворення твердих розчинів заміщення) - явище утворення кристалів однакової форми але різного складу внаслідок заміщення одних атомів, іонів чи молекул в кристалічній решітці іншими. .
Ізоелектрична точка– точка, в якій змінюється знак заряду колоїдної частки.
Індикатор – реактив або пристрій, який реагує на зміну певних фізичних або хімічних характеристик.
Індикатори адсорбційні –органічні барвники, які змінюють свій колір внаслідок адсорбції на поверхні осаду.
Індикатори кислотно–основні– органічні речовини, які змінюють своє забарвлення в залежності від кислотно-основних характеристик розчину (рН).
Індикатори металохромні – органічні речовини (барвники), які утворюють забарвлені сполуки з іонами металів. Використовуються в комплексонометрії.
Індикатори необернені – індикатори, які змінюють свій колір (внаслідок руйнування) тільки в напрямку прямої реакції.
Індикатори обернені– змінюють свій колір як у напрямку прямої, так і оборотної реакції.
Індикатори окислювально-відновні (редокс - індикатори)– органічні барвники (або комплекси органічних лігандів з металами, які змінюють степінь окиснення), які змінюють свій колір в залежності від окислювально-відновного потенціалу розчину.
Індикатори специфічні– індикатори, які утворюють забарвлену сполуку з певним компонентом окислювально-відновної системи (крохмаль з йодом).
Інтервал переходу забарвлення індикатору – інтервал рН, в якому помітно змінюється колір індикатору.
Іонна сила розчину– вплив усіх іонів розчину на активність реагуючих часток.
К
Кількісний аналіз – метод аналізу, який визначає кількість часток (елементів, іонів, ізотопів, функціональних угрупувань, хімічних сполук, тощо) в об¢єкті, який аналізують.
Кінцева точка титрування- момент зміни кольору індикатору від однієї краплини розчину, який додають з бюретки.
Коагуляція– процес злипання колоїдних часток внаслідок втрати ними заряду.
Коефіцієнт активності – відношення активності частки до її рівноважної концентрації.
Комплексні сполуки (координаційні сполуки) – молекули або іони, які утворюються внаслідок приєднання к центральному іону або атому (комплексоутворювачу) нейтральних молекул або інших іонів (лігандів), і здатні існувати як у кристалі, так і у розчині.
Комплексонометрія –титриметричний метод, заснований на реакціях утворення комплексних сполук іонів металів з етилендіамінтетраоцтовою кислотою і її похідними (комплексонами).
Концентрування– підвищення концентрації мікрокомпонентів до рівня, який забезпечує їх визначення з певною похибкою.
Координаційне число – кількість координаційних зв`язків, які здатен утворювати центральний атом з лігандом.
Кристалізація– утворення зародків твердої фази при охолодженні розчину, розтопу або газу.
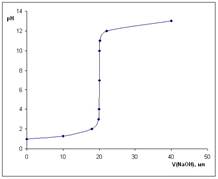
Крива титрування - – це графічна залежність між змінами рН, Е, рKat, pAn та об’ємом робочого розчину.
Л
Ліганди– іони або молекули, які утримуються комплексоутворювачем .
М
Макроаналіз – аналіз речовин або їх сумішей в кількостях, які перевищують 0,1г.
Маскування – перетворення іонів, які заважають визначенню, у сполуки, які не реагують (утворення комплексів або зміна степеню окиснення).
Масова частка (процентна концентрація)– маса сполуки, яка міститься в 100г розчину або будь-якої речовини.
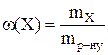 ×100 %
×100 %
Метод нейтралізації -кислотно - основне титрування.
Мікроаналіз – аналіз, при якому маса проби складає менш ніж 0,01 г.
Молярна концентрація –кількість молей речовини, які містяться в 1 літрі розчину.
СМ(Х) = 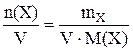
Молярна концентрація еквіваленту (нормальна концентрація) – кількість молей еквіваленту, які містяться в 1 літрі розчину.
СН(Х) = 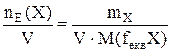
Моніторинг – регулярний аналітичний контроль; перевірка відповідності певних компонентів встановленим стандартам.
О
Окиснення – процес віддачі електронів атомом, молекулою чи іоном
Окисники– атоми, молекули або іони, які приймають електрони.
Оклюзія (утворення твердих розчинів упровадження) – упровадження сторонніх іонів між вузлами кристалічної решітки осаду, який утворюється.
Осадження – процес утворення осаду в насиченому розчині.
Осади – це тверда фаза гетерогенної системи, яка утворюється внаслідок процесу осадження.(кристалічні та аморфні в залежності від умов).
П
Пептизація –процес перетворення гелю на колоїдний розчин.
Первинний стандарт – розчин, який можна приготувати з точністю до четвертого знаку після коми і який зберігає постійну концентрацію довгий час.
Показник титрування (рТ) –значення рН, при якому спостерігається різка зміна забарвлення індикатору. рТ = рКинд.
Помилки індикаторні- при помилки, які виникають титруванні внаслідок неправильного вибору індикатора.
Помилка сольова – помилка титрування, яка виникає в концентрованих розчинах, внаслідок збільшення їх іонної сили.
Протоліз – перенос протону від молекули або іону однієї речовини до іншої.
Протолітометрія – титриметричний метод заснований на реакціях нейтралізації.
Р
Редоксометрія (оксидиметрія, окислювально-відновне титрування) – титриметричний метод, заснований на перебігу окислювально-відновних реакцій.
Робочий розчин– розчин, яким титрують. Ним можуть бути як вторинні, так і первинні стандарти.
Розчинники – рідини, які здатні розчиняти тверді, рідинні та газоподібні речовини.
Розчинність – це загальна концентрація речовини у його насиченому розчині.
С
Сольватація – взаємодія молекул розчинника з частками розчиненої речовини.
Сольовий ефект– підвищення розчинності осаду в присутності стороннього електроліту.
Сорбція – процеси поглинання речовин твердими речовинами чи розчинами.
Співосадження – захват домішок (мікрокомпонетів) осадом макрокомпонента.
Стандарт-титр (фіксанал) - ампула, яка містить точно відому кількість речовини (найчастіше 0,1 моль).
Стандартний електрохімічний потенціал – потенціал окислювально-відновної пари (редокс-пари), який вимірюються в відносно стандартного водневого електроду при концентрації іонів 1 моль/л і температурі 25°С .
Старіння осаду – процес росту великих кристалів за рахунок розчинення маленьких у випадку, коли осад залишають на деякий час у розчині.
Ступінь гідролізу – відношення концентрації гідролізованої частки до вихідної концентрації речовини.
aГ 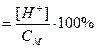
Ступінь дисоціації – число, що показує, яка частина від загальної кількості речовини, що знаходиться в розчині, розпадається на іони.
a 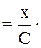 100 %.
100 %.
Стрибок титрування - це різка зміна значень рН (Е, рKat, pAn.) при дуже маленькій (99,9-100,1 мл.= 0,2 мл.) зміні об’єму робочого розчину.
Т
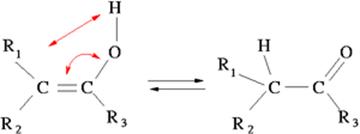
Таутомерія –явище динамічної ізомерії, при якому два чи більше ізомери легко переходять один в одного.
Титр – концентрація розчину в г/мл.
T(A) = 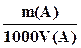
Титрант (робочий розчин) – розчин, концентрація якого встановлена точно (до четвертого знаку після коми).
Титриметрія (обۥємний аналіз) – метод встановлення концентрації вимірюванням об`ємів розчинів речовин, які прореагували.
Титрування – процес точного визначення об`єму робочого розчину шляхом додавання його по краплинах.
Титрування оборотне –ґрунтується на додатку до розчину, який аналізують, надлишку робочого розчину і наступним титруванням його залишку.
Точка стехіометричності (еквівалентності)- момент закінчення хімічної реакції.
Точність – характеристика метода чи методики, яка включає в себе їх правильність та відтворюваність.
Трилонометрія –метод комплексонометричного титрування з використанням Трилону Б.
У
Ультрамікрометоди– це методи, в яких для аналізу використовується маса проби речовини <10-4 г або об`єм розчину в мл <10-3.
Ф
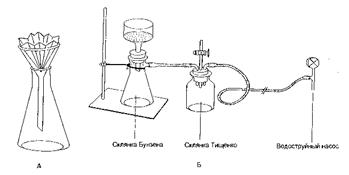
Фільтрування – відокремлення твердих частинок, які знаходяться в рідині, шляхом пропускання її через пористу перегородку.
Х
Хелати – комплекси іонів металів з органічними реагентами, які мають циклічну структуру.
Хемосорбція – процес поглинання, якій супроводжується хімічною взаємодією.
Хімічний аналіз – визначення хімічного складу (якісного та кількісного) і структури речовин.
Хромофори– групи атомів, які надають забарвлення органічним сполукам. Головною їх ознакою є наявність супряжених подвійних зв’язків.
Ч
Чутливість метода – мінімальна кількість речовини, яке можливо виявити чи визначити даним методом з певною похибкою.
Я
Якісний аналіз - метод аналізу, який використовують для виявлення (ідентифікації) певних часток речовини: елементів, іонів, ізотопів, функціональних угрупувань, тощо.
