Хлористые соединения урана
Известны четыре хлорида урана UCl3, UCl4, UCl5, UCl6. Наибольшее значение имеет UCl4.
Тетрахлорид урана
Тетрахлорид урана – темнозеленое кристаллическое вещество с металлическим блеском. Он имеет сравнительно низкие температуры плавления (590 ± 10С) и кипения (7920С). Пары окрашены в красный цвет. Расплавленный UCl4 хороший проводник электричества.
Тетрахлорид урана очень гигроскопичен, поглощая влагу он выделяет хлористый водород:
UCl4 + H2O = UOCl2 + 2HCl
Растворяясь в воде с выделением тепла, UCl4 образует зеленые растворы. Высокая кислотность этих растворов свидетельствует о том, что UCl4 в водных растворах сильно гидролизуется.
Метиловый, этиловый спирты, ацетон, этилацетат и др. полярные растворители растворяют UCl4 , а неполярные (бензол, четыреххлористый углерод и др.) не растворяют его.
При повышенных температурах кислород окисляет UCl4 до UO2Cl2, а затем до U3O8:
UCl4 + O2 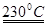 UO2Cl2 + Cl2
UO2Cl2 + Cl2
3 UO2Cl2 + O2 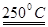 U3O8 + 3Cl2
U3O8 + 3Cl2
Хлором UСl4 может окисляться до UCl5 и UCl6 . Водородом при
525¸5500С восстанавливается до UCl3:
2UCl4 + H2 = 2UCl3 + 2HCl
Металлические Li, Na, K, Ca, Mg, Al восстанавливают тетрахлорид урана до металлического урана:
UCl4 + 2Ca = U + 2CaCl2.
Вследствие координационной ненасыщенности UCl4 образует большое число комплексных соединений: Na[UCl5], Na2[UCl6] и др.
UCl4 может быть получен при взаимодействии двуокиси урана с такими агентами, как CCl4, COCl2, SO2Cl2, PCl5, SOCl2:
UO2 + CCl4 = UCl4 + CO2.
Применяется при переработке некоторых урановых руд методом хлорирования, для получения металлического урана .
СОЛИ УРАНИЛА
Азотнокислый уранил
Азотнокислый уранил из водных растворов выкристаллизовывается в виде призм желто - зеленого цвета, состав образующегося кристаллогидрата UO2(NO3)2×6H2O. Безводный нитрат уранила получить нагревом при обычных условиях трудно, т.к. начинает разлагаться сама соль. Разложение нитрата уранила до UO3 заканчивается при температурах 3300С, а при нагреве выше 6000С образуется U3O8.
Нитрат уранила хорошо растворим в воде (при 200C 54,4%), эфирах, спиртах, альдегидах, кетонах, но не растворим в четыреххлористом углероде, бензоле, толуоле. Его растворимость во многих органических растворах сравнима с растворимостью его в воде, что делает возможным его выделение методом экстракции.
Азотнокислый уранил взаимодействует со щелочами и аммиаком, давая диуранаты, с перекисью водорода – пероксид уранила, со щавелевой кислотой – оксалат уранила и пр.
В водных растворах легко диссоциирует, давая гидратированные ионы UO22+, а также комплексные ионы [UO2(NO3)]+, [UO2(NO3)3]- и др. Он способен к образованию комплексных соединений типов:
MeI[UO2(NO3)3], MeII[UO2(NO3)4].
Азотнокислый уранил широко используется в технологии: вскрытие руд азотной кислотой, экстракционный аффинаж, аффинаж кристаллизацией уранил нитрата, растворение облученного металлического урана, экстракционное разделение урана и плутония, и оксалатов и пр.
Сернокислый уранил
Сернокислый уранил выкристаллизовывается в виде UO2SO4 × 3H2O, при нагревании UO2SO4 × 3H2O до 1500С образуется моногидрат, а при более сильном нагреве, выше 1750С, безводная соль. Сульфат уранила чрезвычайно термически стоек, разлагается на UO3+SO3 лишь при температуре темно-красного каления 680 0С (при более высокой температуре UO3+SO2 + ½ О2).
Тригидрат сульфата уранила кристаллизуется в виде лимонно-желтых призматических кристаллов. Он хорошо растворим в воде. Растворимость при 250С UO2SO4 × 3H2O, в воде составляет 50% безводного сульфата уранила, с повышением в растворе концентрации H2SO4 растворимость резко падает, достигая 1-2% при содержании H2SO4 60%. В разбавленной серной кислоте растворы легко восстанавливаются до 4-х валентного сульфата урана. В сульфатных растворах уранил склонен к образованию комплексных соединений, так при рН=1-2 образуются ионы [UO2(SO4)3]4-, [UO2(SO4)2]2-, которые хорошо адсорбируются на анионитах и экстрагируются аминами.
Комплексные соли сульфата уранила известны с Li, Na, K, Rb, Cs, NH4+,Tl и т.д.
Сернокислотный уранил взаимодействует со щелочами, давая диуранаты; со щавелевой кислотой – оксалаты и пр.
Получается действием H2SO4 на UO3, (NH4)2U2O7 и др. соединения, или на U3O8 серной кислотой с окислителем, например:
U3O8 +4H2SO4 + MnO2 = 3UO2SO4 +4H2O
Применяется при сернокислотном вскрытии руд, при сорбционном и экстракционном выделении урана из растворов и пульп, при получении U(SO4)2 .
