Пример 3. Назвать соли: AlN, (CuOH)2CO3 , Al2(SO4)3, MgHCO3. Написать их графические формулы.
Решение:
AlN – нитрид алюминия
Al ≡ N
(CuOH)2SO4 – сульфат гидроксо меди (II) Al2(SO4)3 – сульфат алюминия
H − O − Cu − O O O − S = O
\ // / / \\
S Al − O O
/ \\ \
H − O − Cu − O O O − S = O
/ \\
O O
/
Al − O O
\ \ //
O − S = O
Mg(HCO3)2 – гидрокарбонат магния
H − O
|
O − C = O
/
 Mg O − C = O
Mg O − C = O
 |
 О Н
О Н
Пример 4
Напишите уравнения реакций получения солей из оксидов хрома.
Решение: Хром в соединениях имеет степень окисления +6, +3, +2. Его оксиды CrO3, Cr2O3 и CrO, соответственно, кислотный, амфотерный и основной. Уравнения реакций, характеризующие их способность образовывать соли, следующие:
CrO3 + 2NaOH = Na2CrO4 + H2O
Cr2O3 + 6 HCl = 2CrCl3 + 3H2O
Cr2O3 + 2NaOH = 2NaCrO2 + H2O
CrO + 2HCl = CrCl2 + H2O
Пример 5
С какими из перечисленных веществ вступит в реакцию серная кислота: KOH, CuO, Ba(OH)2, Fe2O3, Al2O3, CO2, SiO2, H3PO4, O2, H2O? Составьте уравнения возможных реакций
Решение: Серная кислота не взаимодействует с веществами имеющими кислотные свойства (H3PO4, CO2, и SiO2) и с кислородом, т.к. она не способна окисляться.
Уравнения возможных реакций
H2SO4 + 2KOH = K2SO4 + 2H2O
основание
H2SO4 + СuO = CuSO4 + H2O
основной
оксид
H2SO4 + Ba(OH)2, = Ba SO4 + 2H2O
основание
3H2SO4 + Fe2O3 = Fe2(SO4)3+ 3H2O
амфотерный
оксид
3H2SO4 + Al2O3 = Al 2(SO4)3+ 3H2O
амфотерный
оксид
H2SO4 + KOH = KНSO4 + H2O
2H2SO4 + СuO = Cu(HSO4)2 + H2O
H2SO4 (конц.) + nH2O= H2SO4 ∙ nH2O
олеум
Пример 6. Назовите приведенные здесь кислую, основную соли: Al(OH)2Cl, Ba(HSO3)2. Напишите реакции, с помощью которых их можно превратить в средние соли.
Решение:
Al(OH)2Cl – основная соль, хлорид дигидроксоалюминия
Ba(HSO3)2 – кислая соль, гидросульфит бария
1) Основная соль – та соль, в формуле молекулы которой имеется гидроксид - ион.
2) Кислая соль – та соль, в молекуле которой содержится ион водорода.
3)Средняя соль – молекула такой соли содержит катион металла и кислотный остаток, не
содержащий ион водорода.
Основную соль в среднюю превращают добавлением кислоты
Al(OH)2Cl + 2HCl = AlCl3 + 2H2O.
Кислую соль превращают в среднюю действием на нее основания
Ba(HSO3) + Ba(OH)2 = 2BaSO3 + 2H2O.
Пример 7. Написать реакции с помощью которых можно осуществить следующие превращения
Al2O3 → KAlO2 → Al(OH)3 → AlOHSO4 → Al2(SO4)3 → Al → Al(NO3)3
Решение:
а) Al2O3+ 2KOH = 2KAlO2 + H2O
метаалюминат
калия
б) 2KAlO2 + H2SO4 + 2H2O → 2Al(OH)3 + K2SO4
в) Al(OH)3 + H2SO4 = AlOHSO4 + 2H2O
недост. сульфат
гидроксоалюминия
г) 2AlOHSO4 + H2SO4 = Al2(SO4)3 + 2H2O
сульфат
алюминия
д) Al2(SO4)3 + 3Mg = 2Al + 3MgSO4
φºAl3+ | Al = -1,68 B
φºMg2+ | Mg = -2,37 B
Следовательно, магний активнее алюминия и может вытеснить алюминий из его соли.
е) Al + 4HNO3 = Al(NO3)3 + NO + 2H2O
Al – 3e = Al3+ | 1
NO3- + 4H+ + 3e = NO + 2H2O | 1
Пример 8 Напишите уравнения реакций в молекулярных и ионо-молекулярных формах гидроксида натрия со следующими веществами:
P2O5, Al(OH)3, CuSO4, ZnO
Решение:
1) P2O5 + 6NaOH = 2Na3PO4 + 3H2O
P2O5 + 6OH- = 2PO43-+ 3H2O
2) Al(OH)3 + NaOH = Na[Al(OH)4]
амфотер. изб. тетрагидроксоалюминат
натрия
Al(OH)3+ OH- = [Al(OH)4]-
3) CuSO4 + 2NaOH = ↓Cu(OH)2 + Na2SO4
эквивалентные гидроксид
количества меди (II)
Cu2+ + 2OH- = Cu(OH)2
4) PbSO4 + 2NaOH = Na2PbO2 + H2SO4
изб. плюмбит
натрия
PbSO4 +2OH-= PbO22- + SO42-
5) ZnO + 2NaOH = Na2ZnO2 + H2O
амфотер. изб. цинкат
гидроксид натрия
ZnO + 2OH- = ZnO22- + H2O
Пример 9 Напишите реакции следующих превращений
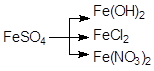
Решение:
1) FeSO4 + 2NaOH = ↓Fe(OH)2 + Na2SO4
2) FeSO4 + BaCl2 = FeCl2 + BaSO4↓
3) FeSO4 + Ba(NO3)2 = Fe(NO3)2 + BaSO4↓
Пример 10 Сколько литров раствора серной кислоты с массовой долей H2SO4 10% и плотностью 1,07 г/мл требуется для нейтрализации гидроксида натрия массой 16 кг?
Решение:
Запишем уравнение реакции нейтрализации:
H2SO4 + 2NaOH = Na2SO4 + 2H2O
Определяем массу H2SO4, необходимую для нейтрализации
2ּ 40 г NaOH – 98 г H2SO4
16000 г NaOH – х
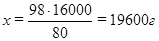
Находим массу 10% раствора H2SO4 по формуле;
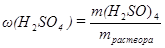 , следовательно
, следовательно
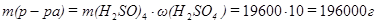
Находим объем раствора H2SO4, необходимый для нейтрализации NaOH
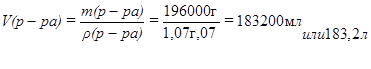
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
1. Глинка Н.Л., Общая химия.–М.: Интегралл-пресс, 2004.
2. Ерохин Ю.М., Фролов В.И. Сборник задач и упражнений по химии.–М.: Высшая школа, 2005.
3. Сыркин А.М., Зорина Л.Н. Классификация и номенклатура неорганических веществ. Учебное пособие, УГНТУ, 2006 г.
4. Курс общей химии /Под ред. Н.В.Коровина-М.:Высшая школа, 1999 г.
Задание №9
по теме "Химия воды. Жесткость воды"
Методика решения задач по теме "Жесткость воды и методы её умягчения" основана на понятии жесткости, знании единиц измерения жесткости, методов умягчения воды и некоторых общих формул.
Единой международной единицы измерения жесткости не существует. Различные страны условно принимают свои единицы. В нашей стране жесткость выражают в ммоль-эквивалентах (мэкв) ионов Са2+ и Mg2+ (либо соответствующих солей кальция и магния), содержащихся в 1л воды; 1 (мэкв) жесткости соответствует 20,04 мг Са2+ в I л воды или 12,16 мг Mg2+ в 1 л воды.
Если известны массы ионов или соответствующих им солей, то жесткость считается по формуле
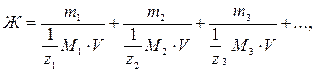
где m1, m2, m3 – массы ионов металлов (или их солей) в воде, мг;
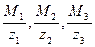 – эквивалентные массы ионов металлов (или их солей), мг/экв;
– эквивалентные массы ионов металлов (или их солей), мг/экв;
V – объём воды, л.
Различают карбонатную (или временную) жесткость (Жк) и некарбонатную (или постоянную) жесткость (Жнк). Некарбонатная жесткость представляет собой разность между общей жесткостью и карбонатной.
Жнк = Жобщ - Жк
Временную жесткость воды (Жк) можно определить по объёму кислоты, пошедшей на её титрование. В соответствии с законом эквивалентов количество эквивалентов всех участвующих в химической реакции веществ должно быть одинаково. Следовательно:
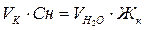 ,
,
где 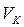 – объём кислоты, пошедшей на титрование, мл;
– объём кислоты, пошедшей на титрование, мл;
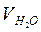 – объём пробы воды, взятой для титрования, мл;
– объём пробы воды, взятой для титрования, мл;
Сн – нормальная концентрация кислоты, экв./л;
Отсюда:
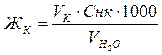 (мэкв/л).
(мэкв/л).
Аналогично можно рассчитать общую жесткость воды (Жобщ.) по объёму трилона Б, пошедшего на титрование:
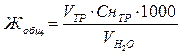 (мэкв/л).
(мэкв/л).
Эквивалент трилона Б равен 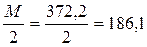 г
г
Для устранения жесткости на практике часто используется известково-содовый метод. Добавление к воде Ca(OH)2 устраняет карбонатную жесткость (ЖК), а добавление (Na2CO3) – некарбонатную жесткость (ЖНК).
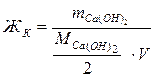 ;
; 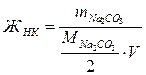 ;
;
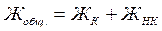 .
.
Иногда при умягчении воды известково-содовым методом дозы извести и соды, вводимые в воду, определяются пробным умягчением. Для ориентировочных расчетов можно использовать следующие формулы:
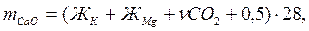
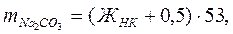
где 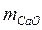 и
и 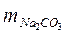 – содержание извести и соды, мг/л;
– содержание извести и соды, мг/л;
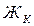 – карбонатная жесткость, мэкв/л;
– карбонатная жесткость, мэкв/л;
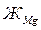 – магниевая жесткость, мэкв/л;
– магниевая жесткость, мэкв/л;
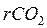 – содержание диоксида углерода, мэкв/л;
– содержание диоксида углерода, мэкв/л;
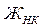 – некарбонатная жесткость, мэкв/л;
– некарбонатная жесткость, мэкв/л;
0,5 – избыток реактива, мэкв/л;
28 – масса мг-эквивалента оксида кальция, мг;
53 – масса мг-эквивалента соды, мг.
