Тема 3. Электрохимические методы анализа
Измерение электрических величин для определения состава веществ является одним из важнейших приёмов аналитической химии. Все электрохимические измерения проводятся с использованием электрохимической ячейки - раствора, в который погружены по меньшей мере два электрода. На электродах происходят различные физические и химические процессы. О степени протекания их можно судить путем измерения напряжения, силы тока, электрического сопротивления, электрического заряда или подвижности заряженных частиц в электрическом поле. Определяемое вещество при этом, как правило, находится в растворе электролита.
С методической точки зрения электрохимические методы можно разделить на прямые и косвенные. К косвенным относятся методы титрования, в которых конечную точку определяют электрохимическим способом.
Другой вид классификации электрохимических методов основан на том, протекает ли в ходе анализа через ячейку электрический ток или нет. В зависимости от этого различают следующие методы:
-потенциометрические;
-вольтамперометрические;
-амперометрические;
-вольтаметрические;
-импедансные, или кондуктометрические;
-электрогравиметрические;
-кулонометрические;
-другие, комбинированные, например, спектроэлектрохимические.
Потенциометрические методы - potentiometry, основаны на измерении напряжения на электродах ячейки в отсутствие тока. Как и любые другие электрохимические методы, они делятся на прямые (например, рН-метрия) и косвенные (потенциометрическое титрование). Если же через ячейку протекает электрический ток (происходит процесс электролиза), то для химического анализа можно использовать зависимость силы тока от напряжения. Соответствующие методы называются вольтамперометрическими - voltammetry, в частном случае, при использовании ртутного капающего электрода - полярографическими. Методы, основанные на измерении напряжения при постоянной силе тока, называются вольтаметрическими - voltmetry,, а на измерении силы тока при постоянном напряжении - амперометрическими - amperometry. В любом варианте вольтамперометрический анализ проводят в условиях, когда степень электрохимического превращения определяемого вещества вследствие электролиза мала. Однако электролиз можно проводить и до полного превращения определяемого вещества. На этом основаны методы электрогравиметрии и кулонометрии. В электрогравиметрии для определения содержания вещества применяют взвешивание продукта электролиза, а в кулонометрии - измерение количества электричества, затраченного на электролиз. Электрогравиметрические и прямые кулонометрические определения обычно проводят при постоянном потенциале рабочего электрода (в потенциостатическом режиме). Косвенный кулонометрический анализ (кулонометрическое титрование), как правило, ведут при постоянной силе тока (в гальваническом режиме). Здесь электролизу подвергают вспомогательный реагент, продукт электрохимического превращения которого служит титрантом для определяемого вещества.
3.1. Потенциометрия
Потенциометрия - один из самых простых электроаналитических методов. Прежде всего, он используется для измерений рН, а также для установления ионного состава растворов. Это также способ преобразования селективных взаимодействий в аналитический сигнал в молекулярных сенсорных устройствах или в процессе химической реакции.
Потенциометрия основана на измерении потенциала ячейки, т.е. разности потенциалов между двумя электродами (индикаторным электродом и электродом сравнения) в отсутствие тока во внешней цепи. Это позволяет получить информацию о химическом составе раствора. Потенциал и область применения индикаторного электрода зависят от его природы и селективности.
В потенциометрии используют два приема:
- измерение потенциала электрода как функции активности (концентрации) определяемого компонента -прямая потенциометрия;
- измерение потенциала электрода как функции объема реагента, добавленного к пробе - потенциометрическое титрование.
3.1.1. Электродный потенциал. Уравнение Нернста
При погружении металлического электрода в раствор, содержащий ионы этого же металла, между твёрдой и жидкой фазами устанавливается равновесие:
Ме0↔Меn+ + ne
Величина электродного потенциала, возникшая на границе Ме - раствор, называется равновесным потенциалом 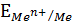 . Зависимость
. Зависимость 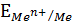 от концентрации ионов Н+ в растворе выражается уравнением Нернста:
от концентрации ионов Н+ в растворе выражается уравнением Нернста:
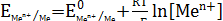 ,
,
где 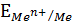 - потенциал металлического электрода при данной концентрации ионов металла [Меn+] в растворе;
- потенциал металлического электрода при данной концентрации ионов металла [Меn+] в растворе; 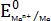 - стандартный(нормальный) электродный потенциал или потенциал этого же электрода в растворе с концентрацией ионов, равной 1 моль/л, или, другими словами, э.д.с. элемента, состоящего из данного и стандартного водородного электрода (потенциал водородного электрода равен 0 при всех температурах); [Меn+] - концентрация ионов металла в растворе, моль/л.
- стандартный(нормальный) электродный потенциал или потенциал этого же электрода в растворе с концентрацией ионов, равной 1 моль/л, или, другими словами, э.д.с. элемента, состоящего из данного и стандартного водородного электрода (потенциал водородного электрода равен 0 при всех температурах); [Меn+] - концентрация ионов металла в растворе, моль/л.
Нормальные потенциалы металлических электродов 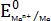 можно найти в справочной литературе. Для концентрированных растворов и растворов сильных электролитов концентрацию ионов металла[Меn+] в уравнении Нернста заменяют активностью ионов металла
можно найти в справочной литературе. Для концентрированных растворов и растворов сильных электролитов концентрацию ионов металла[Меn+] в уравнении Нернста заменяют активностью ионов металла 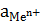 .
.
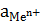 =f[Меn+]
=f[Меn+]
f - коэффициент активности иона (справочные данные).
Выделяют три основных класса потенциалов:
-электродные;
- редокс (окислительно-восстановительные) ;
- мембранные.
Методы прямой потенциометрии основаны на применении уравнения Нернста для нахождения активностей или концентрации участника электродной реакции по измеренной э.д.с. цепи или потенциалу соответствующего электрода.
При потенциометрическом титровании точку эквивалентности (т.э.) определяют по резкому изменению (скачку) потенциала вблизи т.э.
Изменение равновесного потенциала электрода в зависимости от концентрации (активности) ионов в растворе называется обратимостью электрода относительно данного катиона или аниона. В связи с этим рассматривают электроды первого и второго рода.
3.1.2. Электроды потенциометрического метода анализа
В потенциометрическом анализе из электродов составляется гальванический элемент, э.д.с. которого контролируется в ходе анализа. Гальванический элемент образуют два электрода:индикаторный электрод и электрод сравнения.
Индикаторный электрод - это электрод, который реагирует на изменение концентрации определяемого иона в растворе.
Индикаторные электроды можно классифицировать следующим образом:
а) Классические электроды
Класс 0. Инертные металлы (например, Pt, Au) в контакте с раствором окислительно- восстановительной пары, например, система Pt|Ce4+,Ce3+. Идеальные инертные материалы обратимо обмениваются электронами с компонентами электролита, при этом сами не окисляются.
Класс 1. Обратимые: металл/ион металла (активный металл в контакте с раствором собственного иона), например, Ag|Ag+ (электроды первого рода).
Класс 2. Обратимые: металл в равновесии с насыщенным раствором соли иона металла и избытком аниона Х-, например, Ag|AgX, Х- (электроды второго рода).
Класс 3. Обратимые: металл в равновесии с двумя малорастворимыми солями с общим анионом (или растворимым комплексом иона второго металла) и избытком второго катиона, например, Pb|оксалатPb|оксалат Са|Са2+ (электроды третьего рода).
б) Мембранные (ион-селективные) электроды.
Индикаторные электроды должны удовлетворять следующим требованиям:
-равновесный потенциал электрода должен быть воспроизводимым и устанавливаться быстро, иначе анализ потребует много времени;
- обратимость: потенциал должен изменяться с изменением концентрации иона;
- химическая устойчивость: не должен реагировать с другими компонентами, находящимися в растворе.
В качестве индикаторных электродов используют:
-водородный электрод;
- хингидронный электрод;
- ионоселективные мембранные электроды;
- стеклянный электрод;
- металлические электроды 1-го и 2-го рода (изготавливают из Ag, Hg, Cd).
Электроды сравнения
Электрод сравнения - изготовлен из фаз постоянного химического состава, характеризуется известным, постоянным (не зависящим от концентрации определяемого вещества) потенциалом.
Важными требованиями к электроду сравнения являются: обратимость, воспроизводимость и стабильность во времени.
Обратимость означает, что направление электродной реакции можно изменить, поменяв полярность электрода.
Воспроизводимость выражается стандартным отклонением потенциала ячейки при последовательных измерениях в растворе заданной концентрации.
Стабильность работы электрода оценивают по смещению отклика при измерениях в потоке и по величине стандартного отклонения для заданного раствора. Электроды сравнения, используемые в аналитической практике, являются вторичными эталонами и, как правило, электродами второго рода. Потенциалы электродов сравнения определены относительно стандартного водородного электрода (СВЭ, первичный электрод сравнения в электрохимии).
В потенциометрии используют следующие электроды сравнения.
а) Хлоридсеребряный электрод (Ag|AgCl, KCl)
Хлоридсеребряный электрод можно приготовить, например, покрыв анод из серебряной проволоки хлоридом серебра методом электролиза 0,1М раствора хлорида. Проволоку, покрытую хлоридом серебра, погружают в раствор KCl с известной концентрацией. Чаще всего это насыщенный раствор 3,8 М, иногда 1,0 М или 0,1 М (рис. 3, а). Потенциал хлоридсеребряного электрода возникает в результате полуреакции:
AgCl (тв.) + е-↔Ag + Cl-
Хлоридсеребряный электрод - самый воспроизводимый электрод сравнения с хорошей электрической и химической стабильностью при 25°С. Потенциал электрода зависит от всех компонентов раствора, влияющих на концентрацию ионов серебра. Поэтому его нельзя использовать без дополнительного солевого мостика в растворах, содержащих белки, бромид- или сульфид-ионы, которые образуют нерастворимые соединения с ионами серебра, а также в присутствии лигандов, взаимодействующих с AgCl, таких как CN-, SCN-, и сильных окислителей или восстановителей.
Температурный коэффициент хлоридсеребряного электрода очень мал. Благодаря этому он удобен в тех случаях, когда невозможно поддерживать температуру постоянной. Или при температурах выше 80°С.
б) Каломельный электрод(Hg|Hg2Cl2, KCl)
Каломельный электрод состоит из платиновой проволоки, погруженной в пасту из ртути и хлорида ртути (I) в стеклянной трубке. Внутренним раствором служит раствор хлорида калия известной концентрации, насыщенный хлоридом ртути (I) (рис. 3 в). Потенциал каломельного электрода определяется полуреакцией:
Hg2Cl2(тв) + 2е-↔ 2Hg+ 2Cl-.
Потенциал каломельного и хлоридсеребряного электрода зависит от концентрации ионов хлора и описывается уравнением:
Е = const + 0,059lg[Cl-].
Концентрация внутреннего раствора KClостаётся величиной постоянной, поэтому и потенциал электродов стабилен и однозначен.
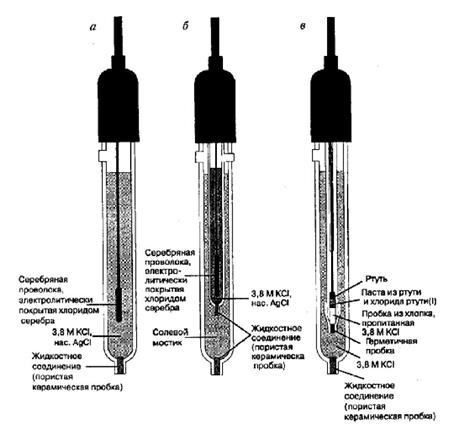
Рис.3. Электроды сравнения: а - хлоридсеребряный; б - хлоридсеребряный электрод с двойным жидкостным соединением; в - каломельный электрод.
3.1.3. Потенциометрическая ячейка
В потенциометрии раствор, содержащий определяемое вещество, активность (концентрацию) которого следует установить, и индикаторный электрод образуют полуэлемент, второй полуэлемент состоит из электрода сравнения (рис. 1).
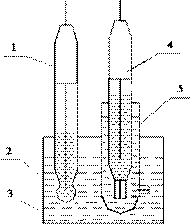
Рис. 4. Схема ячейки для потенциометрических измерений: 1 - индикаторный электрод; 2 – стакан; 3 – анализируемый раствор; 4 электрод сравнения; 5 –электролитический ключ.
Потенциал индикаторного электрода Еинд линейно зависит от логарифма активности (концентрации) определяемого иона. Электрод сравнения в растворе постоянного состава имеет фиксированный потенциал Еср, не зависящий от состава анализируемого раствора. Оба электрода идеально неполяризуемые.
Потенциал ячейки (э.д.с.) Е описывается следующим уравнением:
E= (ЕИНД - ЕСР) + Еj, (21)
где ЕИНД - потенциал индикаторного электрода; ЕСР - потенциал электрода сравнения; Ej - потенциал жидкостного соединения.
Т.о., э.д.с. ячейки определяется разностью потенциалов правого и левого электродов, а полуреакции на электродах определяют их окислительно-восстановительные потенциалы.
Например, в ячейкеAg|AgCl,KCl||Ce3+,Ce4+|Pt на левом электроде (электрод сравнения) протекает полуреакция
AgCl (тв.) + е-↔Ag + Cl-, E0 = 0,222В
на правом (индикаторном) электроде, т.е. на Pt - полуреакция
Ce4++ е-→Ce3+ , Е0 = 1,44В
Для потенциалов электродов можно записать уравнения:
ECР = 0,222 - 0,05916lg[Cl-]
EИНД= 1,44- 0,05916lg 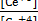
Потенциал (э.д.с.) ячейки при 25°С:
E = EИНД - ECР = 1,218 - 0,05916lg 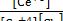
Поскольку концентрация хлорид-ионов в электроде сравнения постоянна, потенциал ячейки зависит от соотношения [Се3+]/[Се4+].
В правильно составленной потенциометрической ячейке Есрпостоянен, а Ej или постоянен или очень мал (им можно пренебречь).
3.1.4. Потенциал жидкостного соединения
Жидкостное соединение - это зона контакта двух растворов различного состава, образующаяся в месте соприкосновения электрода сравнения и анализируемого раствора. Эта неселективная граница раздела является источником потенциала жидкостного соединения (или диффузионного потенциала), Ej.
В потенциометрической ячейке электрод сравнения контактирует с раствором пробы через солевой мостик. Солевой мостик обеспечивает электрический контакт между двумя полуэлементами электрохимической ячейки. Смешивание двух неодинаковых фаз (различного состава) можно довести до минимума, если уменьшить зону соприкосновения фаз. Это обеспечивается при контакте через капилляр, диафрагму из спеченного стекла или пробку из агар-агара. Природа жидкостного соединения (анализируемый раствор|площадь контакта солевого мостика) влияет на воспроизводимость измерений потенциала ячейки. В ячейке с диафрагмой жидкостное соединение обозначается двойной чертой ||. Имеются электроды с двойным жидкостным соединением для высокоточных измерений потенциала (рис.3б, 5).
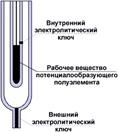
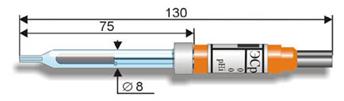
Рис. 5. Двухключевой электрод сравнения.
Двойное жидкостное соединение не только снижает диффузионный потенциал, но и позволяет избежать загрязнения раствора пробы внутренним раствором электрода сравнения. Электроды сравнения с двойным солевым мостиком очень удобны для точных измерений с ион-селективными электродами.
3.1.5. Ионоселективные электроды
Ионоселективные электроды (ИСЭ) - полуэлементы, состоящие из ионоселективной мембраны (селективной межфазной границы), внутреннего раствора и внутреннего электрода сравнения стандартной конструкции (рис. 6) или ионоселективной мембраны и твёрдофазного контакта (твёрдотельный электрод). Такой электрод позволяет селективно определять активности одних ионов в присутствии других. Обычно анализируемый раствор является водным.
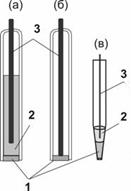
Рисунок 6. Конструкции ионоселективных электродов: (а) Мембранный электрод с внутренним жидкостным контактом; (б) мембранный электрод с твердым контактом; (в) микроэлектрод с жидкой мембраной; 1 - ионоселективная мембрана; 2 - внутренний стандартный раствор 3 - токосъемник (внутренний электрод сравнения).
Эти электроды отличаются от окислительно-восстановительных электродов (электродов нулевого, первого, второго и третьего рода): на ИСЭ не протекает никакой окислительно-восстановительной реакции. Зависимость потенциала ИСЭ от состава раствора обусловлена равновесиями ионного обмена, комплексообразования, распределения и равновесиями осадок-раствор. Часто в качестве внутреннего электрода сравнения ИСЭ содержат электрод второго рода.
Вторым полуэлементом в паре с ионоселективным электродом является внешний электрод сравнения. Контакт между ними осуществляется с помощью солевого мостика. Обычно используют электроды сравнения с двойным жидкостным соединением (рис.5). Схема электрохимической ячейки с ионоселективным индикаторным электродом выглядит следующим образом:
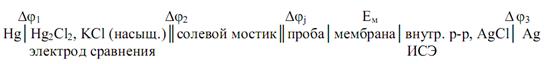
Важной характеристикой ИСЭ являетсяпотенциометрический коэффициент селективности(KПОТА,В), которыйпоказывает, во сколько раз электрод более чувствителен к данным ионам, чем к мешающим.
Например, коэффициент селективностиNa-электрода по отношению к K равен 103. Это значит, что электрод в 1000 раз более чувствителен к ионам Na+, чем K+. Коэффициенты селективности некоторых электродов приведены в справочниках.
Типы ионоселективных электродов.
В зависимости от природы мембраны различают следующие типы ионоселективных мембранных электродов:
Ø Первичные ионоселективные электроды:
· электроды со стеклянной мембраной;
· кристаллические (твердофазные) мембранные электроды;
· электроды с жидкой мембраной:
· жидкие ионообменные мембранные электроды;
· электроды с жидкой мембраной с нейтральными носителями.
Ø Сложные или многомембранныеионоселективные электроды:
· молекулярно-чувствительные устройства, такие, как газочувствительные или ферментные электроды.
Ø Ион-селективные полевые транзисторы ИСТП:
• Эти типы электродов - гибриды ион-селективных электродов и полевых транзисторов из оксидов металлов.
Конструкции различных ион-селективных электродов приведены на рис.7 .
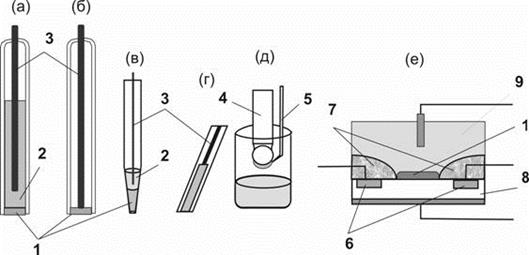
Рисунок 7. Конструкции ионоселективных электродов и полевых транзисторов. (а) Мембранный электрод с внутренним жидкостным контактом; (б) мембранный электрод с твердым контактом; (в) микроэлектрод с жидкой мембраной; (г) тонкопленочный электрод с полимерной мембраной; (д) электрод с газовым зазором; (е) ионоселективнй полевой транзистор. 1 - ионоселективная мембрана; 2 - внутренний стандартный раствор 3 - токосъемник (внутренний электрод сравнения); 4 - рН-метрический стеклянный электрод; 5 - солевой мостик к электроду сравнения; 6 - сток и исток;7 - изолирующий материал (диоксид кремния); 8 - кремниевое основание; 9 - электрод сравнения
Стеклянные электроды
Стеклянный электрод для измерения рН - первый ионоселективный электрод, известен с начала ХХ века. Его широко используют для измерения рН в лабораториях и в мониторинге.
Стеклянный электрод (рис.8) состоит из корпуса, в который налит буферный раствор. В этот раствор погружен внутренний электрод сравнения - чаще всего хлоридсеребряный. Нижняя шарообразная часть корпуса сделана из очень тонкого стекла и обычно называется стеклянной мембраной. Однако это не мембрана в обычном смысле этого слова, так как она непроницаема для компонентов раствора. При контакте с раствором приповерхностный слой стекла выступает в роли ионообменника, обменивая катионы, находящиеся в пустотах силикатного каркаса, на ионы Н+. Для того, чтобы мембрана электрода приобрела способность к такому обмену, её следует предварительно вымочить в кислом растворе.
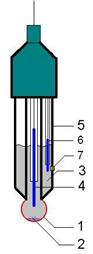
Рис. 8. Комбинированный стеклянный электрод: 1 – мембрана, 2 - буферный раствор насыщенный AgCl, 3–водный раствор KCl, 4 – внутренний электрод сравнения, 5 – стеклянный корпус электрода, 6 – внешний электрод сравнения, 7 – пористая пробка.
Комбинированный электрод состоит из стеклянного электрода и внешнего электрода сравнения (рис. 8 ). Электрод сравнения контактирует с раствором пробы с известным рН через жидкостное соединение.
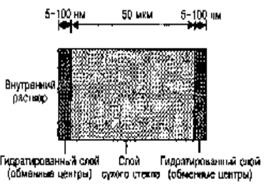
Рис.9. Стеклянная мембрана.
Для получения стабильных значений потенциала стеклянный электрод необходимо вымачивать в разбавленном буферном растворе. Поверхность стекла поглощает воду, образуется слой гидратированного геля. Одновременно образуются силанольные группы, и ионы натрия в слое гидратированного геля замещаются на ионы Н+.
Разность потенциалов между двумя электродами сравнения зависит от рН исследуемого раствора. Все остальные межфазные потенциалы постоянны из-за постоянства состава контактирующих фаз. Изменение рН раствора на единицу в идеальном случае вызывает изменение потенциала ячейки на 59,16 мВ при 25°С.
Равновесное значение потенциала стеклянного электрода зависит от активностей ионов Н+ в анализируемом растворе (а1) и внутреннем растворе электрода (а2). В первом приближении эта зависимость имеет вид:
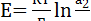 . (22)
. (22)
Поскольку активность ионов Н+ во внутреннем растворе (а2) постоянна, то
 . (23)
. (23)
Подставляя численные значения параметров и переходя от натуральных логарифмов к десятичным, при 25 °С имеем:
Е(250) = EConst - 59,16рН (мВ) (24)
Величина EConst зависит от значения рН внутреннего раствора, а также от потенциала асимметрии стеклянной мембраны. На практике угол наклона градуировочной зависимости может отличаться от значения 59,26 мВ. В этих случаях в уравнение вводят эмпирическую поправку k - коэффициент крутизны:
Е(250) = EConst - k·59,16рН (мВ)
Для нахождения постоянного члена уравненияEConst и коэффициента крутизны k измеряют значения рН стандартных буферных растворов с известными величинами рН и сравнивают измеренные значения с теоретическими. При наличии расхождений между ними прибор соответствующим образом подстраивают. Необходимо использовать по меньшей мере два стандартных раствора, покрывающих весь диапазон измеряемых значений рН. Часто градуировку проводят по нейтральному фосфатному буферу (рН = 6,86), а второй буфер выбирают в кислой или щелочной области, в зависимости от требуемого диапазона рН.
Стеклянные электроды позволяют с высокой точностью измерять значения рН от 1 до 10. На краях этого диапазона рН наклон градуировочной зависимости несколько ниже теоретического. При рН<1 возникает кислотная погрешность. Её величина зависит от сорта стекла, использованного для изготовления мембраны. При рН>10 электрод становится чувствительным к ионам щелочных металлов, вследствие чего возникает щелочная погрешность.
Существуют сорта стекла (в частности, на основе Li2O-BaO-La2O3-SiO2), для которых рабочий диапазон рН более широкий, как в кислой, так и в щелочной области. С другой стороны, чувствительность стеклянной мембраны к ионам натрия и калия можно использовать для создания специальных сортов стёкол и разработки на их основе электродов для определения этих ионов. Например, при замене Na2O на Li2O так называемую натриевую погрешность можно уменьшить. Мембранные электроды из такого стекла можно использовать для измерений рН до рН 13 даже при высокой концентрации ионов натрия.
Между измерениями электроды следует хранить в воде для сохранения гидратированного поверхностного слоя.
Кристаллические (твердофазные) электроды
Мембраны таких электродов состоят из ионных кристаллов или их смесей. Иногда они представляют собой монокристаллы, например, у фторидселективного электрода на основе LaF3. Чаще всего мембраны изготавливают из порошков, уплотнённых прессованием или плавлением. Материалом мембраны могут служить такие соли: AgCl, Ag2S, LaF3,Ag2S + CuS, Ag2S + PbS, Ag2S + CdS.
Электроды с кристаллическими мембранами на основе галогенидов серебра предназначены, главным образом, для определения анионов, но их можно использовать и для определения иона серебра.
Предел обнаружения ионоселективных электродов на основе галогенидов серебра зависит от природы материала мембраны и определяется минимальной активностью ионов серебраaAg+min, обусловленной процессами на границе раздела мембрана|раствор. Источниками поступления ионов серебра в раствор служат:
- сам материал мембраны (его растворимость определяется константой произведения растворимости галогенида серебра);
- соосажденные и адсорбированные на мембране ионы серебра.
Таким образом, электроды с мембранами из нерастворимых солей не являются инертными. Указанные реакции обусловливают предел обнаружения таких электродов порядка 10-5 - 10-6 М.
Фторидный электрод - один из самых важных электродов с кристаллической мембраной (рис.10). С его помощью можно легко и достаточно селективно определить фториды (100 -10-6М). Электродная мембрана его состоит измонокристаллической пластинки LaF3 с добавками Еu(II) для повышения электропроводности мембраны. Внутренний раствор содержит 0,1М NaF и 0,1М NaCl. В него погружен хлоридсеребряный электрод. Рабочий интервал рН фторидного электрода лежит в интервале рН 5,5 - 6,5, создаваемом ацетатным или цитратным буфером.
Рис.10. Фторидселективный электрод.
Электроды с жидкой мембраной
Жидкие мембраны представляют собой трех- или четырехкомпонентные мембраны с положительно или отрицательно заряженными или нейтральными подвижными носителями (переносчиками) ионов. Подвижные носители - соединения с центрами, способными связывать ионы, как правило, внедренные в пластифицированные поливинилхлоридные матрицы. С помощью таких электродов определяют ионы нитрата и кальция. Активным компонентом мембраны кальциевого ион-селективного электрода служит додецилфосфат кальция, растворенный в диоктилфенилфосфате. Электродная функция кальциевого электрода выполняется в интервале 10-1 - 10-6М, основные мешающие ионы: Н+, Zn2+, Fe2+ , Mg2+ .
На рис.11. представлены различные ионофоры.
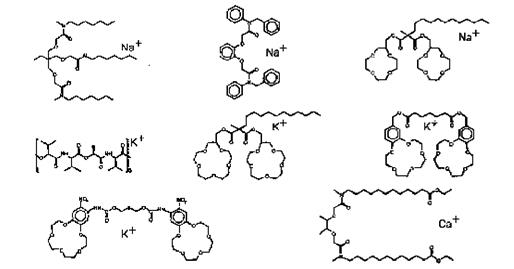
Рис.11. Химическая структура различных ионофоров, применяемых в электродах с жидкими мембранами.
Сложные (многослойные) ионоселективные электроды.
Чувствительные потенциометрические устройства состоят из основного чувствительного элемента (ионоселективного электрода) и модифицирующего мембранного слоя, который ведет себя как дополнительная селективная граница раздела. Природа модифицирующего слоя (химически активного или неактивного) повышает селективность сигнала. Чувствительность основного элемента увеличивается при определении различных неорганических газовых и органических молекул.
3.1.6. Прямая потенциометрия
В этом методе измеряют потенциал электрода (или э.д.с. гальванического элемента), погруженного в исследуемый раствор, и вычисляют концентрацию (активность) определяемых ионов по уравнению Нернста или с помощью калибровочной кривой.
а) измерение рН
Из-за невозможности измерения активности индивидуального иона, как и потенциала изолированного электрода, значение рН на основании концентрации или активности ионов водорода экспериментально определить нельзя. Измеряемые значения рН являются фактически «рабочими» - величинами, определяемыми на основании значений рН, постулированных для стандартных растворов.
Рабочая шкала рН основана на использовании общепринятых значений рН ряда стандартных растворов известного состава, измеренных в потенциометрической ячейке без жидкостного соединения, называемой ячейкой Гарнеда:
Pt | H2 (1 атм) H+ (aH+ = 1), Cl- | AgCl | Ag
Определение понятия «рабочее значение рН» принято Национальным институтом стандартов и технологии США, аналогичными организациями в ряде других стран и ИЮПАК.
В большинстве случаев градуирование стеклянного электрода проводят по двум точкам. Признание понятия «рабочего» рН означает, что электрохимическиизмеренный рН не вполне равен значению, определяемому активностью или концентрацией иона водорода, а скорее является результатом применения общепринятой процедуры.
б) определение активности (концентрации) иона (рА)
• с использованием градуировочного графика
Методом прямой потенциометрии концентрацию или активность иона при наличии ионоселективного электрода можно найти по градуировочному графику.
Зависимость потенциала ионоселективного электрода от активности иона может отклоняться от нернстовской. Её можно приближённо описать уравнением:
E = const±SlgaA (25)
где E-потенциал электрода; const - постоянная, зависящая от природы мембраны; S - угловой коэффициент электродной функции, теоретически равный 59,16 мВ/рА для однозарядного иона (положительная для катионов, отрицательная величина для анионов), аА - активность исследуемого иона А.
Указанная зависимость позволяет в достаточно широком диапазоне активности получить линейный градуировочный график.
Для построения калибровочного графика используют серию стандартных растворов с известной концентрацией определяемых ионов.
Стандартные растворы готовят последовательным разбавлением исходного раствора (например, 0,1 М), приготовленного по точной навеске соли определяемого иона. Измеряют электродный потенциал при погружении электрода в эти растворы и строят график зависимости в системе координат Е(мВ) – lnC ионов. Затем измеряют потенциал исследуемого раствора и по графику определяют его концентрацию.
• методом добавок
Метод добавок применяют для нахождения концентрации определяемого вещества в пробах со сложной или неизвестной основой.
Метод основан на измерении изменения потенциала электрода при добавлении известного объема стандартного раствора к известному объему пробы. Объем стандартного раствора должен быть малым во избежание изменения ионной силы, концентрации определяемого иона и потенциала жидкостного соединения.
Рекомендуется добавлять определяемый ион в количестве примерно 100% от исходного. Методом множественных добавок можно не только найти концентрацию определяемого иона, но и оценить величину S для отклика электрода.
3.1.7. Потенциометрическое титрование
Сущность метода заключается в том, что в исследуемый раствор погружают гальванический элемент, состоящий из электрода сравнения и индикаторного электрода, и титруют раствор, определяя э.д.с. гальванического элемента в ходе титрования. По полученным данным строят кривую титрования.
Кривая титрования - это зависимость э.д.с. гальванического элемента от объема рабочего раствора.
Концентрация определяемых ионов изменяется в зависимости от объема прибавленного раствора неравномерно: сначала это изменение невелико, затем становится заметным и, наконец, в точке эквивалентности достигает наибольшего значения. По кривой титрования, построенной в системе координат Е(мВ) - Vтитранта(мл) или рН - 'Vтитранта(мл) и называемойинтегральной потенциометрической кривой,можно установить точкуэквивалентности как точку перегиба кривой. Вертикальный участок довольно четко указывает на точку эквивалентности. Однако часто таким методом точку эквивалентности определить сложно, например, при малом угле наклона графика. В таком случае используютдифференциальную потенциометрическую кривуюили кривую, построенную по методу Грана.
Дифференциальную потенциометрическую кривую (первая производная исходной кривой) строят в координатахDЕ/DVтитранта - Vтитранта, где DЕ - изменение потенциала электрода между двумя порциями добавленного титранта; DVтитранта - порция добавленного титранта. Точка эквивалентности в этом случае определяется максимумом на кривой титрования.
По методу Грана кривую титрования строят в координатах DVтитранта/DЕ-Vтитранта. Точка эквивалентности определяется как минимум кривой титрования.
Часто точку эквивалентности находят по второй производной исходной кривойтитрования и строят график в координатах: DЕ2 / DV2титранта-Vтитранта.
Различные виды кривых потенциометрического титрования представлены на рис. 12.
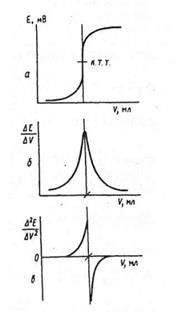
Рис.12. Нахождение точки эквивалентности по исходной кривой потенциометрического титрования(а), её первой (б) и второй (в) производной.
Потенциометрическую индикацию можно использовать не только в осадительном, но и в кислотно-основном (стеклянный электрод для измерения рН), комплексонометрическом (металл-селективные электроды - например, Си2+-селективный) и окислительно- восстановительном (металлические, в частности - инертные) электроды. Используемый для индикации электрод должен быть чувствительным либо к определяемому иону. Либо к иону-титранту.
