Электрохимический потенциал
Количественной характеристикой электрохимической системы является напряжение - разность потенциалов правильно разомкнутой цепи, которая является суммарным эффектом возникновения скачков потенциала на каждой из гетерогенных границ раздела.
Рассмотрим чем же обусловлено появление скачка потенциала на границе раздела фаз.
В электростатике потенциалом в данной точке электрического поля называется работа, которую необходимо совершить для переноса единичного «воображаемого» заряда из бесконечности в вакууме в данную точку фазы.
Термин «воображаемый» предполагает, то переносимый заряд химически не взаимодействует с фазой и что работа переноса связана лишь с электростатическим взаимодействием. Значение этой работы определяет внутренний потенциал – Ф.
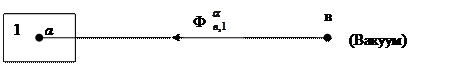 |
Рис. 4.4.1
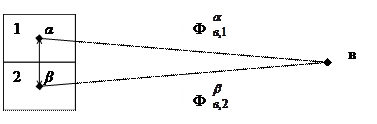 Очевидно, что при переносе заряда не из вакуума в фазу, а из одной фазы в другую, необходимо так же затрагивать работу – переноса и она может быть определена как разность соответствующих внутренних потенциалов фаз относительно вакуума.
Очевидно, что при переносе заряда не из вакуума в фазу, а из одной фазы в другую, необходимо так же затрагивать работу – переноса и она может быть определена как разность соответствующих внутренних потенциалов фаз относительно вакуума.
Рис. 4.4.2
В связи с тем, что работа переноса заряда в электрическом поле не зависит от пути переноса следует:
φ1,2 = Ф 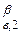 - Ф
- Ф 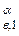 (4.4.1)
(4.4.1)
Разность внутренних потенциалов называется гальвани - потенциалом и обозначается φ (фи).
В реальных процессах участвуют не воображаемые заряды, а реальные (электроны, ионы). При переносе таких частиц из вакуума в данную фазу также необходимо затратить работу. Однако в этом случае возникают силы электростатического взаимодействия и силы химического взаимодействия реальной частицы с фазой, которые в принципе, являются электростатическими, но не ограничиваются лишь кулоновским взаимодействием. Таким образом, перенос из вакуума в фазу реальной частицы связан с затратой как электрической так и химической работы переноса.
Эту работу обычно относят к переносу не одной реальной частицы, а одного моля частиц и называют электрическим потенциалом фазы
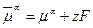 Ф
Ф 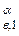 (4.4.2)
(4.4.2)
В этом уравнении химическая работа связана с химическим потенциалом 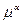 , а электрическая с внутренним Ф
, а электрическая с внутренним Ф 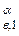 . Электрохимический потенциал измеряется в джоулях и характеризует энергетическое состояние заряженных частиц в фазе.
. Электрохимический потенциал измеряется в джоулях и характеризует энергетическое состояние заряженных частиц в фазе.
При переносе одного моля реальных частиц из фазы в фазу работу переноса можно охарактеризовать разностью электрохимических потенциалов:
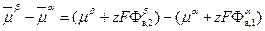 =
= 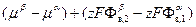 =
= 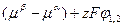
Процесс переноса частиц продолжается до тех пор, пока в системе не наступит электрохимическое равновесие, при котором 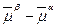 , а их разность будет равна нулю
, а их разность будет равна нулю 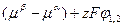 = 0
= 0
Тогда можно записать
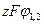 = -
= - 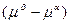 =
= 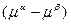
Из полученного выражения
φ1,2 = 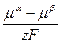 (4.4.3)
(4.4.3)
Таким образом, электрическую разность потенциалов между двумя точками расположенными на границах раздела фаз определяют Гальвани – потенциалы. Но из полученного выражения видно, что теоретически рассчитать Гальвани – потенциал нельзя, так как он при равновесии электрической системы определяется разностью химических потенциалов, которую для разных фаз определить нельзя, так как нельзя определить и рассчитать абсолютное значение химического потенциала.
Измерить Гальвани – потенциал так же нельзя, так как нельзя измерить разность потенциалов в точках, расположенных в различных фазах.
