Тема: Теплові ефекти хімічних реакцій. Направленість процесів
Актуальність теми:Хімічна термодинамікавивчає перетворення різних видів енергії при хімічних реакціях, процесах розчинення, випаровування, кристалізації та ін. Знання законів хімічної термодинаміки дає змогу передбачити можливість протікання даної реакції при певних умовах, знайти ступінь перетворення, вихід кінцевого продукту, тепловий ефект та ін. Закони термодинаміки стосуються і тих процесів, що протікають у живих організмах. Вони дають змогу глибше зрозуміти і пояснити ці процеси, оцінити можливість їх протікання.
Навчальні цілі:
Знати: основні поняття термодинаміки, види енергії, закони термодинаміки, взаємозв’язок і перетворення видів енергії.
Вміти:.визначати ентальпію процесів розчинення солей, утворення кристалогідратів і нейтралізації між кислотними і основними компонентами, розрахувати значення ентальпії, ентропії та енергії Гіббса за довідниками даними і пронозувати можливість чи неможливість самовільного протікання реакцій.
Самостійна позааудиторна робота студентів.
1.Хімічна термодинаміка як теоретична основа біоенергетики.
2.Основні поняття термодинаміки: системи, параметри стану і функції стану системи.
3.Внутрішня енергія і ентальпія.
4.Перший закон термодинаміки.
5.Закон Гесса і термохімічні рівняння.
6.Стандартні теплоти утворення хімічних сполук.
7.Термохімічні розрахунки і їх використання для енергетичної характеристики біохімічних процесів.
8.Другий закон термодинаміки.
9.Ентропія – міра впорядкованості енергії.
10. Рівняння Гіббса і його значення.
11. Критерії і напрям самовільних хімічних процесів.
12. Стандартні термодинамічні величини деяких продуктів харчування і кінцевих продуктів метаболізму.
13. Підготувати вихідні дані для оформлення протоколу лабораторної роботи.
Контрольні питання.
1. Дайте визначення поняттю система, фаза, компонент, ізобарний процес, ізохорний процес, ентальпія, енергія Гіббса,тепловий ефект реакції.
2. Перший та другий закони термодинаміки.
3. Закон Гесса, наслідок із закону Гесса.
4. Обчислити теплоту розчинення хлориду натрію, якщо при розчиненні у воді 12,69 г хлориду натрію поглинається 1,07 кДж теплоти.
5. Розрахуйте теплоту утворення кристалогідрату Na2SO3*7H2O, якщо теплоти розчинення DН (Na2SO3)= 11 кДж/моль, DН (Na2SO3*7H2O)=47 кДж/моль.
6. Обчисліть DН для реакцій:
2Н2 + О2 = 2Н2О
4NH3 + 3O2 =2N2 + 6H2O
2СО + О2 = 2СО2
С +О2 =СО2
СО2 + С = 2СО
3СаСО3 + 2Н3РО4 = Са3(РО4)2 + 3CO2 + 3H2O
7. Зробіть висновок про можливість самовільного протікання цих процесів на основі розрахунку 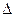 G реакції.
G реакції.
Самостійна робота на занятті.
Виконати лабораторні роботи:
1. Визначення зміни температури при розчиненні і взаємодії між речовинами.
2. Розрахувати ентальпію і енергію Гіббса для досліджуваних процесів.
3. Оформити і захистити протокол.
Методика виконання роботи
Робота 1. Визначення ентальпії розчинення солі.
У зважений калориметр наливають 100 мл води і вимірюють температуру з точністю до 0,1 градуса. Розчиняють у цій воді 5 г. солі на протязі 3-х хв. і вимірюють температуру розчину. Використовуючи числові дані, які заносять в табл. 1, і значення молярних теплоємностей (Ср) речовин із “Довідника з хімії”, які приймали участь в теплообміні, визначають теплоту розчинення солі (DН) за формулою:
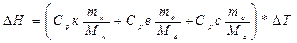 (1)
(1)
де Срк, Срв, Срс – молярні теплоємності алюмінію з якого зроблений калориметр, води і дослідженої солі;
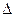 Т – зміна температури;
Т – зміна температури;
mк, mв, mс – маси калориметра, води і досліджуваної солі;
Мк, Мв, Мс - молярні маси речовини з якої виготовлений калориметр, води і досліджуваної солі;
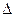 Н – зміна ентальпії при розчинені солі (теплота розчинення).
Н – зміна ентальпії при розчинені солі (теплота розчинення).
Табл. 1
| mАІ | Ср (АІ) | mв | Ср(в) | mс | Ср(с) | tпоч. | tкін. | 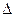 t t | 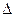 Н Н |
Робота 2. Визначення ентальпії утворення кристалогідрату з безводної солі і води.
Процес утворення розчинів соди із безводної солі і кристалогідрату можна відобразити рівняннями:
A(к.) + aq = A(р.) 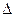 Н1
Н1
A*nH2O(к.) + aq = A(р.) 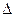 Н2
Н2
