Особенности горения взрывчатых веществ
Взрывчатыми называются индивидуальные вещества или их смеси, способные под влиянием какого-либо внешнего воздействия (нагревания, удара, трения, взрыва другого взрывчатого вещества) к быстрому самораспространяющемуся химическому превращению с выделением большого количества тепла и образованием газов. От обычных горючих веществ, горение которых происходит при взаимодействии с кислородом или другими внешними окислителями, взрывчатые вещества, находясь в конденсированной (твердой или жидкой) фазе, содержат в себе все компоненты, участвующие в горении. Взрывчатыми веществами могут быть как индивидуальные химические соединения, так и механические смеси.
Детонация взрывчатых веществ может инициироваться интенсивным механическим или тепловым воздействием (удар, искровой разряд, взрыв металлической проволочки под действием электрического тока и т.п.). Сила воздействия, необходимая для возбуждения детонации, зависит от химической природы взрывчатого вещества или состояния горючей газовой смеси. К механическому воздействию чувствительны так называемые инициирующие взрывчатые вещества (гремучая ртуть, азид свинца и др.), которые обычно входят в состав капсюлейдетонаторов, используемых для возбуждения детонации вторичных (менее чувствительных) взрывчатых веществ. В конденсированном взрывчатом веществе детонация распространяется с постоянной скоростью, которая среди возможных для этого вещества скоростей распространения детонационной волны является минимальной. При этом зона химического превращения перемещается относительно исходного вещества со сверхзвуковой скоростью. Вследствие этого волны разрежения, возникающие при расширении газообразных продуктов химической реакции, не могут проникнуть в зону реакции и ослабить распространяющуюся впереди ударную волну.
Большинство индивидуальных взрывчатых веществ относятся к нитросоединениям:
● тринитротолуол, тетрил, гексоген, октоген, нитроглицерин, нитраты целлюлозы и др.
Взрывчатыми свойствами обладают также:
● хлораты, перхлораты, азиды, органические перекиси.
Молекулы органических нитросоединений содержат слабо связанный кислород в виде нитрогруппы − О2. Таким образом, в одной молекуле содержатся и горючее, и окислитель. Их горение за счёт внутримолекулярного окисления может начаться при незначительных внешних воздействиях. Значительную группу взрывчатых веществ составляют эндотермические соединения, молекулы которых не содержат кислорода. В этом случае источником энергии является не окисление, а прямой распад. К таким соединениям относятся азиды свинца, серебра и других металлов. К механическим смесям относятся смеси твёрдых углесодержащих горючих с твердыми окислителями. Примером подобной смеси является чёрный порох.
Горение жидкостей
Для понимания механизма горения жидкостей необходимо иметь в виду, что их температура самовоспламенения (табл. 1.2) всегда значительно выше температуры кипения, поэтому горение жидкостей всегда происходит в паровой фазе.
Таблица 1.2
Сопоставление температур кипения и самовоспламенения
горючих жидкостей
| Жидкость | Температура, ºС | |
| самовоспламенения | кипения | |
| Ацетон | 56,5 | |
| Бензол | 80,1 | |
| Диэтиловый эфир | 34,5 | |
| Этиловый спирт | 78,4 | |
| Уксусная кислота | 118,1 | |
| Этилацетат | 77,1 | |
| Хлорбензол | 132,0 | |
| Диэтиломин | 55,2 |
Над поверхностью жидкости постоянно присутствует паровоздушная смесь, состоящая из паров жидкости и молекул воздуха. Концентрация паров характеризуется давлением насыщенных паров, которое существенно зависит от температуры жидкости. Эта зависимость описывается уравнением Клайперона-Клаузиуса:
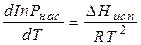 , (1.6)
, (1.6)
где 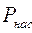 − давление насыщенных паров жидкости при температуре Т;
− давление насыщенных паров жидкости при температуре Т;
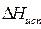 − теплота испарения.
− теплота испарения.
Из уравнения (1.6) следует, что давление насыщенных паров (и соответственно их концентрация) с увеличением температуры жидкости возрастают экспоненциально. Поэтому при некоторой температуре над поверхностью жидкости создается концентрация паров, равная нижнему концентрационному пределу распространения пламени. При зажигании этих паров внешним источником возникает вспышка – сгорание образовавшейся паровоздушной смеси с выделением значительного количества тепла.
Часть этого тепла расходуется на дополнительное испарение горючей жидкости, и, таким образом, горение поддерживается непрерывным процессом испарения горючего с поверхности за счёт тепла, подводимого от пламени. Поскольку пламя имеет значительно более высокую температуру, чем начальная температура среды, после начальной вспышки скорость испарения увеличивается, и возникшее пламя само поддерживается.
В установившемся состоянии горение паровоздушной смеси характеризуется двумя взаимосвязанными процессами: испарением горючей жидкости за счет тепла, выделяемого в зоне пламени, и сгоранием поступающих в зону горения паров.
В установившемся режиме скорости этих процессов должны быть равны. В практически важных случаях сгорание образующихся паров происходит практически мгновенно, сразу после их поступления в зону горения и смешивания с окружающим воздухом. Поэтому скорость выгорания определяется скоростью испарения как наиболее медленным процессом.
Таким образом, горение жидкости есть химический процесс сгорания ее паров, регулируемый скоростью испарения жидкости, зависящий от количества и условий подводимого к жидкости тепла, т.е. от условий теплообмена между пламенем и поверхностью жидкости.
Механизм горения жидкости проиллюстрируем примером горения со свободной поверхности, например, в резервуаре. При достаточной концентрации паров и их зажигании над поверхностью жидкости возникает пламя, а уровень жидкости начинает опускаться. Достаточно быстро после возникновения горения устанавливается стационарный режим, характеризующийся постоянной скоростью выгорания. Схематически горение жидкости со свободной поверхности показано на рисунке 1.3. Сгорание в факеле пламени происходит за счет диффузионного смешения паров горючей жидкости и воздуха. Поверхность жидкости нагревается до температуры кипения. В процессе выгорания происходит прогрев жидкости в глубину.

Рис. 1.3. Схема диффузионного горения жидкости:
1 – зона горения; 2 – зона догорания; 3 – пары жидкости;
4 – конвективные точки воздуха; 5 – зона подогрева жидкости;
6 – жидкость в резервуаре
Подвод тепла к жидкости в процессе диффузионного горения осуществляется главным образом теплопередачей излучением от факела пламени. Скорость выгорания определяется величиной теплоты испарения жидкости и количеством тепла, подведенного к поверхности жидкости от факела пламени. Значения скоростей выгорания некоторых жидкостей приведены в таблице 1.3.
Таблица 1.3
Скорость выгорания жидкостей
| Жидкость | Плотность | Скорость выгорания | ||||
| Линейная, мм/ мин. | Массовая, кг/м2 час | |||||
| Бензол | 0,875 | 3,150 | 165,37 | |||
| Толуол | 0,860 | 2,680 | 138,29 | |||
| Ксилол | 0,855 | 2,040 | 104,65 | |||
| Скипидар | 0,860 | 2,410 | 123,84 | |||
| Ацетон | 0,790 | 1,400 | 66,36 | |||
| Метиловый спирт | 0,800 | 1.200 | 57,60 | |||
| Диэтиловый эфир | 0,715 | 2,930 | 125,84 | |||
| Амиловый спирт | 0,810 | 1,297 | 63,034 | |||
| Изоамиловый спирт | 0,805 | 1,390 | 66,80 | |||
| Бутиловый спирт | 0,812 | 1,069 | 52,08 | |||
| Изобутиловый спирт | 0,800 | 1,122 | 53,856 | |||
| Сероуглерод | 1,270 | 1,745 | 132,97 | |||
| Диметилланилин | 0,950 | 1,523 | 86,31 | |||
Форма и размеры диффузионного пламени жидкостей существенно зависят от диаметра горелки или резервуара, в которых происходит горение. Пламя в горелках диаметром 10−15 мм имеет резко очерченную коническую форму, которая практически не меняется в течение всего процесса горения. Увеличение диаметра горелки приводит к появлению пульсаций в пламени, дроблению его на отдельные фрагменты, колебанию высоты. При диаметрах резервуаров более 15 см процесс диффузионного горения приобретает турбулентный характер. Эксперименты и наблюдения процессов горения при реальных пожарах показывают, что высота диффузионного пламени повышается с увеличением диаметра резервуаров. Структура и форма пламени жидкостей при горении в резервуарах различного диаметра свидетельствуют о переходе ламинарного режима горения при малых диаметрах к турбулентному – при больших. Зона пламени представляет собой очень тонкий слой, в котором происходит окисление горючего. В зоне пламени сгорает стехиометрическая смесь горючего и окислителя. В направлении к границам зоны пламени концентрации реагирующих компонентов убывают.
