Работа 1. Фотоколориметрические определение железа
В белых винах
Метод определения Fe3+ с помощью роданида калия основан на образовании комплекса, имеющего кроваво-красную окраску.
Реакцию проводят в присутствии HNO3(d=1.2) и 30%-ного раствора H2O2: Fe3+ + n(SCN-)→Fe(SCN)n
Приборы: фотоэлектроколориметр с кюветами толщиной 10 мм
Посуда, реактивы:
1. Мерные колбы на 100см3- 6шт.
2. Пипетки градуированные на 10см3-2 шт.
3. Раствор роданида калия KSCN, 5%-ный
4. Раствор железо-аммонийных квасцов
FeNH4(SO4)2, 12H2O с содержанием 20 мкг в 1 см3- раствор №1 (0,8636 г. химически чистых железоаммонийных квасцов растворяют в мерной колбе на 1000 см3 дистиллированнной водой, куда прибавлено 4см3H2SO4.d=1,54 тщательно перемешивают. Полученный раствор содержит 0,1 мг/см3 Fe3+. Далее в мерную колбу на 250 см3 отмеряют пипеткой 50см3 приготовленного раствора, доводят дистиллированной водой до метки и тщательно перемешивают).
Построение градуированной кривой
Для построения градуировочного графика в четыре мерные колбы на 100см3 вносят 5, 10, 15, 20 см3 раствора №1, что соответствует содержанию железа 100, 200, 300, 400 мкг в 100 см3. Прибавляют в каждую колбу по 2 см3 HNO3, по 6 капель 30% Н2О2, по 40 см3 5%-ного раствора KSCN и доводят дистиллированной водой до метки. Спустя 30 минут по завершении химических реакций измеряют абсорбционность каждого из растворов на приборе с зеленым светофильтром в кюветах с толщиной слоя 10 мм. В одну кювету наливают раствор фона, а в другую кювету- раствор с содержанием железа 100 мкг и измеряют абсорбционность (оптич. плотность).
Каждое определение следует повторить 3 раза. Далее, меняя раствор во второй кювете, находят абсорбционность для растворов с содержанием железа 200, 300,. 400 мкг.
Результаты определения заносят в таблицу 4.
Таблица 4.
| Взято стандартного раствора см3 | СодержаниеFe3+ в стандартном растворе | D |
На основании полученных данных строят градуировочную кривую. На оси абсцисс откладывают содержание железа в мкг, а на оси ординат-D.
Анализ вина
Для определения содержания железа готовят раствор вина. В мерную колбу на 100см3 берут 20см3 вина, 2 см3 HNO3, 6 капель 30% H2O2, 40 см3 40% раствора KSCN и доводят содержимое колбы до метки дистиллированной водой. Затем измеряют D- абсорбционность исследуемого вина и по градуировочной кривой определяют содержимое железо в растворе («а» мкг).
Содержание железа в 1дм3 вина определяют по формуле:
Fе (мкг/дм3) = 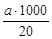 = а . 50мкг/см3 =
= а . 50мкг/см3 = 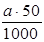 мг/дм3
мг/дм3
Поляриметрия
Цель работы: овладеть методом поляриметрического анализа для качественного и количественного определения оптически активных веществ в потребительских товарах.
Необходимые реактивы, лабораторная посуда: стеклянные палочки, мерные стаканы (100 мл), колбы мерные (100 мл), колбы конические (100 мл), сульфат цинка (0,5 Н), NaOH (1Н), дистиллированная вода, набор углеводов.
Приборы: сахариметр СУ-3, водяная баня, весы технические, электрическая плитка.
Поляриметрией называют метод, основанный на определении оптического вращения. Оптическое вращение – вращение плоскости поляризации света раствором оптически активного вещества. Оптическому вращению подвергается поляризованный свет. Поляризованный свет отличается тем, что колебания световых волн в нем происходят только в одной плоскости, а в неполяризованном – во всех плоскостях. Плоскость, в которой происходят колебания волн поляризованного света, называют плоскостью поляризации. Отклонение плоскости поляризации в угловых градусах называют углом вращения плоскости поляризации. Угол вращения зависит от природы вещества, его концентрации, толщины слоя, длины волны, температуры. При измерении угла вращения одного и того же вещества в специальных кюветах при постоянной температуре его значение зависит только от концентрации.
Способность вещества вращать плоскость поляризации характеризуют удельным вращением – вращением плоскости поляризации в правую или левую сторону, происходящим при прохождении поляризованного света через слой раствора в 1 дм., имеющего концентрацию 1 г/см3 (кг/дм3). Удельное вращение обозначают [αД20], индекс Д указывает на используемую при измерениях длину волны света линии Д в спектре натриевой лампы, а индекс 20 обозначает температуру раствора, обычно равную 200С и обозначают [α]Д20.
Правое удельное вращение обозначают знаком «+», левое – знаком
«-».
Удельное вращение определяют по формуле:
Для жидкости: [α]Д20 = α/ ι*ρ
Для растворов: [α]Д20 = α*100/ с* ι,
где α – угол вращения, град.;
ι – толщина слоя жидкости, дм;
с – концентрация р-ра, %;
ρ – плотность жидкости, кг/дм3.
Измерение угла вращения проводят на специальных приборах – поляриметрах. Удельное вращение является константой, используемой для идентификации веществ.
Таблица 5
Значения удельного вращения [α]Д20 некоторых веществ в воде
| Вещество | [α]Д20 | Вещество | [α]Д20 |
| Глюкоза | +53,1 | Молочный сахар | +53,5 |
| Сахароза | +66,4 | Миндальная кислота | +156,0 |
| Фруктоза | -93,0 | Никотин | -164,0 |
| Аскораиновая кислота | +23,0 |
Расчет концентрации оптически активных веществ в растворе, если известно, его удельное вращение, производят по формуле:
С = а· 100/[а]Д20 ·1,
где: а – угол вращения, град.;
1- толщина слоя жидкости, дм; С- концентрация р-ра, %;
[а]Д20- удельное вращение, град.
Поляриметрию применяют для определения концентрации оптически
активных веществ, их идентификации и обнаружения фальсификации продовольственных товаров.
Порядок работы на поляриметре
1.Установка нуль-пункта.
Закрыть крышку кюветного отделения без установки в нем кюветы.
Уровнять яркость сравнения вращением рукоятки клинового компенсатора.
Если нулевое деление нониуса не совмещается с нулевым делением шкалы, обратится к преподавателю.
Повторить уравнение яркостей полей сравнения, при этом нулевое деление нониуса должно совместиться с нулевым делением шкалы порядка шести раз.
2.Установка кювет.
При установке кювет следует:
- поместить кювету с раствором в кюветное отделение;
- установить кювету, вращая ее вокруг оси, в такое положение, чтобы линия раздела полей сравнения делила поля сравнения на две равные части.
3.Проведение измерения.
Уравнять яркость полей сравнения вращением рукоятки клинового компенсатора.
Произвести отсчет показателей по шкале и нониусу.
Повторить уравнение яркостей полей сравнения и отсчет по шкале и нониусу не менее шести раз.
.
Работа 1. Определение массовой доли сахарозы в кондитерских изделиях
1. 6,5 г исследуемого образца (шоколада, конфет, глазури и т.д.) поместить в мерную колбу на 100 мл.
2. Добавить к навеске образца 50 мл дистиллированной воды (60-700С).
3. Колбу поместить на водяную баню на 15 минут.
4. После этого в колбу добавить 20 мл гидроксида натрия и 20 мл сульфата цинка.
5. Колбу с содержимым охладить до 200С.
6. Довести до метки дистиллированной водой и профильтровать.
7. Полученный фильтрат (прозрачный, без осадка) помещают в кювету (2 дм) для сахариметра.
8. Кювету помещают в кюветный отсек сахариметра и определяют по шкале угол вращения плоскости поляризации.
9. Рассчитывают массовую долю сахарозы в образце по формуле:
С = 4· α · К,
где α – угол вращения плоскости поляризации, град.;
К – поправочный коэффициент (для натурального шоколада К=0,99);
4 – поправка на нормальную навеску сахарозы
Потенциометрия
Работа 1. Определение рН вина, сока (активной кислотности)
Определение кислотности вин и соков потенциометрическим методом имеет важное значение для пищевой технологии.
По величинам общей (титруемой) и активной кислотности на всех этапах производства можно судить о качестве сырья и продукции, режиме ее хранения.
Все кислоты в водных растворах распадаются (диссоциируют) на ионы водорода и кислотного остатка. Так сильные кислоты (Н2SO4, HCl) диссоциируют почти полностью с высокой степенью диссоциации, а слабые (винная, лимонная, яблочная, уксусная и др.) в очень малой степени, чаще выражаемой константой диссоциации.
Для сильных кислот в водных растворах диссоциация практически необратима:
 HCl H+ + Cl-
HCl H+ + Cl-
α (степень диссоциации) = число распавшихся молекул ×100
 общее число молекул (в %)
общее число молекул (в %)
Для слабых кислот диссоциация обратима (равновесие):

 СН3СООН Н+ + СН3СОО –
СН3СООН Н+ + СН3СОО –
 К СН3СООН = [Н+] × [СН3СОО –]
К СН3СООН = [Н+] × [СН3СОО –]
[СН3СООН] = 1,7 × 10-5
В отличие от общей титруемой кислотности, обусловливаемой совместным присутствием сильных и слабых кислот в вине, соке, активная кислотность выражается концентрацией лишь сильных диссоциированных кислот и определяется непосредственно как рН объекта.
В свою очередь, рН раствора отражает не всю номинальную концентрацию растворенных сильных кислот "Сн+", а лишь концентрацию их подвижных ионов "Н+" "а Н", называют активной.
Тогда аН+ = fа ·Сн +,
где fа = 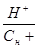 < 1; (коэффициент активности ионов
< 1; (коэффициент активности ионов
Н+ , меньше 1, т.к. ан+ всегда < Сн) и рН объекта =-lg аН+.
Поэтому активная концентрация сильных кислот, выражаемая рН, оказывает влияние на степень кислотности ("силу кислотного вкуса") вина и соков гораздо больше, чем даже высокое содержание слабых кислот.
Из слабых кислот (лимонная, яблочная и др.) наибольшей кислотностью обладает винная кислота.
рН вина, выражающий его активную кислотность, определяют по показаниям потенциометра (рН-метра), иономера.
Потенциометр включен в общую схему с электродами стеклянным (I рода) и хлорсеребрянным (II рода), погружаемыми в образец исследуемого вина.
Выполнение работы
Приборы: Потенциометр (рН-метр), иономер, электроды - хлорсеребряный (сравнения) и стеклянный (индикаторный).
Посуда: I. Стаканчик на 50 см3 .
II. Мерный цилиндр на 50 см3.
Реактивы: буферный раствор, рН = 4,01.
Подготовка прибора
Включают рН-метр тумблером в электросеть и после 30 мин прогревания настраивают шкалу рН (верхняя шкала прибора) по буферному раствору с рН около 4 (для кислотного диапазона).
Техника определения
Электроды промывают дистиллированной водой, следы ее удаляют фильтровальной бумагой и погружают электроды в стакан на 50 см3 со стандартным буферным раствором; переключатель "Виды работ" устанавливают в положение "рН", переключатель пределов измерения устанавливают на диапазон рН 2-6.
Рукояткой "Настройка по буферному раствору" устанавливают стрелку шкалы на значение рН стандартного буферного раствора, (например, рН = 4,01) и проверяют устойчивость показаний в диапазоне 2÷14 рН.
Затем выливают буферный раствор, промывают электроды и стакан дистиллированной водой, ополаскивают их образцом исследуемого вина, .наливают 25 см3 вина в стакан и погружают электроды. Вначале устанавливают переключателем пределов измерения широкий диапазон измерения рН 2-14, приблизительно оценивают значение рН по показаниям стрелки и после установки переключателем узкого диапазона рН 2-6 фиксируют точное значение рН.
Вопросы для самоподготовки
1. Сущность рефрактометрического метода анализа. Применение при анализе пищевых продуктов.
2. Сущность фотоколометрического анализа. Применение при анализе пищевых продуктов.
3. Что такое оптическая плотность раствора, от каких факторов она зависит.
4. Привести объединенный закон Бугера-Ламберта-Бера.
5. Потенциометрия. Общая характеристика метода.
6. Электроды сравнения и стандартные электроды.
7. Как определяют активную и общую кислотность пищевых систем.
8. Применение потенциометрии при анализе пищевых продуктов.
9. Поляриметрия. Общая характеристика метода. Применение поляриметрии при анализе пищевых продуктов.
10. Оптически активные вещества. Плоскость поляризации.
БИБЛИОГРАФИЯ
1. Грузинов Е.Г., Улитина Ю.И. Физико-химические свойства и методы контроля качества товаров Ч.1 и Ч.3. Учебное пособие. М; МГУТУ,2004
2. Золотов Ю.А, Дорохова Е.Н., Фадеева В.И. и др.Основы аналитической химии, т.2. – М.: Высшая школа, 1996.
3. Основы аналитической химии /Под ред. академика Ю.А. Золотова./- М.: Высшая школа, 2002, Кн.2.
4. Харитонов Ю.Я. Аналитическая химия (аналитика) Кн.2. Количественный анализ Физико-химические (инструментальные) методы анализа. – М.: Высшая школа, 2001.
5. Васильев В.П. Аналитическая химия. Кн.2 Физико-химические методы анализа – М.:, Дрофа, 2002.
6. Васильев В.П., Морозова Р.П., Кочергина Л.А., Аналитическая химия, Лабораторный практикум. – М.:, Дрофа, 2004
7. Коренман Я.И. Практикум по аналитической химии Ч.3,ч.4. Москва, КолосС, 2005
