Примеры решения типовых задач. Пример 1.Определите направление протекания при стандартных условиях реакции: Fe2O3(к) + 3H2(г) = 2Fe(т) + 3H2O(г)
Пример 1.Определите направление протекания при стандартных условиях реакции: Fe2O3(к) + 3H2(г) = 2Fe(т) + 3H2O(г)
Решение.Чтобы определить направление протекания реакции, нужно вычислить изменение стандартной энергии Гиббса
Согласно следствию из закона Гесса: ΔrG = ΣΔfG0кон – ΣΔfG0нач
Выпишем из табл.11 [] значения энергий Гиббса образования для всех участников реакции
| Fe2O3(к) | H2(г) | Fe(т) | H2O(г) | |
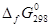 , кДж/моль , кДж/моль | –740,3 | –228,6 |
Отсюда ΔrG° = (2∙0 + 3∙-228,6) – (1∙-740,3 + 3∙0) = 54,5 кДж/моль.
Т.к. ΔrG > 0, в стандартных условиях эта реакция идет в обратном направлении.
Пример 2 .Определите знаки DrН0, DrS0 и DrG0 для реакции
АВ(к)+ В2(г) = АВ3(к),
протекающей при 298 К в прямом направлении. Будет ли DG0 возрастать или убывать с ростом температуры?
Решение.Поскольку известно, что реакция протекает в прямом направлении, следовательно, ΔrG < 0.
В левой части уравнения 1 молекула газа (В2), а в правой части уравнения газа нет, следовательно, при протекании данной реакции энтропия системы уменьшается, т.е. ΔrS <0.
Поскольку DrН0, DrS0 и DrG0 реакции связаны друг с другом уравнением:
ΔrG0 = ΔrH0– T·ΔrS0,
то знак изменения энтальпии системы может быть только отрицательным: DНr<0.
Т.к. энтропийная составляющая данной реакции положительна, то с ростом температуры DrG будет возрастать, и выше некоторой температуры реакция будет протекать в обратном направлении.
Пример 3 . При какой температуре начнетсяреакция:
С6Н6 (ж) + НNO3 (ж) = С6Н5NO2(ж) + Н2О (ж)?
При каких температурах реакция будет протекать в прямом, а при каких – в обратном направлении.
Решение. Температура начала реакции рассчитывается по формуле:
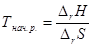
DrН0 и DrS0 рассчитывают по следствию из закона Гесса:
ΔrH = ΣΔfH0кон – ΣΔfH0нач
ΔrS = ΣS0кон – ΣS0нач ,
используя значения энтальпий образования и абсолютных энтропий участников реакции из таблицы 11 []:
| С6Н6 (ж) | НNO3 (ж) | С6Н5NO2(ж) | Н2О (ж) | |
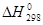 , кДж/моль , кДж/моль | 49,03 | -173,00 | 15,90 | –285,83 |
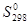 , Дж/моль К , Дж/моль К | 173,26 | 156,16 | 224,26 | 69,95 |
ΔrH = (15,90-285,83) – (49,03-173,00) = -145,70 кДж
ΔrS = (224,26+69,95) – (173,26+156,16) = -35,21 Дж/ К = -0,035 кДж/ К.
Данная реакция начнется при температуре
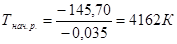 .
.
Поскольку в данной реакции энтальпийная составляющая отрицательная (DНr<0), а энтропийная – положительная( -Т ΔrS >0), то, в соответствии с уравнением:
ΔrG0 = ΔrH0– T·ΔrS0,
при Т>4162 К реакция будет идти в обратном направлении (ΔrG > 0), а при Т<4162 К - в прямом направлении (ΔrG < 0).
