Расчет состава и расхода потока
Состав потока обычно выражают в мольных, объемных или массовых долях. В ходе решения необходимо придерживаться единства размерностей. Если входной поток задают в массовых единицах (кг/ч), его состав необходимо выразить в массовых долях gi; если в мольных (кмоль/ч) или объемных (м3/ч) - в мольных ni (объемных Ji) долях.
Мольная доля ni - отношение мольного расхода i-го компонента в потоке ni к мольному расходу смеси:
ni = 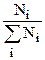 (1.1)
(1.1)
Объемная доля Ji - отношение объемного расхода i-го компонента в потоке Vi к объемному расходу смеси:
Ji = 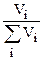 (1.2)
(1.2)
Поскольку все газы в одинаковых условиях имеют одинаковый мольный объем ni = Ji
Массовая доля gi - отношение массового расхода i-го компонента в потоке mi к массовому расходу смеси:
gi = 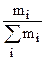 (1.3)
(1.3)
Мольные, объемные и массовые проценты получают умножением соответствующих долей на 100%.
Связь между gi и n i (Ji)задается выражениями:
gi = 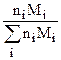 ; (1.4)
; (1.4)
ni(Ji)= 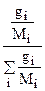 , (1.5)
, (1.5)
где Mi - молярная масса i-го компонента, кг/кмоль.
Среднюю молярную массу смеси веществ Mсм рассчитывают по формуле:
Mсм = å( niMi). (1.6)
Как видно, знаменатель выражения (1.4) равен средней молярной массе смеси, а знаменатель (1.5) - величине, пропорциональной мольному расходу потока. Поэтому вычисления gi и ni удобно начинать с нахождения этих величин.
Величина входного потока (расход вещества в единицу времени) может быть выражена в мольных (N, кмоль/ч), объемных (V, м3/ч) или массовых (m, кг/ч) единицах (рис.1.1).
Мольныйрасход i-го компонента смеси Ni рассчитывают по его массовому расходу и соответствующей молярной массе:
Ni = mi /Mi , (1.7)
а мольный расход смеси - по массовому расходу и средней молярной массе смеси:
Nсм = mсм /Mсм= mсм /å( niMi). (1.8)
Если величина потока задана в массовых единицах, а его состав в массовых долях, мольный расход реакционной смеси можно найти по формуле:
Nсм = mсм × 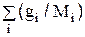 . (1.9)
. (1.9)
Массовый расход смеси рассчитывают по ее мольному расходу и составу:
mсм = Nсм× 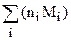 . (1.10)
. (1.10)
Газы и их смеси
Согласно закону Авогадро, при одинаковых условиях одно и то же число молекул любого газа занимает один и тот же объем. С другой стороны, 1 моль любого вещества содержит одинаковое число частиц. Таким образом, при нормальных условиях (Р0 = 101,325 кПа и Т0 = 273,15 К) 1 кмоль любого газа занимает объем 22,4 м3. В этом случае мольный расход смеси находят по ее объемному расходу:
Nсм = Vсм/22,4. (1.11)
Измерения объемов газов обычно проводят в условиях, отличных от нормальных. Для приведения объема газа к нормальным условиям можно пользоваться уравнением, объединяющим законы Бойля-Мариотта и Гей-Люссака
PV/T= P0V0/T0 (1.12)
Здесь V – объем газа при давлении P и температуре T; V0 – объем газа при нормальном давлении P0 и температуре T0.
Мольные массы газов вычисляют по уравнению Клапейрона - менделеева
PV = mRT/M, (1.13)
где P- давление газа, кПа; V – объем, м3; m – масса, кг; M – молярная масса, кг/кмоль; R- универсальная газовая постоянная (8,314 кДж/кмоль×К)
Рассмотренные соотношения справедливы лишь при очень малых давлениях.
Воздух представляет собой природную газовую смесь, состав которой для технических расчетов приведен в табл. 1.1.
Таблица 1.1.
Состав воздуха для технических расчетов
| Компоненты воздуха | O2 | N2 |
| Мольные(объемные)доли, n (J) | 0,21 | 0,79 |
| Массовые доли, g | 0,23 | 0,77 |
Различные газы смешиваются друг с другом в любых соотношениях. При этом каждый газ, входящий в состав смеси, характеризуется своим парциальным давлением. По закону Дальтона давление смеси газов, химически не взаимодействующих друг с другом, равно сумме давлений газов, составляющих смесь.
Парциальное давление i-го компонента рi в газовой смеси определяется его мольной долей в этой смеси:
рi = P×ni. (1.14)
где Р - общее давление, кПа.
Таблица 1.2.
Давление насыщенного водяного пара (Рн.п) при различных температурах
| Т,0С | Рн.п., кПа | Т,0С | Рн.п , кПа |
| 0,61 | 12,3 | ||
| 1,23 | 19,9 | ||
| 2,34 | 31,2 | ||
| 4,24 | 47,4 | ||
| 7,37 | 101,3 |
Плотность любого газа или газовой смеси r (кг/м3) можно рассчитать по формуле:
r(Р,Т)=M/V (Р,Т), (1.15)
где V (Р,Т) – объем газовой смеси при данных условиях.
Для идеальных газов и их смесей при нормальных условиях
rн,i=Mi/ 22,4 и rн,см=Mсм/ 22,4. (1.16)
