Биохимические процессы, протекающие при проращивании
Замоченный ячмень проращивают в токовых или пневматических солодовнях. В пневматических через слой проращиваемого зерна продувают воздух определенной влажности, температуры и интенсивности аэрации. При этом в зерне протекают сложные морфологические и биохимические превращения. К морфологическим превращениям относят развитие зародыша и нарушение клеточной структуры эндосперма, к биохимическим — активацию ферментов, превращение сложных веществ в простые и процесс дыхания.
При проращивании у зерна появляется зародышевый корешок (глазок), проникающий через плодовую, семенную оболочки и цветочные пленки в то место, где зерно было прикреплено к колосу. Разрываются клетки зародышевого корешка, и появляется несколько новых корешков (ростки), которые, в свою очередь, покрываются капиллярными волосками. Одновременно с этим начинает развиваться зародышевый листок (проросток, или стебелек), который прорывает плодовую и семенную оболочки и, увеличива-
 |
 |
 |
 |
Первый день
Второй-
третий
день

Четвертый-
пятый
день
Седьмой-восьмой
день
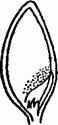
Рис. 22. Схема-растворения эндоспермапо дням проращивания зерна исоответствующим им днямразвития зародыша
ясь, продвигается между семенной оболочкой и цветочными пленками. Прометок должен развиваться только до определенной величины, не достигая вершины зерна.
На рис. 22 показано растворение эндосперма ячменя по дням проращивания 'зерна.
В начале'развития питание зародыша зерна обеспечивается за счет небольшого запаса питательных веществ (сахара, аминосоединения, минеральные вещества и др.), которые находятся вокруг зародыша и, растворяясь в воде, поступившей в зерно при замачивании, питают его. Для дальнейшего развития зародыша требуется постоянный приток нлзкомолекулярных питательных веществ, образованию которых способствуют гидролитические, ферментативные процессы.
Активация ферментов и расщепление резервных веществ эндосперма ячменя становятся возможными лишь при наличии в зерне свободной влаги. Под действием ее крахмал, белки, пектиновые вещества и др. Набухают и переходят в состояние, в котором легко атакуются ферментами. Клеточные стенки становятся более проницаемыми.
По мере проращивания часть крахмальных зерен эндосперма и вешества; связывающие их, растворяются. Эндосперм становится настолько мягким, что легко растирается между пальцами. Такое разрыхление зерна при солодоращении изменяет его плотность. Обычно плотность массы зерна ячменя составляет 1,3 г/см3 и оно тонет в воде. Плотность хорошо разрыхленных (растворенных) зерен солода меньше единицы. Поэтому при погружении в воду они плавают. Зерно плохо растворенного (стекловидного) солода тонет.
При соблюдении технологического режима солодоращения ростки зародыша достигают 1,5—2-кратной длины зерна. Зародыш листа (стебелек) с зачатками листьев, располагающийся под цветочными
пленками в виде язычка, достигает полной длины зерна. Если не прекратить проращивание зерна, то зародышевый листок прорвется наружу и образует проростки белого цвета. У тонкопленчатых ячменей цветочные пленки прорываются легче, поэтому проростки могут появиться и на ранней стадии солодоращения.
На морфологические изменения зерна и на глубину его растворения влияет интенсивность аэрации ячменя при проращивании. Слабая аэрация замедляет рост корешков, и растворение эндосперма протекает быстрее. Интенсивная аэрация способствует росту корешков и листовой части зародыша, но при этом усиливается дыхание и расходуется больше питательных веществ.
При высокой температуре и влажности аэрируемого воздуха и низкой влажности зерна рост зародыша усиливается, но ослабляются растворение эндосперма и поступление питательных веществ к зародышевому листку (проростку). В результате этого получается солод с длинными и тонкими корешками.
Активация и образование ферментов. В спелом зерне меньшая часть ферментов находится в активном состоянии, а большая часть связана с белками и поэтому не активна. При прорастании зерна белки под действием протеолитических ферментов расщепляются, и связанные с ними ферменты переходят в свободное, активное состояние. В первую очередь растворяется белковое окружение крахмальных зерен. Это позволяет открыть доступ к их гемицеллюлозным стенкам. Действие гемицеллюлаз делает доступным содержимое крахмальных зерен для воздействия а-амилазы. Накопление ферментов происходит не только в результате перехода их в свободное состояние, но и в результате новообразования в алейроновом слое и зародыше. Значительную роль в этом играет гибберелловая кислота (ГК) — ростовое вещество, образующаяся в прорастающем зерне. Она поступает из зародыша к щитку и затем к алейроновому слою, где вызывает образование и активацию ферментов. То есть ГК является индуктором образования ферментных систем (рис. 23).
Образовавшиеся из высокомолекулярных веществ под действием ферментов низкомолекулярные вещества из эндосперма через щиток
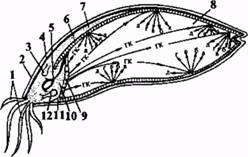
| а — р-амилаза; 6 - эндо-р-глюканаза; в — а-амилаза; г — прогеаза; д - фосфатаза; гк — гибберелловая кислота; 1 — корешки; 2 - цветковая (мякинная) оболочка; 3 - листок; 4 - плодовая (семенная) оболочка; 5 - базальный слой; 6 - алейроновый слой; 7 - зародыш листа; 8 - эндосперм; 9 - клетки эпителия; 10 - зародыш; 11 - щиток; 12 - эародаш корня. |
Рис. 23. Схема образования ферментов в при
поступают к зародышу, где служат основой для образования новых веществ, а также для участия в процессе дыхания.
В непроросшем зерне а-амилаза не определяется аналитическими методами, а при прорастании, по-видимому, частично переходит из связанного в активное состояние и частично образуется вновь. р-Амилаза в покоящемся зерне содержится в свободной и связанной формах, на вторые-пятые сутки проращивания зерна количество активной (3-амилазы значительно увеличивается. Растет активность и других ферментов.
Активность ферментов в солоде и скорость их накопления при проращивании зависят от сорта и состава ячменя, способа проращивания, интенсивности аэрации и температуры процесса. При солодо-ращении активность амилолитических ферментов возрастает в 3-5 раз, протеолитических — примерно в 2,5 раза, фосфатаз — в 5—7 раз, а-глюкозидазы - в 2 раза.
Во время проращивания в солоде увеличивается активность по-лифенолоксидазы, но в готовом солоде сохраняется только часть ее активности, окисляющей антоцианогены.
Активирование и образование ферментов идет параллельно с жизнедеятельностью зародышевого корешка.
Ферменты могут действовать при высоких температурах и в отсутствие кислорода, когда зародыш погибает. Эту их способность используют при солодоращении: сначала прорастающему зерну подают достаточно кислорода для образования ферментов, а затем подачу воздуха прекращают. При этом ферменты продолжают действовать, растворяя эндосперм, а зародыш почти не развивается. Это дает возможность уменьшать потери ценных веществ зерна.
Способность ферментов сохранять свою активность при высокой температуре используют при сушке солода. Повышая температуру в солодосушилке, зародыш убивают, почти не снижая активности ферментов. Поэтому при затирании ферменты продолжают свою работу.
Ферменты в зерне распределены неравномерно, большая часть их находится в зародыше, в эндосперме, прилегающем к щитку, и в периферийных частях зерна.
Дыхание зерна. В прорастающем зерне под действием ферментов начинается расщепление всех высокомолекулярных соединений (крахмала, белка и, др.) и превращение их в простые низкомолекулярные вещества, которые затем расходуются на рост зародыша. Проращивание зерна сопровождается интенсивным дыханием -потреблением кислорода и образованием диоксида углерода. Основным материалом для дыхания служат углеводы, но в дыхании могут участвовать также кислоты, жиры, азотсодержащие вещества. Все процессы при дыхании определяются и регулируются действием ферментов.
Различают два вида дыхания: аэробное, когда реакция протекает при избытке кислорода, и анаэробное, вызываемое недостат-
ком кислорода, повреждением растительных тканей и инактивацией дыхательных ферментов.
Баланс химических превращений углеводов при аэробном дыхании происходит по следующим схемам:
с 2н22оп + н2о = 2С6н12о6;
Мальтоза Глюкоза
С6НПО6+ 6О2 =* 6СО2 +6Н20 + 2822 кДж/г-моль (674 ккал).
По этой схеме мальтоза (С]гНдОи), образовавшаяся из крахмала под действием ферментов превращается в глюкозу (С6Н12О6), которая окисляется до диоксида углерода и воды с выделением теплоты.
При недостаточном притоке воздуха во время замачивания и проращивания нарушается естественное дыхание зерна, что наблюдается, например, при проращивании зерна в высоком слое, когда в массе зерна накапливается диоксид углерода и повышается температура. Это вызывает анаэробное дыхание, протекающее в соответствии с суммарным уравнением спиртового брожения:
С6Н|206 = 2С2Н5ОН + 2СО2 + 234,5 кДж/г-моль (56 ккал). Глюкоза Этиловый спирт
В последней реакции на каждую молекулу глюкозы, израсходованную на дыхание, выделяется в 12 раз меньше теплоты и в 3 раза меньше диоксида углерода, чем при аэробном дыхании. Поэтому, чтобы обеспечить себя необходимой энергией, зерно должно расходовать намного больше сахара, чем при аэробном дыхании. При хорошей аэрации обеспечивается более эффективное в энергетическом отношении аэробное дыхание и снижается расход углеводов, затрачиваемых на анаэробное дыхание.
То есть повышение температуры зерна и приток кислорода воздуха усиливают интенсивность дыхания, а накапливающийся диоксид углерода замедляет дыхание.
Подавление анаэробного дыхания в присутствии кислорода и развитие аэробного дыхания в этих условиях получило название эффекта Постера.
В зависимости от интенсивности аэрации в прорастающем зерне, кроме диоксида углерода всегда образуется некоторое количество органических кислот, спиртов и эфиров, благодаря чему свежепроросший солод приобретает специфический запах, напоминающий запах свежих огурцов.
При чистом аэробном дыхании дыхательный коэффициент, представляющий собой отношение объемов выделившегося диоксида углерода и поглощенного кислорода, будет равен единице.
На разных стадиях замачивания и проращивания ячменя величина дыхательного коэффициента неодинакова. В начале замачивания ячменя дыхательный коэффициент больше единицы, т. е. в это время диоксида углерода образуется больше, чем потребляется кислорода. В конце солодоращения, наоборот, дыхательный коэффициент меньше
единицы, т. е. кислорода потребляется больше, чем выделяется диоксида углерода.
Потери экстрактивных веществ зерна на дыхание значительны, величина их зависит от условий проращивания и сорта ячменя.
В табл. 8 показаны потери сухих веществ ячменя по дням проращивания.
Таблица 8
| Длительность проращивания, сут | Температура проращивания, "С | Потери сухих веществ ячменя, % | |
| на дыхание | на ростки | ||
| Первые | 14,5 | 1,08 | - |
| Вторые | 1,70 | 0,45 | |
| Третьи | 1,99 | 0,84 | |
| Четвертые | 0,99 | 1,07 | |
| Пятые | 0,61 | 1,06 | |
| Шестые | 0,51 | 0,13 | |
| Седьмые | 0,21 | 0,02 |
Наибольшие потери экстрактивных веществ наблюдаются на третьи сутки проращивания, а затем они начинают уменьшаться. В конце цикла потери в 5 раз меньше, чем в первые сутки.
Практически установлено, что для получения солода с хорошей растворимостью, высокой ферментативной активностью и минимальными потерями сухих веществ процесс солодоращения должен протекать медленно, при возможно низких температурах.
Превращение углеводов. В непроросшем зерне основное количество углеводов находится в нерастворенной форме. Небольшое количество растворимых сахароз (около 2%), содержащееся в зародыше, расходуется в начале проращивания, а затем потребность в питательных веществах удовлетворяется благодаря реакциям расщепления высокомолекулярных веществ, прежде всего крахмала. Крахмал содержится в клетках в виде круглых и овальных зерен, окруженных гемицеллюлозными мембранами и связанных между собой белковыми веществами (см. рис.3). Поэтому расщеплению крахмала предшествует расщепление гемицел-люлоз и белков соответствующими ферментами.
Крахмал на 80% состоит из амилопектина и на 20% из амилозы. Часть его расщепляется под действием амилолитических ферментов (а- и р-амилаз), разрывающих связь а-(1—4). ^-Амилаза воздействует на молекулу амилозы или амилопектина и отщепляет от цепи полисахарида молекулы мальтозы вплоть до места, где цепь имеет ответвление [а-(1-6)-связи]. а-Амилаза действует на внутренние связи и образует декстрины, состоящие примерно из 6 глюкозных остатков. Образующиеся декстрины становятся доступными для действия (5-амилазы. Мальтоза расщепляется (З-глюкозидазой до глюкозы.
Таким образом, в результате гидролиза крахмала образуется смесь олигосахаридов, декстринов и моносахаридов.
Ячмень и солод содержат ферменты, гидролюующие р-глюкан: эндо-р-глюканазу, вызывающую резкое снижение вязкости раствора р-глюкана за счет разрыва цепочки полисахарида изнутри, и экзо-р-глюканазу, последовательно отщепляющую от нередуцирующего конца молекулы полисахарида углевод целлобиозу. Для пивоварения наибольшее значение имеет эндо-р-глюканаза. При замачивании активность этого фермента не изменяется, а при проращивании нарастает и в готовом солоде она в 10—20 раз больше, чем в ячмене.
Часть Сахаров, образовавшихся при гидролизе крахмала, расходуется на дыхание и образование новых клеток в процессе развития зародыша.
Концентрация Сахаров в свежепроросшем солоде примерно в 3,5 раза больше, чем в исходном ячмене, а содержание крахмала к концу проращивания ячменя становится на 4—6% меньше.
Изменение азотсодержащих веществ. При солодоращении ячменя высокомолекулярные азотистые соединения (белки) под воздействием протеолитических ферментов претерпевают глубокие изменения. При этом снижается содержание водонерастворимого белка и повышается содержание водорастворимого белка и продуктов его ферментативного гидролиза (аминокислот и полипептидов). Считается, что в процессе солодоращения до 40% азотистых веществ становятся водорастворимыми. В действительности белковых веществ распадается значительно больше, однако часть образующихся аминокислот расходуется на развитие зародыша, а часть снова превращается в водонерастворимые белковые соединения.
Протеолитические ферменты относятся к классу гидролаз, точнее, пептидгидролаз, они расщепляют сложные соединения на более простые с участием воды в соответствии с уравнением
H,C-CH-CO-NH-CH3+H3O=H3C-CH-COOH + СНГСООН
NH2 COOH NH2 NH2
Аланилглицин Алании Глицин
Таким образом, ферменты, разрывая в полипептидной цепочке пептидную связь (—CO-NH—), присоединяют по месту разрыва воду и образуют две аминокислоты.
Солод содержит 3 группы пептидгидролаз: аминопептидазы, кар-боксипептидазы, дипептидазы. Аминопептидазы действуют при наличии в молекуле субстрата свободной а-аминной группы, расщепляют пептиды и амиды, содержащие N-концевые аминокислоты. Карбоксипептидазы расщепляют в полипептидах пептидную связь, находящуюся рядом со свободной карбоксильной группой пептида. Дипептидазы катализирует гидролитическое расщепление дипепти-дов на свободные аминокислоты.
Протеолитические ферменты, называемые протеиназами (папаин), гидролизуют внутренние пептидные связи в молекулах белков и полипептидов, поэтому носят название эндопептидаз.
При проращивании ячменя активность аминопептидазы увеличивается в 1,7—2 раза; карбоксипептидазы в 10—20 раз, по сравнению с ячменем. Дипептидаза наиболее активна в замоченном зерне, затем во время проращивания во второй стадии солодорашения ее активность падает. Активность эндопептидазы на пятые сутки солодораще-ния увеличивается в 3—12 раз по сравнению с ячменем.
Глубина растворения высокомолекулярной фракции белковых веществ влияет на качество солода и пива. При слабом растворении белков пиво плохо фильтруется и осветляется, а при понижении температуры в пиве появляется муть. Пиво, полученное из солода с сильным белковым растворением, имеет низкую пеностойкость, не обладает полнотой вкуса.
Показателем качественной оценки солода, точнее глубины распада белковых веществ, служит формольное число, т. е. число миллиграммов формольного азота в 100 г сухого вещества (СВ) солода (формольный азот — это аминный азот, определенный при использовании формалина). Солод, содержащий более 230 мг формольного азота, считается перерастворенным, 200—230 мг — очень хорошо растворенным, 180-200 мг - хорошо растворенным, ниже 180 мг -плохо растворенным.
Наиболее интенсивный распад белков совпадает с максимумом накопления и активности протеолитических ферментов (обычно на 5 сутки ращения). В результате солодоращения теряется около 11% сухих веществ зерна и до 13% белковых веществ.
Действие цитоиггических ферментов. В переходе структуры зерна в рыхлое состояние большую роль играют цитазы — цитолитические фементы, в состав которых входят целлюлазы, гемицеллюлазы, глю-каназы, ксиланазы, пектиназы и др. Они действуют, в основном, на вещества стенок клеток эндосперма. Под влиянием гемицеллюлазы стенки клеток эндосперма растворяются и становятся проницаемыми для других ферментов (оптимальные условия их действия рН 5 и температура 4УС), то есть крахмал и белок делаются доступными для амилаз и протеаз.
Гемицеллюлозу и гумми-вещества атакуют две группы ферментов: эндо-р-глкжаназа и экзо-р-глюканаза. Эндо-р-глюканаза, разрывая связи внутри молекулы fJ-глюкана, сильно снижает вязкость растворов и поэто\(у оказывают значительное влияние на технологические процессы пивоварения. При низкой вязкости пивного сусла ускоряется процесс его приготовления, а пониженное содержание р-глюкана приводит к повышению стойкости готового пива. Экзо-р-глюканаза отщепляет от концов молекул полисахаридов молекулы сахара. Во время солодоращения р-глюкан превращается в р-глюка-новые декстрины, растворы которых имеют более низкую вязкость,
затем в олигосахариды, включая целлобиозу, и так — до глюкозы. Меньшую часть гумми-веществ составляют пентозаны, которые под действием ферментов распадаются до редуцирующих Сахаров.
Оценить, насколько эффективно действуют цитолитические ферменты солода, можно по снижению вязкости лабораторного сусла.
Изменение жиров. В зерне ячменя содержится около 2% жира, при проращивании количество его уменьшается за счет окисления и расщепления ферментом липазой на глицерин и карболовые кислоты. Жир разрушает пену в пиве, поэтому переход жира в пиво нежелателен.
Изменение рН и титруемой кислотности. Водная вытяжка ячменя имеет рН 6, свежепроросшего солода 6,25, но титруемая кислотность значительно повышается вследствие расщепления углеводов, белковых веществ и образования органических кислот (молочной, янтарной, яблочной, аминокислот). Кислотность повышается также в результате дезаминирования аминокислот, т. е. процесса, в котором от аминокислот отщепляются щелочные аминогруппы и они превращаются в оксикислоты.
Титруемая кислотность ячменя, солода (при титровании с фенолфталеином) выражается в см31 н раствора NaOH, израсходованного на титрование 100 см3 лабораторного сусла. Нормальная кислотность для ячменя составляет 7—11; для свежепроросшего светлого солода 10,5—15; темного 11,5—15,5; для сухого светлого солода 14—17,5, темного 13,5—17 см3 на 100 г экстракта.
Изменение растворимого экстракта. Масса водорастворимых веществ при солодоращении (в результате ферментативных процессов) увеличивается примерно в 2 раза. Отдельные компоненты зерна растворяются по-разному. Так, из-за низкой активности амилаз крахмал при солодоращении расщепляется лишь на 4—6%. Зато при затирании (температура 65—75°С), когда достигается максимум активности амилаз, он расщепляется полностью. Белковые вещества при солодоращении расщепляются больше, чем при затирании, так как протеоли-тические ферменты имеют более низкий температурный оптимум.
