Найдите массу осадка, образующегося при сливании раствора, содержащего 16,25г хлорида железа (III) и раствора, содержащего 16г гидроксида натрия
а) 0,1моль, б) 16г, в) 10,7г, г) 14,27г
Вариант 2
1. Какое вещество проводит электрический ток?
а) безводная серная кислота
б) раствор иодида натрия в бензоле
в) раствор хлорида кальция в воде
г) раствор кислорода в воде
 2. Какое вещество диссоциирует в воде в соответствии с приведенной схемой?
2. Какое вещество диссоциирует в воде в соответствии с приведенной схемой?
 |  |  | |||||||||||||||
 |  |  | |||||||||||||||
 | |||||||||||||||||
 |  | ||||||||||||||||

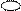



 +
+
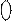 | |||||||
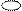 |  | ||||||
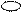 | |||||||
а) Н2; б) КОН; в) НI; г) правильного ответа нет
3. Какое вещество диссоциирует в воде в соответствии с приведенным уравнением?
М(ОН)2 = М2+ + 2OН- (М - металл)
а) K2SO4 ,б) NaOH , в) Ва(ОН)2 , г) Са(NOз)2
4. При диссоциации какого вещества не образуются ионы гидроксония НзO+?
а) А1(НSO4)3 , б) NаНСОз , в) NаОН , г) НзАsO4
5. Какое из приведенных веществ является наиболее сильным электролитом?
а) НNOз , б) Н2СО3 , в) Н2SiO3 , г) Н3РO4
6. Лакмус не изменит окраску в водном растворе:
а) оксида кремния
б) гидроксида бария
в) азотной кислоты
г) оксида кальция
7. Какие ионы не могут присутствовать в растворе одновременно?
а) Н+, К+, NO 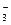 ,
,  SO
SO 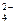
б) Nа+, Cu2+ , NO 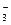 , ОН-
, ОН-
в) Н+ , Са2+, С1-, NO 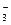
г) Мg2+, H+ , Вг -, С1-
8. С каким веществом будет взаимодействовать водный раствор сульфата меди (II)?
а) НС1 , б) NаNОз , в) Аg , г) КОН
9. Гидроксид цинка будет взаимодействовать с:
а) Мg, б) раствором Nа2SO4 , в) СаСОз, г) раствором КОН
10. Разбавленная серная кислота не будет реагировать с:
а) А1(ОН)з , б) Мg , в) раствор К2SiO3, г) правильного ответа нет
11. Сульфат свинца (II) можно получить при помощи реакции ионного обмена между:
а) Рb и разбавленной Н2SO4
б) раствором Pb(NO3)2 и ВаSO4
в) раствором Pb(NO3)2 и Н2SO4
г) РbO и SO3
12. Гидроксид железа (III) образуется при реакции между:
а) раствором FeСlз и раствором КОН
б) раствором FeCl2 и раствором КОН
в) Fe и Н2O
г) Fe2 O3 и Н2O
13. Составьте полное и сокращенное ионное уравнения реакций между гидроксидом меди (II) и серной кислотой. Найдите суммы всех коэффициентов в полном и сокращенном ионном уравнениях соответственно:
а) 12 и 3 , б) 8 и 6 , в) 10 и 6 , г) 10 и 3
14. Ионное уравнение Са2+ + СО 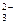 == СаСОз¯
== СаСОз¯
соответствует взаимодействию между:
а) СаSiO3 и раствором Na2СО3
б) раствором Са(ОН)2 и СО2
в) СаО и СO2
г) раствором Са(NO3)2 и раствором К2СО3
15. Найдите количество вещества, выпадающего в осадок при сливании раствора, содержащего 0,2 моль сульфата меди (II), и раствора, содержащего 0,3 моль гидроксида калия.
а) 0,3 моль , б) 0,2 моль , в) 0,15 моль , г) 0,1 моль
16. Найдите массу осадка, образующегося при сливании раствора, содержащего 4г сульфата меди (II) и раствора, содержащего 4г гидроксида натрия.
а) 2,45г , б) 4,9г , в) 4г , г) 0,1г
Галогены
Вариант 1
1. Назовите жидкий галоген:
а) хлор; б) фтор; в) бром; г) йод
2. Определите степень окисления хлора в веществе KClO3 :
а) –1; б) +1; в) +5; г) +7
3. Какой из галогенов обладает наименьшей активностью:
а) йод; б) фтор; в) хлор; г) бром
4. Какая из предложенных реакций осуществима:
Напишите уравнение
а) NaJ + F2 = б) KJ + Cl2 =
в) NaF + Cl2 = г) KCl + J2 =
5. Какой объем хлороводорода образуется при взаимодействии 5л хлора и 2л водорода (н.у.)?
а) 2л; б) 5л; в) 3л; г) 4л
6. HСlO3 – это кислота:
а) хлорноватистая; б) хлористая; в) хлорноватая; г) хлорная
7. Назовите вещество А, напишите уравнения реакций:
+H2 +KOH +AgNO3 +HNO3 +KBr




 I2 X1 X2 X3 X4 A
I2 X1 X2 X3 X4 A
а) иодид серебра; б) нитрат серебра; в) бромид серебра; г) серебро
8. Сколько литров кислорода выделяется при разложении на свету 400 мл 12% раствора хлорноватистой кислоты? (н,у.)
(r= 1,12 г/мл)?
9. Соляная кислота – это:
а) раствор хлороводорода в спирте;
б) раствор хлора в воде;
в) раствор хлороводорода в воде;
г) раствор хлора в спирте
10. Пищевая соль – это:
а) KI; б) NaCl; в) KCl; г) AgI
Вариант 2
1. Назовите твердый галоген:
а) бром; б) йод; в) хлор; г) фтор
2. Определите степень окисления хлора в хлорной кислоте HClO4:
а) +5; б) +1; в) -1; г) +7
3. Какой из галогенов наиболее электроотрицателен:
а) йод; б) бром; в) хлор; г) фтор
