П атомды спирттердің сапалық реакциясына мына әрекеттесу жатады:Cu(OH)2
101,102,103,104. УДАЧИ)))
1. Энтропияның төмендеуі жүйенің мына өзгерісі кезінде орын алады:. СҰЙЫҚТАН ҚАТТЫҒА ӨТКЕНДЕ
2. Өздігінен жүретін үдерістер кезінде: ГИББС ЭНЕРГИЯСЫ ТӨМЕНДЕЙДІ
3. Жай заттардың стандартты түзілу энтальпиясының өзгерісі тең болады (Дж/моль): ∆Но = 0
4. Термодинамиканың бірінші заңының математикалық өрнегінің түрі: Q = ∆U + A.
5. Күй параметрлерінің өзгерісіне (p = const, ∆p = const) жүйенің сәйкес келетін күйі: ИЗОБАРАЛЫҚ
6. Егер жүйенің энтальпиясы төмендейтін болса, онда реакция: 1, а.
а) жылуды бөле жүреді. б) жылуды сіңіре жүреді. в) жылу өзгермей жүредіжәне 1. Экзотермиялық 2. Эндотермиялық болады.
Сәйкестікті тағайындаңдар:
7. Жүйенің ішкі энергиясының өзгерісі былайша анықталады: ∆U = U2 – U1
8. Адам организмінде этанол екі сатыда тотығады: –493 кДж/моль
ΔН1 ΔН2
С2Н5ОН → СН3СНО → СН3СООН
ΔНº1= -256 кДж/моль; ΔНº2= -237 кДж/моль.
Гесс заңын пайдаланып, этил спиртінің сірке қышқылына дейін тотығуы реакциясының ΔНºх.р есептеңдер.
9. Гетерогенді жүйе болып табылады: СО2 + Н2О (ж).
10. Гесс заңы бойынша реакцияның жылу эффекті тәуелсіз болады: ОНЫҢ ҚАНДАЙ ЖОЛМЕН ЖҮРУІНЕ ЖӘНЕ НЕШЕ САТЫДАН ТҰРАТЫНЫНА ТӘУЕЛДІ ЕМЕС
11. Жүйе ашық болып саналады, егер ол қоршаған ортамен: ЗАТ ЖӘНЕ ЭНЕРГИЯ
12. Жүйе ...... өткенде оның энтропиясы өседі:.СҰЙЫҚТАН ГАЗҒА ӨТКЕНДЕ
13. Термодинамикада стандартты жағдай деп есептеледі: Т = 298 К, Р = 101,3 кПа
14. Жүйе ашық болып саналады, егер ол қоршаған ортамен былайша алмасатын болса: ЗАТ ЖӘНЕ ЭНЕРГИЯ
15. Гиббс энергиясы бойынша мынадай қорытынды жасауға болады:.ӨЗДІГІНЕН ПРОЦЕСТІҢ ЖҮРУІ МҮМКІНДІГІ
16. Жүйенің энтропиясы мына өзгеріс кезінде өседі:. СҰЙЫҚТАН ГАЗҒА ӨТКЕНДЕ
17. Химияда қалыпты жағдай (қ.ж.) ретінде қысым мен температураның мына мәндері алынады: Т = 298 К, Р = 101,3 кПа.
18. Эндотермиялық реакциялар кезінде ...ЖЫЛУ СІҢІРІЛЕДІ ЭНТОМОЛОГИЯСЫ ӨСЕДІ ЭНТАЛЬПИЯСЫ ӨСЕДІ
19. Гиббс энергиясын (изобарлық-изотермиялық потенциал) есептеу үшін қолданылатын формуланы көрсетіңдер: ∆G = ∆H-T∆S
20. Гесс заңынан шығатын 1-салды өрнектейтін формуланы көрстеіңдер: ^H°X.P = {^H°ТҮЗ ӨНІМ - {^H°ТҮЗ БАСТАПҚЫ ЗАТ
21. Гесстің термохимиялық заңынан туындайтын маңызды сал бойынша, химиялық реакцияның жылу эффекті тең болады: ТЕРМОХИМИЯЛЫҚ ТЕҢДЕУ РЕАКЦИЯСЫНЫҢ СТЕХИОМЕТРИЯЛЫҚ КОЭФФИЦИЕНТТЕРІН ЕСЕПКЕ АЛА ОТЫРЫП, ӨНІМНІҢ ТҮЗІЛУ ЖЫЛУЫ РЕАКЦИЯСЫНАН БАСТАПҚЫ ЗАТТЫҢ ТҮЗІЛУ ЖЫЛУЫН АЙЫРҒАНҒА ТЕҢ МӨЛШЕРІ
22. Заттардың эксперимент кезіндегі жану жылуларын анықтау үшін қолданылатын арнайы аспап былайша аталады: калориметр
23. Мына үдеріс үшін H2 (г) + 1/2 O2 (г)= H2O (г) есептеулер жүргізбей-ақ ∆S°таңбасын анықтаңдар: ∆S<0
24. Мына үдеріс үшін 2NH3(г)= N2(г)+ 3H2(г)есептеулер жүргізбей-ақ ∆S°таңбасын анықтаңдар: ∆S<0 ∆S 0 =0
25. Тепе-теңдік жағдайындағы энтальпияны есептеу үшін қолданылатын өрнекті көрсетіңдер: ∆H=TAS немесе H= U+Pv
----26. бірінші бастамасын тұжырымдаңдар: сумма изменения внутренней энергии и совершенной системой (над системой) работы равна сообщенной (или выделенной ею) теплоте
27. Энтропияның өлшем бірлігі: Дж/К
28. Химиялық үдеріс өздігінен мына жағдайда жүруі мүмкін, егер...∆G < 0 ГИББС ЭНЕРГИЯСЫ ТӨМЕНДЕЙДІ, ЭНТРОПИЯ АРТҚАНДА
29. Термохимиялық теңдеудегі стехиометрлік коэффициенттер мынаны көрсетеді: ӘСЕР БЕРЕТІН ЖӘНЕ ТУЫНДАЙТЫН ЗАТТАРДЫҢ НАҚТЫ ЗАТ МӨЛШЕРІ
30. Оқшауланған жүйе сыртқы ортамен: ЗАТ ЖӘНЕ ЭНЕРГИЯ АЛМАСПАЙДЫ ТЕРМОСТАТТАҒЫ РЕАКЦИЯ
31. Химиялық реакция міндетті түрде энергияны бөле, немесе сіңіре жүреді, себебі ... ӨЙТКЕНІ ОНЫҢ ЖҮРУІ БІР ХИМИЯЛЫҚ БАЙЛАНЫСТАРДЫҢ ТҮЗІЛІП, БІРЕУЛЕРІНІҢ АЙЫРЫЛУЫНА БАЙЛАНЫСТЫ
32. Аммиак мына реакция бойынша алынады: N2(r) + 3Н2(г) = 2NH3(г) + 92 кДж. Аммиактың стандартты түзілу жылуын көрсетіңдер. 27кДж
33. Атмосфералық қысым кезінде иодты белгілі бір температураға дейін қыздырғанда ол балқымай буланады. Қатты заттың тікелей газ күйіне өту құбылысының атауы:Сублимация
----34. Бейтараптау реакциясының стандартты жылуы –57 кДж/моль. Сілті затының мөлшері 2 моль болатын натрий гидроксидін тұз қышқылымен бейтараптау реакциясының жылу эффектін көрсетіңдер:
35. Төменде келтірілген термодинамикалық функциялардың ішінен үдерістің өздігінен жүру мүмкіндігін көрсететінін таңдап алыңдар: ГИББС ЭНЕРГИЯСЫ ТӨМЕНДЕЙДІ, ЭНТРОПИЯ АРТҚАНДА
36. Мына реакция үшін әсер етуші массалар заңының математикалық өрнегі: Cl2(г) + H2(г) = 2HCl(г)V = k[Cl2][H2]
37. Температуралық коэффициенті 3-ке тең реакцияның жылдамдығы температураны 10ºС-қа көтергенде былайша өседі:3 раза.
38. Химиялық реакцияның молекулалығы дегеніміз ... ХИМИЯЛЫҚ АЙНАЛЫМНЫҢ ЭЛЕМЕНТАРЛЫ АКТІНЕ ҚАТЫСАТЫН МОЛЕКУЛА САНЫ
39. Организмдегі химиялық реакцияларды тездететіндер: КАТАЛИЗАТОР ФЕРМЕНТ
----40. Мына жүйедегі FeO(қ) + H2(г) ⇄ Fe(қ) + H2O(г) – Q химиялық тепе-теңдік реакция өнімдері бағытында ығысады, егер:Повышении температуры
41. Реакция жылдамдығының температураға тәуелділігін анықтайтын Вант-Гофф ережесінің математикалық өрнегін жазыңдар: V2 = V1γ(∆t / 10).
42. Көптеген реакциялар үшін температураны көтергенде жылдамдықтың артуын дұрыс түсіндіретін тұжырымды таңдап алыңдар. БӨЛШЕКТЕР АРАСЫНДАҒЫ СОҚТЫҒЫСТАР КӨБЕЙЕДІ
43. Ферментті үдерістердің кинетикасын сипаттайтын теңдеу: V = Vmax[S] / (K + [S]).
----44. Кинетическое уравнение для реакции, протекающей по уравнению: В(тв) + 2А(г) = С(г):V = k[A]2
Реакция мына теңдеу бойынша жүреді: В(қ) + 2А(г) = С(г). Осы реакцияның жылдамдығы мына теңдеумен анықталады:
45. Мына реакция үшін 2Н2(г) + О2(г) = 2Н2О әсер етуші массалар заңының математикалық өрнегі: V = k[H2]2[O2].
46. Реакция жылдамдығының температуралық коэффициенті 3-ке тең. Температураны 40°С-қа көтергенде реакции жылдамдығы неше есе артады:81 раз
----47. Өте жылдам (іс-жүзінде лезде) жүретін реакцияның типі: Обмена между ионами
48. Мына реакция үшінА(с) ⇄ В(қ) + С(с) тепе-теңдік константасы неге тең: Кр = [C] / [A]
49. Мына жүйедегі тепе-теңдікті көміртек(IV) оксидінің түзулуі жағына қарай ығыстыру үшін: Повысить давление 2СО(г) + Н2(г) ⇄ СН4(г) + СО2(г) + Q
50. Әсер етуші массалар заңы бойынша:ӘСЕР ЕТУШІ ЗАТТАРДЫҢ КОНЦЕНТРАЦИЯСЫНА ХИМИЯЛЫҚ РЕАКЦИЯЛАРДЫҢ ЖЫЛДАМДЫҒЫНА ТУРА ПРОПОРЦИОНАЛЬ.
51. Әсер етуші массалар заңының негізінде 2Fe(қ) + 3Cl2(г) = 2FeCl3(қ) химиялық реакцияның жылдамдығы мына теңдеумен өрнектеледі: V = k[Cl2]3
52. Температцураны 10-нан 40ºС-қа дейін көтергенде реакцияның жылдамдығы 16 есе өсті. Осы реакция жылдамдығының температуралық коэффициенті тең болады: 2, 5.
----53. Мына жүйедегі тепе-теңдікке СО2(г) + С(қ) ⇄ 2СО(г) – 172,2 кДж көміртектің концентрациясын арттыру былайша әсер етеді:
54. Дұрыс анықтаманы таңдап алыңдар: «Химиялық реакцияның реттілігі дегеніміз»:. КИНЕТИКАЛЫҚ РЕАКЦИЯ ТЕҢДІГІНДЕГІ САНДЫҚ КӨРСЕТКІШ
55. Есер етуші массалар заңына сәйкес: ӘСЕР ЕТУШІ ЗАТТАРДЫҢ КОНЦЕНТРАЦИЯСЫНА ХИМИЯЛЫҚ РЕАКЦИЯЛАРДЫҢ ЖЫЛДАМДЫҒЫНА ТУРА ПРОПОРЦИОНАЛЬ.
56. Мына реакция үшін: С(қ) + СО2(г) ⇄ 2СО(г) тепе-теңдік константасының мәні анықталады: Кр = [СО]2 / [CО2]
57. Мына гомогенді жүйедегі 2SO2(г) + O2(г) ⇄ 2SO3(г) тепе-теңдікке қысымды қөтеру былайша әсер етеді. ТЕПЕ ТЕҢДІК ОҢҒА ЖЫЛЖИДЫ
58. Химиялық реакцияың жылдамдық константасына әсер етпейді: ЗАТТАР КОНЦЕНТРАЦИЯСЫ
59. Химиялық рекцияның жылдамдығы – бұл ... белгілі бір уақытта әрекеттесетін заттар мөлшерінің өзгеруі
60. Вант-Гоффтың эмпирикалық ережесіне сәйкес реакциялық қоспаның температурасын 30-дан 40 °С-қа дейін көтергенде химиялдық реакцияның жылдамдығы... 2-4 есе артады
61. Клапейрон-Менделеев теңдеуіндегі R шамасы былайша аталады... универсал газ тұрақтысы 8,31 Дж/К*моль
----62. Оң катализатор химиялық реакцияның жылдамдығын өзгертеді, себебі:
63. «Ерітінді бетіндегі қаныққан бу қысымының салыстырмалы төмендеуі еріген заттың молярлық үдесіне тең». Бұл анықтама кімнің заңына сәйкес келеді: Закона Рауля
64. Стаканда қайнап жатқан тұз ерітіндісінің қайнау температурасы жоғарылайды, егер: ЕГЕР ОҒАН ТАҒЫ ТҰЗ ҚОССА
65. Криоскопиялық константа тәуелді болады: ЕРІТКІШТІҢ ТАБИҒАТЫНА
66. Дұрыс анықтаманы таңдап алыңдар.Ерітінді дегеніміз:. КӨП КОММЕНТТІ ГОМОГЕНДІ ЖҮЙЕ
67. Электролит ерітінділерінің коллигативтік қасиеттерінің ұшпайтын бейэлектролит ерітінділерінің қасиеттерінен ауытқу дәрежесін көрсететін эмпирикалық коэффициент былайша аталады: Изотонический коэффициент (коэффициент Вант-Гоффа).
68. Сутектік көрсеткіш рН дегеніміз: СУ ЕРІТІНДІСІНДЕГІ СУТЕК ИОНЫ МОЛЯРЛЫҚ КОНЦЕНТРАЦИЯСЫНЫҢ ТЕРІС ТАҢБАМЕН АЛЫНҒАН ОНДЫҚ ЛОГАРИФМІ
69. Аздаған мөлшерде күшті қышқыл немесе күшті негіз қосқанда өзінің рН мәнін іс жүзінде өзгертпейтін ерітінді: Буферный
70. Судың иондық көбейтіндісі дегеніміз СУТЕК ИОНЫ МЕН ГИДРОКСИД ИОНЫНЫҢ КОНЦЕНТРАЦИЯСЫНЫҢ КӨБЕЙТІНДІСІ ТҰРАҚТЫ ТЕМПЕРАТУРАДА, КӨЛЕМ ТҰРАҚТЫ
71. Қанның буферлік қасиеттерін қамтамасыз ететін амфолиттерге жатады: Белковые буф
71. Қанның буферлік қасиеттерін қамтамасыз ететін амфолиттерге жатады: Ақуыздық буферлер
72. Генри заңы бойынша ерітіндінің берілген көлеміндегі берілген температурада еритін газдың мөлшері
тура пропорционал болады: Газдың сұйықтыққа қысымы
73. Изотонды ерітінділер – мына көрсеткіштері бірдей ерітінділер: Осмостық қысымы бірдей ерітінділер
74. NaCl концентрлі ерітіндісінде қызыл қан түйіршіктері бүрісіп қалады. Бұл кезде орын алатын үдеріс:Плазмолиз
75. Қаналмастырғыштар ретінде қолданылатын барлық ерітінділер: Қанға изотонды ерітінділер (0,9 NaCl ,5 – глюкоза , 10- альбумин ериді)
76. Егер сілтінің ерітіндісіне артық мөлшерде қышқылдың ерітіндісін құйсақ, онда ортаның рН-ы былайша өзгереді: 9 дан 5 ке дейін төмендейді
77. Буферлік сыйымдылық дегеніміз: 1 л буферлі еретіндінің pH 1 бірлікке өзгерту үшін қажетті күштіқышқыл /HCl/ не күшті негіздің /NaOH/ эквивалентті концентрациясын айтады
78. Буфферлік ерітінділер дегеніміз мына ерітінделер: Аздаған мөлшерде қышқыл HCl сілті қосып ,сонымен қатар ерітіндіні сұйылтқанда белгілі бір дәлдікпен pH ы тұрақты болып қалатын ерітіндіні
айтады
79. Төменде берілген қоспалардың ішінде буферлік әсер танытатыны: CH3COOH + CH3COONa.
80. Еріген заттың массалық үлесі көрсетеді: 100 г ерітіндідегі еріген заттың массасы
81. И.М.Сеченов заңы бойынша: Газдың электролит ерітіндісінде ерігіштігі қысым өскен сайын төмендейді
82. Дұрыс тұжырымды таңдап алыңдар. Ерітінділер: кем дегенде екі құрамдас бөліктен тұратын құрамы
өзгермелі гомогенді жүйелер (көпкомпоненнтті гомогенді жүйе)
83. Жасушаны тұздың гипертонды ерітіндісіне батырғанда байқалатын құбылыс: Плазмолиз
84. Қантты емес диабет кезінде көп мөлшерде сұйылтылған несеп бөлінеді, оның осмостық қысымы 154,6 кПа-ға дейін төмендейді. Осындай несептің ерітіндісі қан плазмасына (Росм =740-780 кПа) қатысты ........ерітінді болып саналады : Гипотонды
85. Мына теңдеу С = kP газдар үшін кімнің заңының математикалық өрнегі болып табылады: Генри заңы
86. Ерітіндідегі сутек иондарының концентрациясы өскенде: Ph ерітіндісінің сандық мағынасы төмендейді
87. Мына жұптардың буферлік әрекет танытатыны: Н2CO3 + NaHCO3.
88. Молярлық концентрациясы 0,01 моль/л калий гидроксиді КОН ерітіндісінің рН мәні: рН = 12.
89. Төменде келтірілген жұптардың ішінен қанның буферлік жүйесіне кіретінін таңдап алыңдар: H2CO3 +KHCO3
90. Ерітіндінің молялдық концентрациясы дегеніміз: 1000г еріткіштегі еріген зат мөлшері
91. Коллигативтік қасиеттерді анықтайтын қасиеттер: Еріген зат пен еріткіш арасындағы әрекеттесу
92. Ерітіндінің осмостық қысымы тәуелді: жартылай өткізгіштің мембрананың екі жағыныңконцентрациясының айырымына тәуелді
93. Жасушаны гипотонды ерітіндіге батырғанда байқалатын құбылыс:Эндоосмос
94. Газдардың ерігіштігінің температураға байланысты тәуелділігі: газдың ерігіштігі темп жоғарылаған сайын төмендейді газдың ерігіштігі -экзотермиялық процесс
95. Буферлік ерітінділерді дайындау үшін мына заттардың жұбын алуға болады:H2CO3+NaHCO3
96. Ерітіндінің молярлық концентрациясы дегеніміз: 1 л ерітіндідегі еріген заттың мөлшері
97. Ерітінді бетіндегі еріткіштің қаныққан бу қысымының салыстырмалы төмендеуін анықтайтын көрсеткіш: Еріген заттың мольдік үлесіне
98. Ерітіндінің осмостық қысымы мынаған тәуелді: жартылай өткізгіштің мембрананың екі жағының концентрациясының айырымына тәуелді
99. Қайнау температурасы кезінде: Қаныққан бу қысымы атмосфера қысымына тең
100. Берілген ерітіндімен салыстырғанда осмостық қысымы жоғары ерітінді былайша аталады:Гипертонды
101. Ерітінді бетіндегі еріткіш қаныққан бу қысымының салыстырмалы төмендеуі тура пропорционал болады: еріген заттың молдік мөлшеріне тең
102. Эбуллиоскопиялық тұрақты тәуелді: еріткіштің табиғатына
103. Буферлік әрекет танытын ерітінді: H2CO3+KHCO3
104. рН мәні берілген буферді дайындау үшін мына шамаларды білу қажет: буферлік жүйенің компоненттерінің сәйкестігін есептеу
105. Сілті бойынша да, қышқыл бойынша да ерітіндінің буферлік сыйымдылығы жоғары болуы үшін рН =9,2 буферлік ерітінді дайындаған кезде мына қоспаны алу керек: D. Боратную, К = 6,0∙10-10.
106. Қанға изотонды глюкоза ерітіндісінің концентрациясы: 5%
107. Қанға изотонды натрий хлориді ерітіндісінің концентрациясы: 0,9 пайыз
108. Байланыс полюстілігі жоғарырақ молекула: HF
109. Адамдар мен жануалардың тіршілігіне хлор мына формада қажет: Хлорид
110. Атомдары иондық байланыспен қосылған қосылыс:NaF
111. Адамдар мен жануарлар организміндегі минералдық алмасуды зерделеу үшін қолданылады:Радиоизотоптар
112. Органоген-элементтер қатарын көрсетіңдер: C.N.O.H.S
113. Организмдегі кальцийдің мөлшері шамамен 1,4% (70кг дене массасына 1 кг). Бұл элементті мына топқа жатқызуға болады:Макроэлементтің
114. Медициналық практикада дезинфекциялайтын зат және цианидтер үшін уқайтарғыш ретінде қолданылатын маргенецтің қосылысын көрсетіңдер. Оны қолдану мына химиялық қасиетіне негізделген:KMnO4. Қышқылдық/окислитель
115. Уланғанда, толассыз құсу, жедел қан жоғалтқанда, шок кезінде, жараны, сілемей қабатын жуу үшін қолданылады: натрий хлориді
116. Мына кешенді иондағы [Al(OH)x]ˉ кешентүзушінің координациялық санын анықтаңдар, егер орталық атомның заряды +3, ал лигандтың заряды -1 болса: 4
117. Калий гексанитрокобальтатының(III) химиялық формуласы: . K3[Co(NO2)6].
118. Электрстатикалық тартылыс күштерінің нәтижесінде түзілген химиялық байланыс былайша аталады:иондық
119. Азот молекуласындағы байланыстың түрі: ковалентті полюссіз
120. Көп ретте кешентүзуші ретінде бола алады:катиондар
121. Мына қосылыс үшін кешеннің заряды нөлге тең: [Pt+2(NH3)2Cl2)
122. Құрамы [Pt(NH3)3Cl]Cl болатын кешенді қосылыстың аталуы: хлоротриаминплатина II валентті хлориды
123. Кешенді қосылыстарда кешентүзуші мен лигандтардың арасында міндетті түрде байланыстың мынатүрі болады: донорлы акцепторлы механизм бойынша түзілген
124. Қалқанша безі тироксиннің негізгі элементі (массалық үлесі бойынша 65%): иод
125. Ауыз суындағы бұл элементтің аздаған концентрациялары қосылыстар түрінде тіс жегісінің алдыналады, ал жоғары концентрациялары – тіс эмалінде дақтардың пайда болуын тудырады:фтор
126. Микроэлементтердің қатарын көрсетіңдер: Fe.Zn.F.Mo.Cu
127. Адам және жануарлар тіршілігі үшін фосфор мына түрде қажет: фосфат
128. d-Қатарының микроэлементтерін көрсетіңдер: Fe CO CR
129. Адам және жануарлар тіршілігі үшін фтор мына түрде қажет: фторид
130. Организмде иод көп мөлшерде кездесетін ағза: Қалқанша без
131. Организмге ауыз суы және тағамдық заттардың құрамында келіп түсетін су былайша аталады:Экзогенді
132. Донорлық-акцепторлық механизм бойынша коваленттік байланыс түзілетін қосылыс: 𝑵𝑯𝟒𝑪𝒍
133. Екі ортақтасқан электрон жұптары арқылы екі атомның арасында түзілетін байланыс былайша аталады: Ковалентті байланыс
134. Кешенді қосылыстарда лигандтар мынадай қасиеттер көрсетеді: электронды жұптың доноры
135. Мына кешенді қосылыстағы [Ni(NH3)6]Cl3 электрон жұптарының доноры мен акцепторын көрсетіңдер:𝑵𝒊+𝟑- акцептор, 𝑵𝑯𝟑-донор
136. Бромопентаамминкобальт(III) сульфаты атауына сәйкес келетін кешен: [Co(𝑵𝑯𝟑)𝟓𝑩𝒓]𝟐𝑺𝑶𝟒
137. Тұрақтырақ кешенді ион болып табылады: . Кн[Fe(CN)6]3- = 1,0∙10-31.
138. р-Қатарының микроэлементтерін көрсетіңдер: Br , I , F
139. Хлор молекуласындағы химиялық байланыстың түрі: Коваленттік полюсті
140. Байланысқан атомдар ядроларының арасындағы қашықтықтың аталуы: ұзақ байланыс
141. Кешентүзуші – металл ионының координациялық саны ең алдымен мынаған тәуелді: Металл табиғатына
142. Төменде келтірілген қосылыстардың ішінен ішкі кешенді қосылыстарға (хелаттар) жататыны:
143. Органоген-элементтер қатарын көрсетіңдер:
144. Организм үшін уытты элементке жатқызуға болады:
145. Табиғаттағы (бүкіл Әлемдегі) ең көп тараған элемен:
146.Атомның заряды тең болады:
147. Молекуладасында байланыс s- және p-электрон бұлттарының қабысуынан пайда болған:
148. Қышқылдық қасиеттері өте айқын байқалатын заттың формуласы
149. Кальций мен фтор негізінен жинақталатын нысан:
150. Асқазан сөлінің құрамына кіретін қышқыл:
151. Уыттылығы өте жоғары (улы) элементтердің қатары:
152. Антисептикалық, күйдіргіш әсер көрсететін зат:
153. Адамдар мен жануарлардың тыныс алу ферметтерінің құрамына кіретін топтар:
154. Мына кешендегі Na4[Сd(ОН)6] кешентүзуші-ионның координациялық санын (КС) көрсетіңдер::
155.Кешенді қосылыстардың мына белгілерінің ішінен оларды жіктеуге негіз болатындарын таңдап алыңдар:
1. Лигандтардың табиғаты 2. Кешентүзушінің табиғаты.
3. Кешеннің бояуы. 4. Кешенді ионның заряды.
5. Кешентүзушінің координациялық саны.
156. Лигандтың дентаттылығы дегеніміз:
157. Орбитальдық квант саны атомның мына қасиеттерін анықтайды:
158. s-Орбитальдағы электрондардың максимал саны:
159. р-Орбитальдағы электрондардың максимал саны:
160. Бас квант санының n қабылдайтын мәндері:
161. d-Элементтеріне жататын элементтер жұбы:
162. Төменде келтірілген үшінші период элементтерінің ішінен айқын бейметалдық қасиеттер көрсететіні:
163. Иондық байланыс дегеніміз:
164. Коваленттік байланыс дегеніміз:
165. Донорлық-акцепторлық байланыс дегеніміз:
166. Мына қатарда N2O3, P2O3, As2O3, Sb2O3, Bi2O3:
167. Сутектік байланыс дегеніміз:
168. Периодта элементтің реттік нөмірі өскенде оксидтер қатарындағы қышқылдық қасиеттер:
169. Бейметалдарға жататын элементтердің қатары:
170. Бір элементтің екі изотопының атомдары ерекшеленеді:
171. Күрделі бейорганикалық заттарды әдетте төрт топқа бөледі:
172. Оксидтер деп мына қосылыстарды айтады:
173. Пероксидтер деп мына қосылыстарды айтады:
174. Екідайлы оксидтерге жататын қатар:
175. Негіздерге қышқылдармен реакция тән, олар ....... реакциясы деп аталады.
176. Н2 молекуласындағы байланыстың түрі:
177. Сутектің тотығу дәрежесі -1 болатын қосылыс:
178. Оттектің тотығу дәрежесі -1 болатын қосылыс:
179. Байланыстың сипатын былайша болжауға болады:
180. Химиялық реакция міндетті түрде энергияны бөліп немесе сіңіріп жүреді, себебі:
181. Иондық қосылыстардан тұратын қатар:
182. Табиғатта тек ионды қосылыстар түрінде кездесе алатын металдардың қатарын көрсетіңдер:
183. Сумен сутекті бөле әрекеттесетін металдардың қатарын көрсетіңдер:
184. Стандартты сутек электродынан және өзінің тұзына батырылған металл электродынан тұратын гальваникалық элементте сутек бөле жүретін реакция жүреді. Металды көрсетіңдер:
185. Ерітіндінің рН-ын мына тізбектің көмегімен өлшеуге болады:
186. Электродтық потенциалды есептеу үшін қолданылатын формула:
187. Түрлі электродтардың тепе-теңдіктегі потенциалының температура мен электролиттің концентрациясына тәуелділігі:
188. Мембраналық потенциал негізінен мына иондар жұбының концентрациясымен анықталады:
189. Концентрациялары әр түрлі бір электролиттің екі ерітіндісінің немесе екі әр түрлі электролит ерітінділерінің жанасу шекарасында пайда болатын потенциал былайша аталады:
190. Бейстандартты жағдайлардағы тотығу-тотықсыздану потенциалын анықтайтын фомула:
191. Потенциометрлік титрлеу деп титрлеу барысында эквиваленттік нүкте былайша анықталатын титриметрлік талдау әдісін айтады:
192. Кондуктометрлік титрлеу деп титрлеу барысында эквиваленттік нүкте былайша анықталатын титриметрлік талдау әдісін айтады:
193. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында электрөткізгіштігі ең жоғары болатын электролит:
194. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында иондық күші ең жоғары болатын электролит:
195. Молярлық концентрациясы бірдей электролиттердің сулы ерітінділерінің арасында электрөткізгіштігі ең жоғары болатын электролит:
196. Тотығу-тотықсыздану электроды дегеніміз:
197. Мембраналық потенциал негізінен мына катионның концентрациясымен анықталады:
198. Тотығу-тотықсыздану потенциалының шамасы тәуелді болады:
199. Тотығу-тотықсыздану электроды - құрамында .... бар ерітіндіге батырылған .... тұратын жүйе. Дұрыс сөздерді орнына қойыңдар.
200. Электрөткізгіштігінің мәні ең жоғары болатын биологиялық сұйықтықты немесе адам организмінің тінін көрсетіңдер:
201. Электрөткізгігштігінің мәні ең төмен адам организмінің тінін көрсетіңдер:
202. Электролиттер ерітінділеріндегі электр тогын тасымалдаушылар - ....., олар электролиттің ....... нәтижесінде түзіледі. Жіберілген сөздерді орнына қойыңдар.
203. Стандартты сутектік электрод – бұл:
204. Мыс электродының потенциалын мына формула бойынша анықтауға болады:
205. Мембраналық потенциал – мына шекарада пайда болатын потенциал:
206. Төмендегі кондуктометрлік титрлеу қисығы мына реакцияға сәйкес келеді:
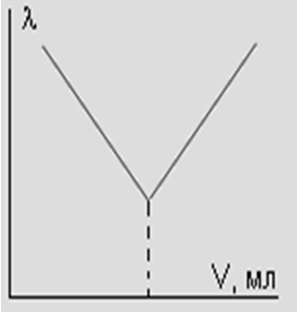
207. Фазааралық бөліну ауданы өскенде беттік энергияның өзгеруі:
208. Көміртек(IV) оксиді қатты кальций оксидіне адсорбцияланғанда СаСО3 түзіледі. Бұл үдерістің атауы:
209. Мына берілген заттардың қайсылары: Nа2SО4 (1), Н3РО4 (2), КОН (3), изоамил спирті (СН3)2СН(СН2)2ОН (4), анилин С6Н5NН2 (5), пальмитин қышқылы СН3(СН2)14СООН (6) суға қатысты беттік белсенділік қасиеттер танытады:
210. Адсорбция изотермасы адсорбцияның мына факторға тәуелділігін көрсетеді:
----211. Мына қатардағы СН3СН2СН2СООН > СН3СН2СООН > СН3СООН беттік керілістің заңдылығын сипаттайтын ереже:
212. Қатты дененің немесе сұйықтықтың газ тәріздес немесе еріген затты сіңіруі былайша аталады: Адсорбция
213. Пластмасса пластинкасына бір тамшыдан: бензин, сынап және су тамызылды. Бұл кезде бензиннің тамшысы жайылып кетеді, сынап тамшысының формасы шар тәрізді болады, ал су тамшысы жалпаяды: сынап
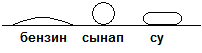
Осы заттарды беттік керілістерінің төмендеуі бойынша қатарға орналастырыңдар.
214. Оң адсорбция кезіндегі адсорбенттің беттік керілісі ....... және оң адсорбцияланатын заттар ........ деп аталады:Төмендейді, жоғарғы-активті заттар
215. Панет-Фаянс ережесіне сәйкес Ca2+, Mg2+, Cl‾, Br‾, J‾, K+ иондарының ішінен АgCl бетінде талғамды адсорбциялана алатындары:Cl. Br. I
216. Қатты дененің бетінде жүретін молекулалық адсорбция мына заттарға тән:электролиттік емес және газдарға
----217. Судың бетінде ББЗ молекуласының дұрыс бағытталуына сәйкес келетін сурет:
218. Мына берілген иондардың: NO3‾, Na+, PO43-, Sr2+, Al3+, Br‾, SO42- адсорбент SrSO4 бетінде адсорбциялана алатындары: Sr2+, So42-
219. Г = –С/RT(Δσ/ΔC) теңдеуі қандай фазалардың бөліну шекарасындағы адсорбцияны сипаттайды:сұйықтық-сұйықтық , сұйықтық-газ
220. Мына тұжырымдама: «Қаныққан қышқылдар мен спирттердің қатарында тізбек бір СН2-тобына ұзарғанда сулы ерітіндіде гомологтың беттік белсенділігі 3-3,5 есе өседі» сәйкес келетін ереже (заң): Дюило-Траубе ережесі
221. Коллоидтық химияда қос электрлік қабат түзілген кезде бет аудан зарядының таңбасын анықтау үшін қолданылатын тұжырым (ереже):
222. Бір заттың екінші бір зат бетінде жинақталу үдерісі былайша аталады: адсорбция
223. Атмосфералық қысымның күрт төмендеуі кессон ауруын тудыруы мүмкін. Мұндай сырқатты емдеу үшін: Ауруды барокамераға апарып жоғары қысымға түсіріп кейін қысымды жайлап түсіреді
224. Мына теңдеу Г = Гmax P/ (K + P) ..... теңдеуінің математикалық өрнегі болып табылады: Ленгмюра
225. Талғамды адсорбцияны анықтайтын ереже: Панет Фаянс
226. Бүйректің жұмыс жасауының негізінде жатқан үдеріс: Диализ
227. Пластинкаға бір тамшыдан үш сұйықтық тамызылды:
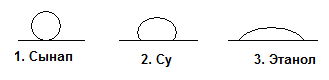
Осы заттарды беттік керілістерінің өсуіне қарай бір қатарға орнналастырыңдар: 1,3,2
----228. Өкпенің жоғары адсорбциялық әсері мына физикалық сипаттаманың салдарына байланысты:
229. Сумен талғамды суланатын беттердің аталуы: Гидрофилді
----230. Газ фазадан адсорбенттің қатты бетіне сәйкес келетін адсорбция изотермасының қисығы:
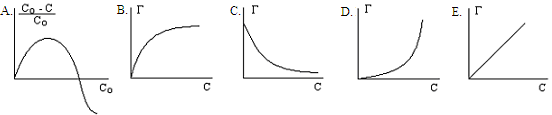
231. Беттік белсенді зат: НСl
232. Коллоидтық ерітінді арқылы жарық шоғын өткізгенде байқалатын құбылыс: Жарықтың шашырауы, (дифрокатция)
233. Коллоидтық ерітінділерді тазарту әдісі: Диализ, Электродиализ, Ультрафильтрозия
234. Электрофорез кезінде қозғалады: дисперсті фазаның зарядталған бөлшегі
235. Мыс(ІІ) гидроксидінің золі теріс зарядталған бөлшектерден тұрады. Мына қосылған электролиттердің ішінде коагуляция табалдырығы ең төмен: алюминий хлориді (III) AlCl3
236. Салмақ күштерінің әсерінен қалқып жүрген (диспергацияланған) бөлшектердің тұну жылдамдығы ескермеуге болатындай өте аз жүйелер былайша аталады: Кинетикалық және агрегаттық тұрақтылық
237. Теріс зарядталған бөлшектері бар коллоидтық ерітіндінің бөлшектері қай электродқа қарай қозғалады: Анод
238. Нәруыздың ісіну дәрежесінің ортаның рН-ына тәуелділігі екі максимумы және бір минимумы бар қисықпен сипатталады. Минимумға сәйкес келетін нүктені былайша атайды: изоэлектрлік нукте
239. Коллоидтық бөлшектердің аттас зарядтарының және (немесе) еріткіш молекулаларынан тұратын сольват қабығының болуымен байланысты тұрақтылықтың түрін былайша атайды: агрегаттық седиментациялық тұрақтылық
240. Төменде келтірілген анықтамалардың ішінен электрофорезге сәйкес келетінін таңдай алыңдар: сыртқы электр өрісі әсерінен дисперсті фазаның зарядталған бөлшектердің дисперсті ортаға қатысты қозғалуы
241. Бөлшектері теріс зарядталған кремний қышқылының золі үшін мына қатарда СrС13 (1), Ва(NО3)2 (2), К2SО4 (3) коагуляция табалдырығы былайша орналасады: 3>2>1
242. Дисперстік фазасы сұйық ортада қалқып жүрген өлшемдері 10-5 м-ден (100 мкм) жоғары болатын қатты бөлшектерден тұратын микрогетерогенді жүйенің аталуы: cуспензия
243. Дисперстік фаза бөлшектерінің ірірек агрегаттарға жабысуы (бірігуі) былайша аталады: коагуляция
244. Оң зарядталған бөлшектері бар зольге теріс зарядты бөлшектері бар зольді қосқан кезде байқалатын үдеріс:ӨЗАРА КОАГУЛЯЦИЯ
245. Коллоидтық ерітінділердің молекулалық-кинетикалық қасиеттеріне жатады:БРОУНДЫҚ ҚОЗҒАЛЫС
246. Каучуктың ісіну дәрежесі ең төмен болатын еріткіш:СУ
247. Ионданған негіздік және қышқылдық топтарының саны тең полиэлектролит молекуласының зарядтары бірдей болатын күйі былайша аталады:ИЗОЭЛЕКТРИЧЕСКИМ СОСТОЯНИЕМ
248. Температура жоғарылағанда құрылымданған жүйелердің тұтқырлығы:ҚҰРЫЛЫМЫН БҰЗЫЛУЫНА БАЙЛАНЫСТЫ ТӨМЕНДЕЙДІ
249. Артық мөлшерде алынған күміс нитратының сулы ерітіндісіне баяу натрий хлоридінің сулы ерітіндісі қосылды. Күміс хлоридінің коллоидтық ерітіндісі түзілді. Золь бөлшектерінің заряды: ОҢ
250. Оң зарядталған бөлшектері бар коллоидтық ерітіндіге мына иондарды қосқан кезде жоғары коагуляциялық белсенділік және тез коагуляция байқалады:РО4 3-
251. Фарадаей-Тиндаль эффекті мына жүйелерде байқалады:КОЛЛОИДТЫ ЕРІТІНДІЛЕРГЕ
252. Дисперстік фазасы сұйық ортада қалқып жүрген өлшемдері 10-7 – 10-9 м (1-100 мкм) болатын қатты бөлшектерден тұратын микрогетерогенді жүйенің аталуы: КОЛЛОИДТЫ - ДИСПЕРСТІ
253. Жартылай өткізгіш мембраналардың кішімолекулалық қоспаларды (иондар мен молекулаларды) өткізіп, коллоидтық бөлшектерді ұстап қалу қасиеттеріне негізделген құбылыс: ДИАЛИЗ
254. Дисперстік фазасы сұйық ортада қалқып жүрген өлшемдері 10-5 см (100 мкм) болатын сұйық бөлшектерден тұратын микрогетерогенді жүйелердің аталуы:СУСПЕНЗИЯ
----255. Сұйықтықтың беттік керілісі температура жоғарылағанда:
256. “Агрегаттық тұрақтылық” дегеніміз: БӨЛШЕКТЕРДӘІ ФАЗАЛЫҚ ІРІЛЕТУІНЕ ЖЕТЕТІН ПРОДУЦЕНТТЕРГЕ ЖҮЙЕНІҢ ҚАРСЫ ТҰРУ ҚАБІЛЕТІ
257. Артық мөлшерде алынған NaJ сулы ерітіндісіне баяу AgNO3 сулы ерітіндісі қосылды. Күміс иодидінің коллоидтық ерітіндісі түзілді. Золь бөлшектерінің зарядын көрсетіңдер: ТЕРІС
258. Электроосмос кезінде электр өрісінде қозғалатын бөлшектер: ДИСПЕРСТТІК ОРТА
259. Ас қорыту кезіндегі майларды эмульгациялайтын зат: ӨТ ҚЫШҚЫЛЫ
260. Инсулиннің изоэлектрлік нүктесі 6-ға тең. Нәруыздың электрофорездік қозғалғыштығы ең төмен болатын рН-тың мәні: 6
261. ЖМҚ концентрациясы өскенде олардың осмостық қысымы тезірек өседі де, Вант-Гофф заңына бағынбайды. Ауытқудың себебі мынада: ЖМҚ ИКЕМДІ ТІЗБЕКТЕР БІРНЕШЕ ҚЫСҚА МОЛЕКУЛАЛАР РЕТІНДЕ ӘРЕКЕТ ЕТЕДІ
----262. Сынауықтағы суға шайқай отырып, бірнеше тамшы шайыршықтың (канифоль) ерітіндісі қосылды. Коллоидтық ерітіндіні алу әдісінің аталуы:
263. Көп мөлшерде алынған күміс нитратының сулы ерітіндісіне натрий хлоридінің сулы ерітіндісі абайлап қосылды. Коллоидтық ерітіндіні алу әдісінің аталуы: ОҢ
264. Дисперстік фазасы сұйық ортада қалқып жүрген өлшемдері 10-5 см-ден (100мкм) жоғары қатты бөлшектерден тұратын микрогетерогенді жүйенің аталуы:СУСПЕНЗИЯ
265. Әр түрлі зарядталған бөлшектері бар зольдерді араластырған кезде орын алатын құбылыс: КОЛЛОИДТЫ ӨЗАРА ҰЙҚАС
266. Теріс зарядталған бөлшектері бар мыс(ІІ) сульфиді золінің ерітіндісіне қосылған иондардың ішінде коагуляциялық қабілеті ең жоғарысы: Al(3+)
267. Жекелеген электролиттің әсеріне қарағанда электролиттер қоспасының тиімдірек әсері былайша аталады: cинергизм электролит
268. Эмульсияға жататын жүйе: гетерогенді
269. Коллоидтық бөлшектердің ірірек агрегаттар түзіп, бір-біріне жабысу үдерісі былайша аталады:
270. Желатиннің сулы ерітіндісіне спиртті қосқанда ерітіндіге еріген затпен байытылған тамшылардың бөлінуі байқалады. Бұл құбылыстың аталуы:
271. Жоғарымолекулалық заттарды (крахмал, желатин, альбумин) қосқанда лиофилді зольдердің электролиттердің коагуляциялық әсеріне тұрақтылығының өсуі былайша аталады:
272. Медицинада менингитті диагностикалау үшін жұлын сұйықтығының «алтын санын» анықтайды. «Алтын саны» мынаны сипаттайды:
273. «Протаргол» және «Колларгол» препараттары ..... дисперсті жүйе болып табылады, ондағы химиялық элемент ......: КОЛЛОИДТЫ ДИСПЕРСТІ ЖҮЙЕ, КҮМІС, ОТТЕК,АЗОТ
274. Сірнелер мен гельдердің көлемінің сұйықтықтың бөлінуі салдарынан өздігінен кішірею құбылысын былайша атайды: СИНЕРЕЗИС ҚҰБЫЛЫСЫ
275. Субстанциялардың (бірқатар химиялық ерітінділер немесе биологиялық құрылымдар, мысалы, жасушалардың цитоплазмалары) механикалық әсердің нәтижесінде тұтқырлықтарының төмендету және тыныштық күйде тұтқырлықтарын өсіру қабілеті былайша аталады: ТИКСОТРОПИЯ
276. Полимердің массасы және көлемінің өсуі арқылы жүретін жоғарымолекулалық қосылыстың кішімолекулалық еріткішті өздігінен таңдамалы сіңіру үдерісі былайша аталады:
277. Мицелланың формуласын жазған кезде потенциаланықтағыш иондарды мына ережеге сәйкес таңдайды:
278. Физиотерапевтік әдіс – дәрілік заттың ерітіндісін (иондарын) электр өрісінің әсерінен тері немесе сілемейлі қабат арқылы денеге енгізу мына құбылысқа негізделген:
279. Эмульсиядағы дисперстік фаза мен дисперсиялық ортаның агрегаттық күйлерін көрсетіңдер:1,2- дибромэтан
280. Дұрыс тұжырымды көрсетіңдер: «Этиленді бромдау кезінде....»: электрофил G- байланыстарды шабуылдайды
281. Мына формуладағы CH3→ CH2→ Br атомдардың арасындағы бағдар көрсете : G- бай ланыстардың тізбегі бойынша электрондық тығыздықтың ығысуы
282. Спирттер, аминдер, тиолдарға тән реакцияның түрі және механизмі:АN Нуклеофильді қосып алу
283. Спирттер, аминдер, тиолдарға тән реакцияның түрі және механизмі:АN Нуклеофильді орынбасу
284. Спирттердің дегидратациялануы қандай механизм бойынша жүреді: E Мономолекулярлық (элминдеу)
285. Алкендерге тән реакцияның түрі және механизмі: Электрофильді қосылу
286. Арендерге көбірек тән реакцияның түрі және механизмі:SE Электрофильді орынбасу
287. Қаныққан көмірсутектерге тән реакцияның түрі және механизмі:SR Радикалды орынбасу
288. Пропеннің хлорсутекпен әрекеттесу реакциясының түрі және механизмі:Электрофилді қосып алу
289. Марковников ережесі бойынша жүретін әрекеттесу реакциясы: Пропеннің сутекпен
------290. Төменде келтірілген органикалық қосылыстың қайсысында sp3-гибридтік күйдегі көміртек атомы бар:4-хлорлы көмірсу
291. Ацетилен молекуласының С2Н2геометриялық формасын көрсетіңдер:Сызықтық және диагональды
------292. Нуклеофилді бөлшектің ең маңызды белгісін таңдап алыңдар: Электрон жұбының донорлығы
293. Электрофилді бөлшектің ең маңызды (негізгі) белгісін таңдап алыңдар:Электрон жұбының акцепторлығы(Бос валентті орбитальдің болуы)
294. Жұптаспаған электроны бар және заряды жоқ бөлшектің аталуы: Бос радикал және нейтрон
295. Ароматты көмірсутекке жатады:Толуол,арен,финол,бензол
296. sp3-, sp2- және sp-гибридтік күйдегі көміртек атомдарына сәйкесінше қандай валенттік бұрыштар тән 10905, 1200, 1800
297. Ең жоғары теріс индуктивтік әсер (–Ј) танытатын топ СL
298. Қосарланған жүйеге жатады:Жауабы: С.
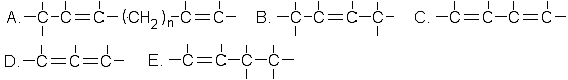
299. Бензолдың гомологтарын алған кезде (Фридель-Крафтс реакциясы) алкилдеуші реагент болып табылады: R-Cl, AlCl3
300. Полимерлену реакциясы мына көмірсутекке тән:Изопрен
301. Бензолды синтездеуге болатын қанықпаған көмірсутек..... және бұл кезде реакцияға заттың ...... мөлшері қатысады:Ацетиленнің 3 молі
302. -С6Н5радикалының аталуы:Фенил
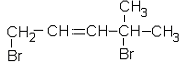
303. Қосылысты халықаралық номенклатура бойынша атаңдар:1,4-дибром – 4метилпентен-2
304. Наркоз үшін келтірілген заттардың ішінен С2Н5-О-С2Н5 формуласына сәйкес келетін затты көрсетіңдер: Диэтилді эфир (этоксиэтан)
305. Электрофилді реагенттер дегеніміз – бұл: Электрон жұбының акцерторы болатын бөлшектері
306. Нуклеофил – бұл: Электрон жұбының доноры болатын бөлшек
-----307. Радикалды реагенттер болып табылады: бос атомдар және жұп емес электрондар
308. Электрофилді қосып алу реакциясы мына қосылыс үшін мүмкін болады: Бутен-2 қышқылы
-----309. Келтірілген қосылыстардың ішінде монофункциялық қосылысқа жатады: 1 группа Гидроксибензол (фенол)
-----310. Келтірілген қосылыстардың ішінде полифункциялық қосылысқа жатады: көп группа Жүзім (шарап) қышқылы
-----311. Келтірілген қосылыстардың ішінде монофункциялық қосылысқа жатады:Пальмитин қышқылы, алкан,алкен, алкодиен,алкины
312. Келтірілген қосылыстардың ішінде монофункциялық қосылысқа жатады: Ацетон
313. Бренстед қышқылдары дегеніміз мына бөлшектер: (донор)Протон беруге бейім бейтарап молекула және иондар
314. Бренстед негіздері дегеніміз мына бөлшектер:(акцептор) Протон қосып алуға бейтарап молекула және иондар
-----315. Мына анықтама «Бос орбитальдары бар және электрон жұбын қосып алып коваленттік байланыс түзуге қабілетті атом, молекула немесе ион» сәйкес келеді: электрофил(Льюис қышқылы)
316. Коваленттік байланыс гомолиттік үзілген кезде түзілетінбөлшектер:Бос радикалдар
317. Бутадиен-1,3 молекуласындағы С2 – С3байланысының ұзындығы бутан молекуласындағыға қарағанда қысқарақ. Мұны немен түсіндіруге болады:С2 мен С3 атом арасындағы қосымша π-байланыстың түзілуі
318. Брёнстед-Лоури теориясына сәйкес күштірек қышқщыл болып табылады: С2Н5ОН
319. Келтірілген орынбасарлардың қайсысы бензол сақинасындағы орто- және пара-орындардағы көміртек атомының электрондық тығыздығын арттырады:Этил –С2Н5
-----320. Кетондар осы спирттерден тотықтырған кезде алынады: Екіншілік спирттерден
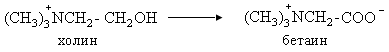
-----321. Бетаинді алу реакциясының типін көрсетіңдер: Ферменттік тотығу
-----322.Үшіншілік спирт:2-метилпропанол-2
323. Адреналинге мына органикалық қосылыстардың қасиеттері сәйкес келеді: Аминдер,спирт
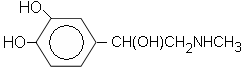
324. Этанаминді ацетамидтен және хлорэтаннан алу реакцияларының сәйкесінше типтерін көрсетіңдер: нуклеофильді орын басу, тотығу
1) СН3CONH2→ С2Н5NH2 2) С2Н5Cl → С2Н5NH2
325. Хлорлы этилге NaOH сулы ерітіндісімен әсер еткенде алынатын қосылыс: спирт және натрий хлориді С2Н5ОН
326. 1,2-диолды фрагментке сапалық реакцияны жүргізетін қосылыс: CuOH2
-----327. Фенолды бромдау реакциясының типі мен механизмі:Электрофильді орын басу
328. Этиленгликоль этиленнің мына затпен әрекеттесуі кезінде түзіледі: Калий перманганатының сулы ерітіндісі
329. Элиминдеу реакциясымен этиленді алу үшін қажет бастапқы қосылыс:Этанол
330.Анилин құрылысы төмендегідей аминдерге жатады: С6Н5NH2 бірінші ароматты
п атомды спирттердің сапалық реакциясына мына әрекеттесу жатады:Cu(OH)2
