Уравнение Гендерсона, выводы из него. Основные характеристики буферных растворов. Буферная емкость. Использование буферных систем в анализе
Уравнение показывает как зависит кислотно-основное равновесие буферного раствора от свойств компонентов кислотно-основной буферной системы и от количественного соотношения этих компонентов в растворе. Показателем кислотно-основного равновесия в растворе является водородный показатель, pH. Свойство кислоты (её способность распадаться на ионы), как составляющей буферной системы, характеризуется значением константы равновесия, константы диссоциации кислоты, Ka. (или в логарифмической форме pKa = – lgK, в частности, если K = 10–11, то pK = 11). Количественая структура (состав) буферной системы может быть оценена в виде отношения соль/кислота (эквиваленты, эквивалентная масса). Учитывая сказанное, уравнение Гендерсона-Гассельбаха выглядит следующим образом:pH = pKa + lg (соль/кислота).С помощью этого уравнения можно оценить любую из его переменных, если известны две другиеБуферные растворы-это растворы, способные сохранять приблизительно постоянное значения рН при добавлении к ним небольших количеств сильных к-т или сильных оснований. Содержат либо одно индивид.в-во, либо смесь в-в.Примеры-к р-ам индив.в-в относятся насыщенный водный раствор гидротартрата калия KHC4H4O6, водный раствор тетрабората натрия(буры) Na2B4O7*10H2O, пример буферных систем из смеси в-в могут служить водные растворы, содержащие хлороводородную к-ту и глицин, ацетатный буфер – водный р-р уксусной к-ты и ацетата натрия, универсальная буферная смесь(смесь ортофосфорной, уксусной и борной к-т с р-ом гидроксида натрия)..Определение буферной емкости (β)по ГФ-БЕ называют выраженное в грамм-эквивалентах количество сильного основания(В), прибавления которого к 1 л.буферного раствора вызывает возрастание величины рН этого раствора на единиц. β= 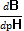 . Дистил.вода, применяемая для определения буферных растворов, должна иметь значения рН=5,8-7,0.Вкачественном и количественном анализе буферные системы испол-ют тогда, когда необходимо поддерживать постоянное значения рН среды.Н-р, при комплексонометрич.определении катионов некоторых металлов(Mg, Ca, Pb и др) применяют аммиачно-буферную смесь, ацетатный буфер используют при отделении ионов бария отионов кальция и стронция с помощью дхромат ионов.
. Дистил.вода, применяемая для определения буферных растворов, должна иметь значения рН=5,8-7,0.Вкачественном и количественном анализе буферные системы испол-ют тогда, когда необходимо поддерживать постоянное значения рН среды.Н-р, при комплексонометрич.определении катионов некоторых металлов(Mg, Ca, Pb и др) применяют аммиачно-буферную смесь, ацетатный буфер используют при отделении ионов бария отионов кальция и стронция с помощью дхромат ионов.
Окислительно – восстановительные системы. Окислительно – восстановительные потенциалы редокс – пар (стандартный окислительно – восстановительный потенциал, реальный условный потенциал, формальный окислительно – восстановительный потенциал). Типы электродов (электроды сравнения, индикаторные электроды, их строение, функции). Уравнение Нернста.
Окислительно-восстановительные системы. ОВР используются как в качественном, так и в количественном анализе.В любой ОВР участвуют две редокс пары. Редокс пара-это система из окислительно, восстановительных форм данного вещества, в котором окисленная форма является акцептором электронов и восстанавливается, принимая электроны, а восстановленная форма –донор электронов и окисляется отдавая электроны.Существуют вещества, которые в одних реакциях окислители, в др.-восстановители(зависит от природы партера реагента и условий протекания ОВР)-н-р,Н2О2, нитрит-ионNO2-2 и др.Окислительно-восстан.потенциалы редокс пар-мера способности химического вещества присоединять электроны (восстанавливаться). Окислительно-восстановительный потенциал выражают в милливольтах (мВ). Биологически важной системой является система:Fe3+/Fe2+.Примером окислительно-восстановительного электрода:Pt/Fe3+,Fe2+Стандартный ОВП – когда все участники ОВР нах-ся в стандартных состояниях, их активности =1.Реальный условный потенциал –это потенциал редокс пары при условии, что участники р-и находятся в реальных условиях, а не в стандартных состояниях.Формальный ОВП системы-это условный потенциал редокс пары при формальных конц. реагентов.(т.е.при конц.=1 моль/л).Типы электродов. Электроды сравнения - электрохимические системы, предназначенные для измерения электродных потенциалов. Необходимость их использования обусловлена невозможностью измерения абс. величины потенциала отдельного электрода.В качестве электрода сравнения может служить любой электрод в термодинамически равновесном состоянии, удовлетворяющий требованиям воспроизводимости, постоянства во времени всех характеристик и относительной простоты изготовления. Для водных электролитов наиболее часто применяют в качестве электродов сравнения водородный, каломельный, галогеносеребряные, оксидно-ртутный и хингидронный электроды. Уравнение Нернста - уравнение, связывающее окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, и стандартными потенциалами окислительно-восстановительных пар.
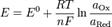 ,где
,где 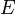 - электродный потенциал, E0 - стандартный электродный потенциал, измеряется в вольтах;
- электродный потенциал, E0 - стандартный электродный потенциал, измеряется в вольтах; 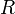 — универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
— универсальная газовая постоянная, равная 8.31 Дж/(моль·K); 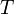 — абсолютная температура;
— абсолютная температура; 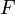 — число Фарадея, равное 96485,35 Кл/моль;
— число Фарадея, равное 96485,35 Кл/моль; 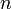 — число моль электронов, участвующих в процессе;
— число моль электронов, участвующих в процессе; 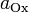 и
и 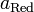 — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
— активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
Потенциал реакции (ЭДС реакции). Направление протекания окислительно – восстановительной реакции. Связь ЭДС с энергией Гиббса Влияние различных факторов на значения о. – в. потенциалов и направления протекания реакций. Использование окислительно – восстановительных реакций в анализе.
Потенциал реакции(Е)-величина равная разности ОВ потенциалов редокс-пар(т.е.их электродных потенциала)Н-р, в реакции Се+4+Fe+2=Ce+3+Fe+3(число электроноы здесь=1), уравнение для потенциала(ЭДС) р-ии - Е=Е0 - - 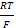 ln
ln 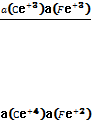 , где Е0 - стандартный потенциал реакции.В числители под знаком логарифма записано произведение активности продуктов реакции, а в знаминателе –произведение активности исходных в-в.В общем случае для ОВР ее потенциал(ЭДС) – Е=Е1-Е2, где Е1иЕ2-окислительно-восстанов.потенциалы двух редокс-пар.Направления протекания ОВР. Учет знака потенциала ОВР позволяет определить направление протекания р-ии.Если потенциал Е больше нуля(Е=Е1-Е2>0), то р-ия протекает в прямом направлении в соответствии с записью уравнения р-ии.Если <0, р-ия протекает в обратном направлении, если он равен 0, то система находится в состоянии устойчивого хим. Равновесия. Связь ЭДС с энергией Гиббса.Потенциал реакции(ееЭДС) Е связан с изменением энергии Гиббса ∆Gпри протекания данной реакции соотношением: ∆G=-nFE, изменении энергии Гиббса при любой химической р-ии меньше нуля,тор-ия протекает в прямом наравлении в соответствии с записью в уравнении.Если ∆G>0, р-ия идет в обратном направлении, ∆G=0 –устойчивое хим.равновесие.Всегда n>0 и F>0, можно сделать вывод:при ∆G<0, потенциал р-ии Е>0, ∆G>0, потенциал р-ии Е<0, ∆G=0 – Е=0.Влияние факторов на значение ОВ потенциалов.Зависят от природы р-ии(природа реагента, растворителя), конц.реагентов, рН среды, темпер., присутствие др.в-в в растворе.Использование.ОВР широко испол.как в качественном, так и в колич.анализе.в качественном анализе-(н-р, катионы одновалентной ртути, открывают действуя на него хлоридные комплексы олова в соляной к-те-выпадает белый осадок каломелиHg2Cl2., анионы, облад-ие выраж. восстановительными св-ми окисляются йодом(н-р, анионы S-2, SO3-2, S2O3-2.) или раствором перманганата калия в серно кислой среде. В количественном агравиметрическом анализе используется ОВР (для определения железа(11) его предварительно окисляют до железа (111) прибавляя конц. азотную к-ту., после чего осаждают р-ом аммиака, затем прокаливают до оксида Fe2O3 и взвешивают), при анализе ЛРС измельченный образец озоляют(путем окислительного нагревания и прокаливания) в фарфоровом тигле превращают в минеральный остаток –золу, которую затем анализируют.
, где Е0 - стандартный потенциал реакции.В числители под знаком логарифма записано произведение активности продуктов реакции, а в знаминателе –произведение активности исходных в-в.В общем случае для ОВР ее потенциал(ЭДС) – Е=Е1-Е2, где Е1иЕ2-окислительно-восстанов.потенциалы двух редокс-пар.Направления протекания ОВР. Учет знака потенциала ОВР позволяет определить направление протекания р-ии.Если потенциал Е больше нуля(Е=Е1-Е2>0), то р-ия протекает в прямом направлении в соответствии с записью уравнения р-ии.Если <0, р-ия протекает в обратном направлении, если он равен 0, то система находится в состоянии устойчивого хим. Равновесия. Связь ЭДС с энергией Гиббса.Потенциал реакции(ееЭДС) Е связан с изменением энергии Гиббса ∆Gпри протекания данной реакции соотношением: ∆G=-nFE, изменении энергии Гиббса при любой химической р-ии меньше нуля,тор-ия протекает в прямом наравлении в соответствии с записью в уравнении.Если ∆G>0, р-ия идет в обратном направлении, ∆G=0 –устойчивое хим.равновесие.Всегда n>0 и F>0, можно сделать вывод:при ∆G<0, потенциал р-ии Е>0, ∆G>0, потенциал р-ии Е<0, ∆G=0 – Е=0.Влияние факторов на значение ОВ потенциалов.Зависят от природы р-ии(природа реагента, растворителя), конц.реагентов, рН среды, темпер., присутствие др.в-в в растворе.Использование.ОВР широко испол.как в качественном, так и в колич.анализе.в качественном анализе-(н-р, катионы одновалентной ртути, открывают действуя на него хлоридные комплексы олова в соляной к-те-выпадает белый осадок каломелиHg2Cl2., анионы, облад-ие выраж. восстановительными св-ми окисляются йодом(н-р, анионы S-2, SO3-2, S2O3-2.) или раствором перманганата калия в серно кислой среде. В количественном агравиметрическом анализе используется ОВР (для определения железа(11) его предварительно окисляют до железа (111) прибавляя конц. азотную к-ту., после чего осаждают р-ом аммиака, затем прокаливают до оксида Fe2O3 и взвешивают), при анализе ЛРС измельченный образец озоляют(путем окислительного нагревания и прокаливания) в фарфоровом тигле превращают в минеральный остаток –золу, которую затем анализируют.
Общая характеристика комплексных соединений, классификация комплексных соединений. Строение комплексных соединений. Равновесия в растворах комплексных соединений. Константы устойчивости и нестойкости комплексных соединений. Условные константы устойчивости. Влияние различных факторов на процесс комплексообразования.
Комплексные соединения- это соединения, образованные из простых, способных к самостоятельному существованию.КС образуют как металлы, так и не Ме.(чаще Ме).КС состоит из атома металла-компексообразователя М, с которым связаны лиганды L. Атом М и лиганды L образуют внутреннюю сферу комплекса(внутреннюю координац.сферу), она заключается в квадратные скобки. Если внутренняя сфера комплекса несет отриц. Или полож. Заряд, то для компенсации этого заряда необходимы ионы, обр-щие внешнюю сферу.K4[Fe(CN)6]·3H2O-тригидрат гексацианоферрата(11) калия.Атом металла-комплексообразователя выступает железо(11), лиганд- CN-.Железо(11) и шесть цианогрупп образуют внутреннюю координац.сферу комплекса, внешняя сфера –четыре катиона К+ и 3 молекулы воды. На первом месте записывается комплексообразователь, а за ним – лиганды. Число лигандов отмечается цифрой в нижнем индексе. Формулу комплексного иона (внутренняя сфера) заключают в квадратные скобки, и тогда заряд комплексного иона записывается в верхнем индексе за скобками.В формуле комплексной соли (или соединения) частицы внешней сферы записывают перед скобками, если ионы имеют положительный заряд (катионы), и после скобок, если их заряд отрицателен (анионы). Числа ионов внешней сферы отмечаются нижним индексом при формуле иона. Классификация.1.По принадлежности КС к определенному классу соединений(комплексные к-ты, комп.основания, комп.соли)2.По природе лиганда(аквакомплексы, аммиакаты, ацидокомплексы,гидрокомплексы 3.По знаку заряда комплекса(катионные, анионные, нейтральные –заряд комплекса=0)4.По внутренней структурекомплекса. КС катионного и анионного типа чаще всего растворимы в воде.В их водных растворах устанавливается хим.равновесие.Комплексы-не электролиты-мало растворимы, растворившая часть этих комплекса введет себя как слабый электролит.Н-р, при растворении ферроцианида калия K4[Fe(CN)6]→4K++[Fe(CN)6]4- это электролитическая диссоциация-отщепляются ионы внешней сферы, затем происходит вторичная диссоциация комплекса- отщепляются леганды внутренней сферы[Fe(CN)6]4-+ H2O=[ Fe(CN)5(H2O)]-3+ CN-, [ Fe(CN)5(H2O)]-3+ H2O=[ Fe(CN)4(H2O)2]-2+ CN-, [Fe(CN)(H2O)5]++ H2O=[Fe(H2O)6]+2+ CN-,каждая ступень диссоциации внутренней сферы комплекса характеризуется своей константой химического равновесия. Прочность комплексного иона характеризуется его константой диссоциации, называемой константой нестойкости. 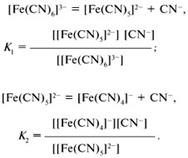
Аналогично составляются выражения для К3, К4, К5, К6, в которых квадратными скобками обозначены равновесные концентрации ионов.В аналитической химии вместо констант нестойкости в последнее время пользуются константами устойчивости комплексного иона:
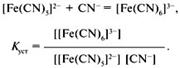
Константа устойчивости относится к процессу образования комплексного иона и равна обратной величине константы нестойкости:Куст = 1/Кнест.Константа устойчивости характеризует равновесие образования комплекса.Константы нестойкости или константы устойчивости определяются различными физико-химическими методами. Использование химических методов затруднено, т.к. измерение равновесных концентраций веществ часто приводит к смещению равновесия. Условная константа устойчивости меньше, чем реальная, почти в 10м раз. Условные константы устойчивости имеют большое практическое значение, поскольку при фиксированных рН и концентрации лиганда побочной реакции они постоянны и ими можно пользоваться в расчетах так же, как и обычными константами устойчивости. В то же время расчеты с использованием условных констант значительно менее трудоемки, так как коэффициенты побочных реакций можно рассчитать заранее и табулировать. Условные константы устойчивости сохраняют постоянное значение только при строго конкретных условиях, например при постоянных значениях рН и ( или) постоянных концентрациях посторонних лиган-дов. Их следует применять в тех случаях, когда известны значения а и их зависимость от рН или концентрации постороннего лиганда. Условные константы можно использовать в расчетах точно так же, как и обычные константы, однако результаты таких расчетов относятся к конкретным частным условиям. Влияние факторов на процесс комплексообразование.Влияние рН среды, конц.лиганда(чем больше конц. Лиганда, тем полнее металл связывается в комплекс), влияние посторонних ионов, образующих малорастворимые соединения с металлом-комплексообразователем(введение посторонних ионов, может привести к разрушению комплексов), влияние ионной силы раствора(изменение ионной силы р-ра изменяются равновесные активности ионов),влияние температуры.
Методы разделения и концентрирования веществ в аналитической химии. Основные понятия. Классификация методов разделения и концентрирования. Осаждение и соосаждение. Применение экстракции в аналитической химии. Принцип метода жидкостной экстракции. Основные понятия жидкостной экстракции.
Методы разделения и конц.в-в.Понятие. Разделение –это операция(процесс), в результате которой компоненты, составляющие исходную смесь отделяются друг от друга.Концентрирование –это операция(процесс), в результате повышается отношение конц.(кол-ва) микрокомпонента к конц. Макрокомпонента(или основы).Результаты конц.количественно хар-ют коэффициентом концентрирования Кконц=  Кконц-коэфф.концентрирования(>1),
Кконц-коэфф.концентрирования(>1),  конц. в-ва в исходном р-ре и после концентрирования,
конц. в-ва в исходном р-ре и после концентрирования,  объем исходного р-ра и после концентрирования.Классификация. Физические методы –упаривание(неполное испарение растворителя), выпаривание(испарения растворителя досуха),перегонка(отделение летучих компонентов).Химические методы-осаждения, соосождение.Осаждение-разделение(систематический ход анализа),концентрирование(осаждение определяемого иона из большого объема анализируемого раствора и растворение осадка в малом объеме).Физ-хим. Методы-экстракция, хромотография.Соосаждение-это одновременное осаждение из одного и того же р-ра растворимого в данных условиях микрокомпонента с выпадающим в осадок макрокомпонентом. Соосаждение- осаждение с коллектором. Причины соосаждения-поверхностная абсорбция(соосажденное в-во адсорбируется на поверхности коллектора и осаждается с ним), окклюзия(механический захват части маточного р-ра с соосаждаемым ионом внутрь осадка коллектора), инклюзия(включение соосаждаемого в-ва в кристаллическую решетку коллектора).Экстракция – это когда из водного р-ра в-во извлекается в несмешивающийся с водой органический растворитель.ПрименениеЭксракция надхромовой к-ты при обнаружении ионов хрома(синяя окраска), экстракция роданидного комплекса кобальта при обнаружении инов кобальта(синяя окраска).Принцип метода.Основана на использовании различной способности в-в распределятся между двумя несмешивающимеся контактирующими жидкими фазами., т.е. на их различной растворимости в этих жидких фазах.Основные понятие жидкостной экстракции. Экстрагент-органический растворитель, извлекающий данное в-во из водной фазы. Экстрагируемое в-во-в-во, извлекаемое экстрагентом из водного р-ра.Экстракционны реагент-в-во, способствующее экстракции извлекаемого в-ва.Экстракт-отдельная жидкая органическая фаза, со-ая экстрагированное из водного р-ра в-во.Экстрактор- аппарат для проведения экстракции.
объем исходного р-ра и после концентрирования.Классификация. Физические методы –упаривание(неполное испарение растворителя), выпаривание(испарения растворителя досуха),перегонка(отделение летучих компонентов).Химические методы-осаждения, соосождение.Осаждение-разделение(систематический ход анализа),концентрирование(осаждение определяемого иона из большого объема анализируемого раствора и растворение осадка в малом объеме).Физ-хим. Методы-экстракция, хромотография.Соосаждение-это одновременное осаждение из одного и того же р-ра растворимого в данных условиях микрокомпонента с выпадающим в осадок макрокомпонентом. Соосаждение- осаждение с коллектором. Причины соосаждения-поверхностная абсорбция(соосажденное в-во адсорбируется на поверхности коллектора и осаждается с ним), окклюзия(механический захват части маточного р-ра с соосаждаемым ионом внутрь осадка коллектора), инклюзия(включение соосаждаемого в-ва в кристаллическую решетку коллектора).Экстракция – это когда из водного р-ра в-во извлекается в несмешивающийся с водой органический растворитель.ПрименениеЭксракция надхромовой к-ты при обнаружении ионов хрома(синяя окраска), экстракция роданидного комплекса кобальта при обнаружении инов кобальта(синяя окраска).Принцип метода.Основана на использовании различной способности в-в распределятся между двумя несмешивающимеся контактирующими жидкими фазами., т.е. на их различной растворимости в этих жидких фазах.Основные понятие жидкостной экстракции. Экстрагент-органический растворитель, извлекающий данное в-во из водной фазы. Экстрагируемое в-во-в-во, извлекаемое экстрагентом из водного р-ра.Экстракционны реагент-в-во, способствующее экстракции извлекаемого в-ва.Экстракт-отдельная жидкая органическая фаза, со-ая экстрагированное из водного р-ра в-во.Экстрактор- аппарат для проведения экстракции.
