Реакционная способность алканов и циклоалканов
Негосударственное образовательное учреждение
Высшего профессионального образования
«Самарский медицинский институт «РЕАВИЗ»
О.А. Журавская
ОСНОВНЫЕ КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ИХ РЕАКЦИОННАЯ СПОСОБНОСТЬ
Учебно-методическое пособие
Для студентов медицинских вузов
Самара 2011
УДК
Ж 91
Рецензенты:
– кандидат химических наук, доцент А.А. Данилин;
– кандидат химических наук, доцент О.К. Шаховкина.
Журавская О.А. Основные классы органических соединений и их реакционная способность:Учебно-методическое пособие для студентов медицинских вузов. – Самара, НОУ ВПО «Самарский медицинский институт «РеаВиЗ», 2011 − 52 с. ???
Изучение биоорганической химии в медицинских вузах связано с усвоением большого объема материала при малом количестве аудиторных часов.
В учебном пособии освещены вопросы строения и реакционной способности основных классов органических соединений, материал представлен в текстуальной форме, таблицах, схемах и рисунках, что позволяет оптимизировать процесс запоминания.
Пособие предназначено для студентов медицинских вузов, обучающихся по специальностям «Лечебное дело» и «Стоматология» очной и очно-заочной формы обучения.
© НОУ ВПО СМИ «РеаВиЗ», 2011
Раздел 2. Основные классы органических соединений и их реакционная способность
Реакционная способность алифатических и ароматических углеводородов
Реакционная способность алканов и циклоалканов
К предельным (или насыщенным) углеводородам относят углеводороды, в молекулах которых атомы углерода находятся в состоянии sp3-гибридизации. По строению углеродного скелета такие углеводороды делят на алканы и циклоалканы.
Алканы – это ациклические насыщенные углеводороды с общей формулой СnH2n+2.
Неполярные связи С–С и С–Н в алканах (и циклоалканах) не склонны к ионному разрыву, но способны расщепляться гомолитически под действием свободных радикалов.
Значит, для алканов характерны реакции радикального замещения SR (от англ. substitution radicalic).
По этому механизму протекают реакции галогенирования (алканы циклоалканы С5 – С6):
Этапы:
1. Инициирование цепи:
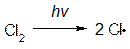
свободные радикалы
Высокая реакционная способность радикалов объясняется их стремлением достроить внешний электронный уровень до устойчивого октета.
2. Развитие цепи:
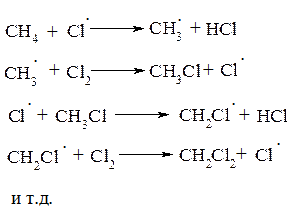
В результате последовательных реакций в цепи могут образоваться:
CH3Cl – хлористый метил (хлорметан);
CH2Cl2 – хлористый метилен (дихлорметан);
CHCl3 – хлороформ (трихлорметан);
CCl4 – четыреххлористый углерод (тетрахлорметан).
3. Обрыв цепи:
а) Cl· + Cl· → Cl2
б) CH3· + Cl· → CH3Cl
в) CH3· + CH3· → CH3 – CH3
Реакция региоселективна.
Региоселективность – предпочтительное протекание реакции по одному из нескольких реакционных центров одинаковой химической природы.
Скорость SR:
третичные УВ > вторичные УВ > первичные УВ
(связано со стабильностью образующихся радикалов и подвижностью водородов под влиянием +J-эффекта)
