Бензен як представник ароматичних вуглеводнів
Будова молекули. Молекулярна формула бензену - С6Н6 .
Першим структурну формулу бензену запропонував у 1865 році німецький хімік А.Кекуле:
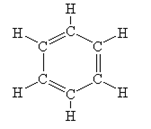
Через кілька років Кекуле висунув ідею, що подвійні зв’язки не закріплені в молекулі, а постійно переміщуються від одного атома Карбону до іншого:
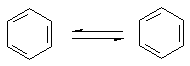
Проте і ця формула не повністю відповідає реальній структурі молекули бензену. в молекулі бензену немає простих і подвійних зв’язків. Електронна густина розподілена рівномірно, а тому всі зв’язки між атомами Карбону в молекулі бензену рівноцінні. Найточніше це відображає структурна формула у вигляді правильного шестикутника з колом усередині:
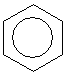
Фізичні властивості бензену: Рідина, безбарвна, має специфічний запах, t кипіння = 80°С, не розчиняється у воді, добре розчиняється у спиртах, ацетоні, етерах та інших органічних розчинниках. Також сам бензен є чудовим розчинником для багатьох речовин.
Хімічні властивості бензену.
1) Повне окиснення (горіння). Бензен горить кіптявим полум’ям :
С6Н6 + 7,5 О2 → 6 СО2 + 3 Н2О
2 С6Н6 + 15 О2 → 12 СО2 + 6 Н2О
2) Реакції заміщення атомів Гідрогену в бензольному кільці на галоген (протікає легше, ніж в алканів) :

C6H6 + Br2 → C6H5Br + HBr
3) Реакції приєднання (протікають значно важче, ніж заміщення).
а) приєднання водню (гідрування) :

C6H6 + 3 H2 → C6H12
б) приєднання хлору (хлорування) :
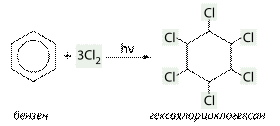
C6H6 + 3 Cl2 → C6H6Cl6
Застосування бензену:
1) Виробництво отрутохімікатів для захисту рослин;
2) Як розчинник;
3) Виробництво вибухових речовин;
4) Як добавка до моторного палива;
5) Органічний синтез, наприклад, одержання аніліну, фенолу, стирену й полістирену, лікарських препаратів.
Оксигеновмісні органічні сполуки.
Спирти.
Багато органічних сполук містять у своїх молекулах, крім атомів Карбону і Гідрогену, ще й атоми Оксигену. Такі сполуки називаються оксигеновмісними. Оксигеновмісні сполуки поділяються на класи – клас спиртів, клас карбонових кислот, клас естерів, клас жирів тощо.
Спирти – це органічні сполуки, які містять одну або більше гідроксильних груп, безпосередньо зв’язаних з насиченим атомом Карбону. Загальна формула спиртів R(OH)n , де R – вуглеводневий радикал.
За природою вуглеводневого радикалу спирти поділяють на насичені, ненасичені та ароматичні.
За кількістю гдроксидних груп спирти поділяють на одноатомні та багатоатомні.
Загальна формула одноатомних насичених спиртів – CnH2n+1OН.
Типовими представниками насичених одноатомних спиртів є метанолCH3OH і етанолC2H5OH. Оскільки до складу молекул наведених спиртів входить одна гідроксильна група OH, такі спирти належать до одноатомних.
Гідроксильна група OH є функціональною групою, тобто такою, що зумовлює хімічні властивості спиртів.
За систематичною номенклатурою, назву спирту утворюють від назви відповідного насиченого вуглеводню, додаючи до неї суфікс -ол.
