Растворимость неорганических веществ в воде
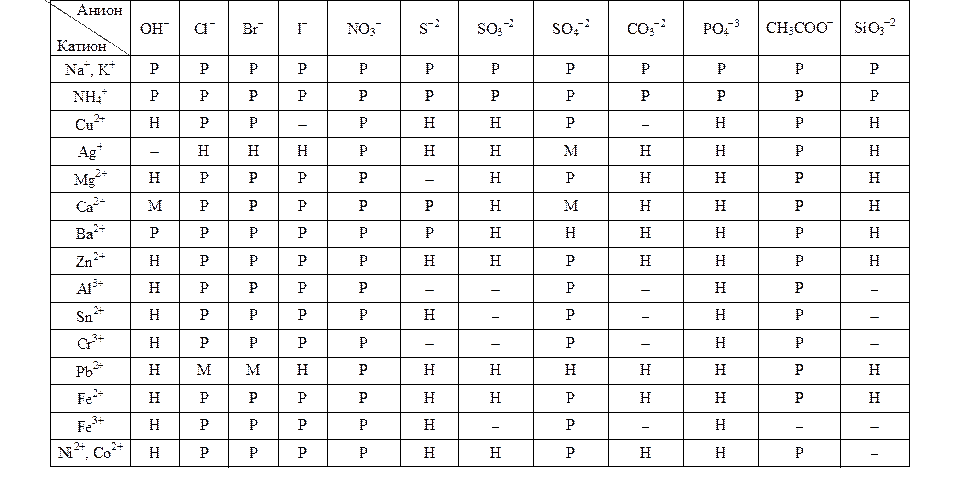
Примечание. Р – растворимое соединение; М – малорастворимое соединение; Н – нерастворимое вещество, прочерк – вещество не существует или разлагается водой.
Таблица 3
Названия важнейших кислот и их солей
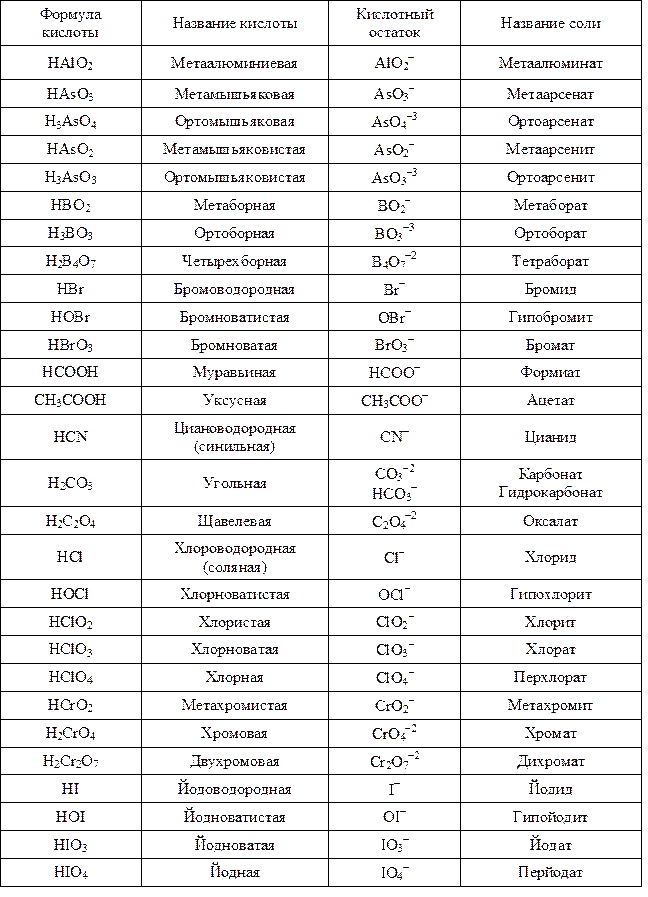 Окончание табл. 3
Окончание табл. 3
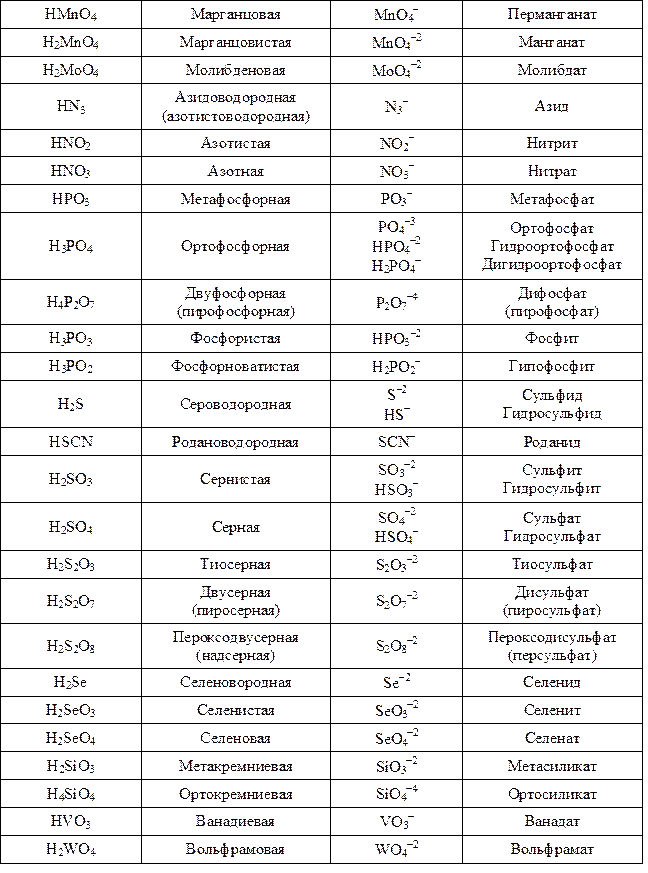
Таблица 4
Стандартные энтальпии образования DНо298, энтропии Sо298
и энергии Гиббса D Gо298 некоторых веществ при 298 К (25°С)
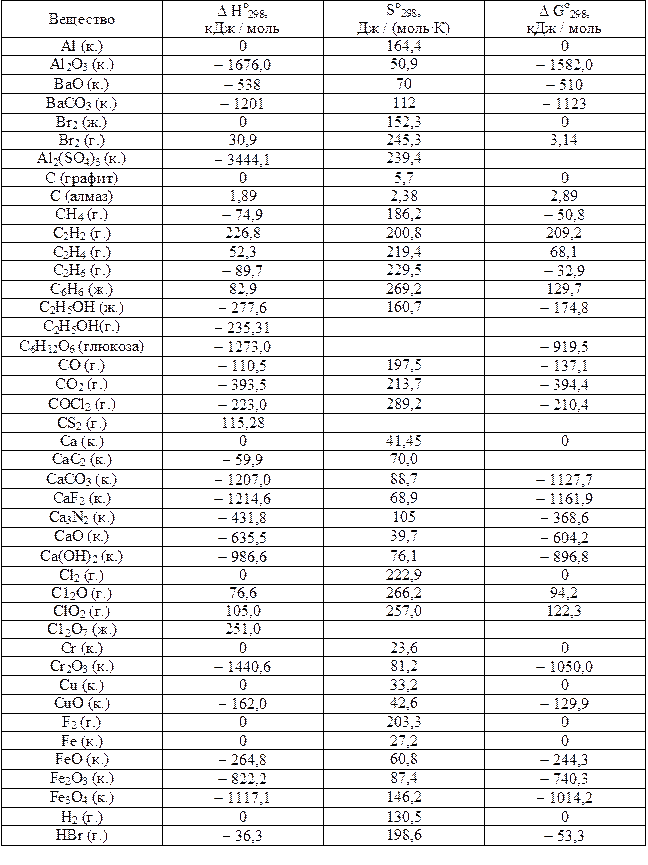
Окончание табл. 4
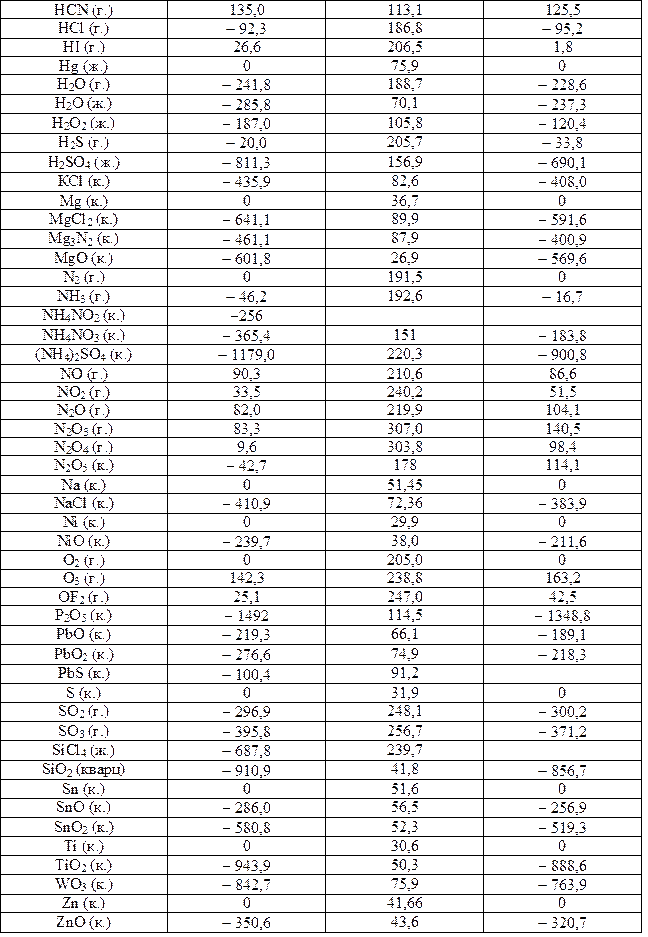
Таблица 5
Константы и степени диссоциации некоторых слабых электролитов в водных растворах при 25 °С
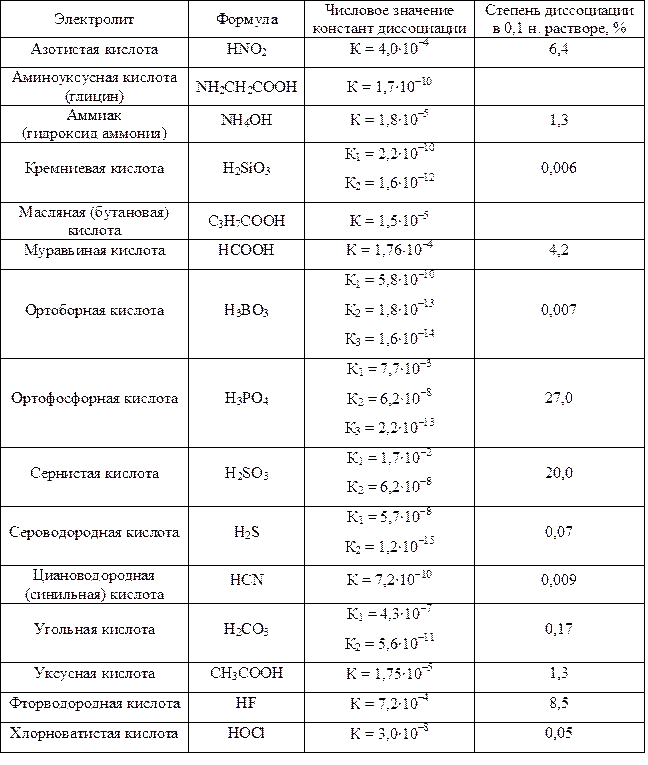
Таблица 6
Произведение растворимости некоторых малорастворимых веществ в воде при 25 °С
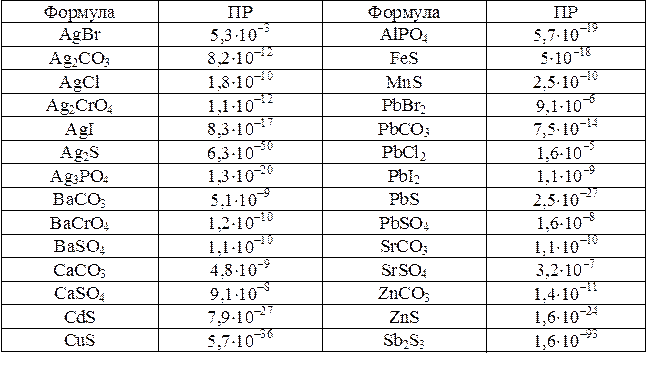
Таблица 7
Константы нестойкости некоторых комплексных ионов в водных растворах при 25 °С
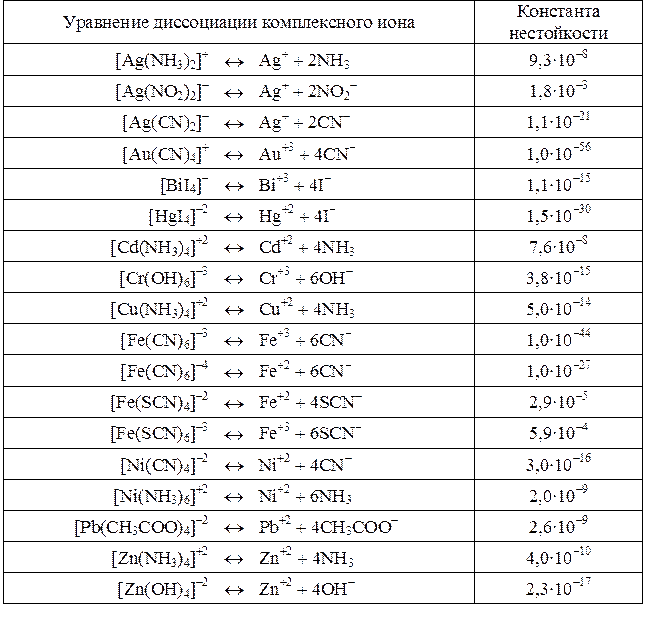
Таблица 8
Стандартные окислительно-восстановительные потенциалы металлов (j°)
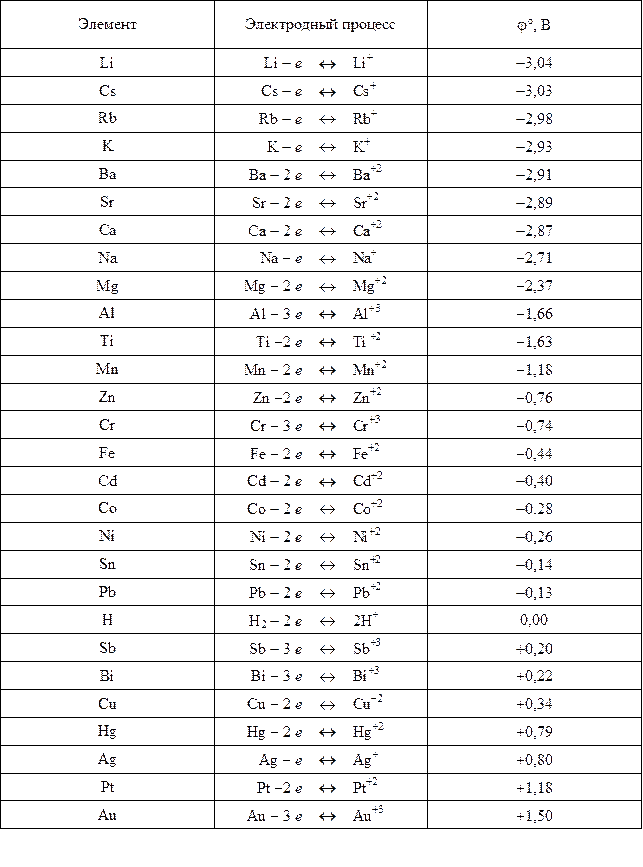
Таблица 9
Стандартные электродные потенциалы j° в водных растворах при 25 °С
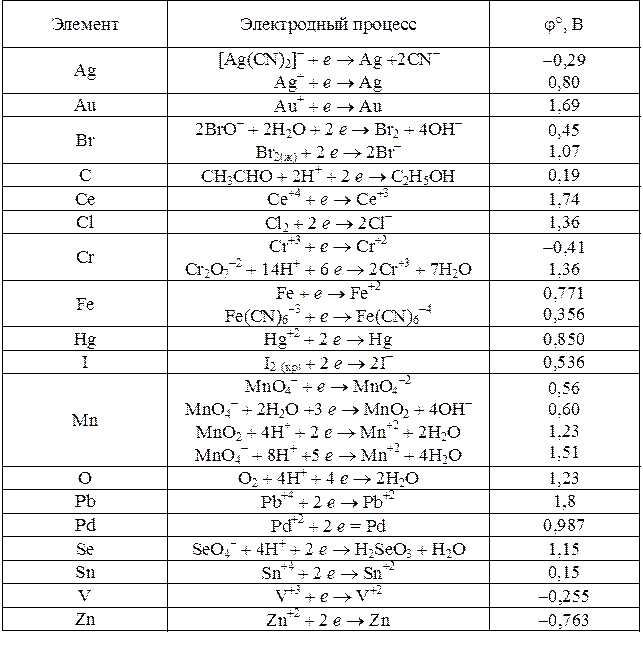
Оглавление
Предисловие 4
Раздел 1. Основные классы неорганических соединений 5
Раздел 2. Основные понятия и законы химии. Эквивалент вещества, закон эквивалентов 18
Раздел 3. Энергетика химических реакций. Химико-термодинамические расчеты 24
Раздел 4. Химическая кинетика 33
Раздел 5. Химическое равновесие 44
Раздел 6. Общие свойства растворов. Способы выражения концентраций растворов. Растворимость. 53
Раздел 7. Электролитическая диссоциация. Свойства растворов электролитов 72
Раздел 8. Ионное произведение воды. Водородный показатель 86
Раздел 9. Обменные реакции в растворах электролитов. Гидролиз солей 96
Раздел 10. Произведение растворимости. Условие образования осадка 110
Раздел 11. Комплексные соединения. Строение, номенклатура, равновесия в растворах 114
Раздел 12. Дисперсные системы. Свойства коллоидных растворов 121
Раздел 13. Окислительно-восстановительные реакции 137
Раздел 14. Общие свойства металлов 149
Раздел 15. Сплавы. Физико-химический анализ 159
Раздел 16. Электродные потенциалы. Химические источники электрической энергии 179
Раздел 17. Электролиз. Законы Фарадея 188
Раздел 18. Коррозия металлов. Методы защиты от коррозии 197
Раздел 19. Основные свойства s-элементов и их важнейших соединений. Жесткость воды 203
Раздел 20. Химия строительных материалов 211
Раздел 21. Органические соединения. Общие представления, классификация, номенклатура 217
Раздел 22. Высокомолекулярные соединения (полимеры) 230
Рекомендуемая литература 236
Приложение 237
Таблица 1. Периодическая система химических элементов д. и. менделеева 237
Таблица 2. Растворимость неорганических веществ в воде 239
Таблица 3. Названия важнейших кислот и их солей 240
Таблица 4. Стандартные энтальпии образования DНо298, энтропии Sо298, и энергии Гиббса DGо298 некоторых веществ при 298 К (25 °С) 242
Таблица 5. Константы и степени диссоциации некоторых слабых электролитов в водных растворах при 25 °С 244
Таблица 6. Произведение растворимости некоторых малорастворимых веществ в воде при 25 °С 245
Таблица 7. Константы нестойкости некоторых комплексных ионов в водных растворах при 25 °С 246
Таблица 8. Стандартные окислительно-восстановительные потенциалы металлов(j°) 247
Таблица 9. Стандартные электродные потенциалы j° в водных растворах при 25 °С 248
Римма Алексеевна Абакумова,
Леонид Иванович Акимов
Наталья Александровна Андреева
Михаил Дмитриевич Бальмаков
Ирина Викторовна Гончарова
Всеволод Владимирович Инчик
Адольф Михайлович Миронов
Денис Адольфович Миронов
Александр Иванович Павлов
Ольга Леонидовна Сувернева
Алевтина Васильевна Ухина
Ольга Михайловна Халина
ХИМИЯ
