Ионно-обменные реакции в растворах электролитов
В разбавленных растворах электролитов (кислот, оснований, солей) между ионами могут протекать химические реакции, не сопровождающиеся изменениями степеней окисления. Они называются реакциями ионного обмена.
Ионно-обменные реакции протекают практически необратимо, если образуются малорастворимые вещества (они выпадают в осадок), легколетучие вещества (они выделяются в виде газа) или малодиссоциирующие вещества – слабые электролиты (в том числе вода), комплексные соединения.
Ионообменные реакции записывают обычно с помощью молекулярного, полного ионного и краткого ионного уравнений. Например, молекулярное уравнение:
Pb(NO3)2 + 2HI = PbI2↓ + 2HNO3;
ионное уравнение:
Pb2++ 2NO3–+ 2H++ 2I– = PbI2↓ + 2H++ 2NO3–;
сокращенное ионное уравнение:
Pb2++ 2I– = PbI2↓.
Ионное произведение воды
Вода – очень слабый электролит, поэтому на ионы диссоциирует в незначительной степени:
Н2О ⇄ Н++ ОН–.
Для данного равновесия на основе закона действия масс, можно записать константу равновесия – константу диссоциации воды (КД):
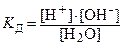 или Кд × [ Н2О] = [Н+] × [ ОН–].
или Кд × [ Н2О] = [Н+] × [ ОН–].
Обозначая Кд × [Н2О] через КВ, получим:
КВ= [Н+]×[ОН–]
КВ– называют ионным произведением воды. При 25 °С КВ= 1·10–14, тогда
| [Н+]×[ОН–] = 1·10–14 | (14) |
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентраций ионов водорода и гидроксид-ионов есть величина постоянная. В чистой воде при 25 оС
[H+] = [ОН–] = 1·10–7моль/л
Раствор, в котором концентрация ионов водорода равна концентрации гидроксид-ионов называют нейтральным. Если концентрация [Н+] > [ОН –], то такой раствор называют кислым. Если концентрация [Н+] < [ОН–], то раствор называют щелочным.
Кислотность или щелочность раствора выражают другим более удобным способом: вместо концентраций ионов водорода [H+] и гидроксид-ионов используют их десятичный логарифм, взятый с обратным знаком:
| рН = – lg [Н+], рОН = – lg [ОН–]. | (15) |
Соответственно,
| рН + рОН = 14. | (16) |
Величина рН называется водородным показателем и для характеристики среды раствора используется чаще:
рН > 7 – среда щелочная;
рН < 7 – среда кислая;
рН ≈ 7 – среда нейтральная.
При использовании величин концентраций часто наблюдается отклонение от закона действующих масс, в основном для сильных электролитов. Поэтому вместо концентраций пользуются активностями электролита (а). Отличие активности электролита от концентрации связано с частичной или полной диссоциацией его молекул на ионы, появлением сил электростатического взаимодействия этих ионов, взаимодействием ионов с молекулами растворителя. Активность связана с концентрацией через коэффициент активности (γ):
| а = С∙ γ | (17) |
Коэффициент активности– работа против сил, вызывающих отклонение свойств раствора от свойств идеальных растворов. Например, рН = –lg aH+.
Установлено, что в малоконцентрированных растворахкоэффициент активности иона определяется только электростатическими взаимодействиями. Следовательно, γ зависит только от концентрации электролита и заряда иона и не зависит от природы электролита. Мерой электростатического взаимодействия является ионная сила раствора (I).
Связь коэффициента активности электролита с ионной силой раствора описывает предельный закон Дебая-Хюккеля:
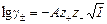 , , |
где А – коэффициент, зависящий от температуры и диэлектрической постоянной растворителя Для воды при 298К А = 0,509. Обычно для приближенных расчетов рассчитывают ионную силу раствора и на основании этого определяют коэффициент активности по справочным данным:
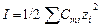 , , | (19) |
Гидролиз солей
Гидролизом соли называется процесс взаимодействия ионов соли с ионами воды с изменением рН среды. Обязательным условием гидролиза является образование малодиссоциированного вещества (слабого электролита).
Качественно реакцию среды определяют с помощью индикаторов. Выделяют четыре типа реакций взаимодействия солей с водой:
1. Соль, образованная ионами сильного основания (катионами) и сильной кислоты (анионами), гидролизу не подвергается. Растворы таких солей имеют нейтральную среду рН ≈ 7.
K2SO4 + H2O ≠
2. Соль, образованная катионами сильного основания и анионами слабой (средней) кислоты, гидролизуется по аниону (рН раствора >7).
KCN + H2O ⇄ KOH + HCN,
ионное уравнение: K++ CN– + H2O ⇄ K++ OH–+ HCN,
сокращенное ионное уравнение CN–+ H2O ⇄ OH–+ HCN.
3. Соль, образованная катионами слабого основания и анионами сильной кислоты, гидролизуется по катиону (рН < 7).
NH4Cl + H2O ⇄ NH4OH + HCl,
ионное уравнение NH4++ Cl–+ H2O ⇄ NH4OH + H++ Cl–,
сокращенное ионное уравнение NH4++ H2O ⇄ NH4OH +H+.
4. Соль, образованная катионами слабого основания и анионами слабой кислоты, гидролизуется полностью до образования слабой кислоты и слабого основания (рН раствора ≈7).
NH4CN + H2O → NH4ОН + HCN.
Гидролиз солей, образованных многозарядными ионами протекает ступенчато. Например, гидролиз фосфата натрия протекает в три ступени:
1-я ступень: Na3PO4 + H2O ⇄ Na2HPO4 + NaOH;
ионное уравнение:
3Na++PO43–+ H2O ⇄ 2Na++ HPO42–+ Na++ OH–;
2-я ступень Na2HPO4 + H2O ⇄ NaH2PO4+ NaOH;
ионное уравнение
2Na++НPO42–+H2O ⇄ Na++ H2PO4–+ Na++OH–;
3-я ступень NaH2PO4+ H2O ⇄ H3PO4+ NaOH;
ионное уравнение
Na+ +Н2PO42- + H2O ⇄ H3PO4 + Na+ + OH–;
Гидролиз хлорида меди протекает в две ступени:
1-я ступень CuCl2 + H2O ⇄ CuOHCl + HCl;
ионное уравнение
Cu2++ 2Cl–+ H2O ⇄ CuOH++ Cl–+ H++ Cl–;
2-я ступень: CuOHCl + H2O ⇄ Cu(OH)2 + HCl;
ионное уравнение
CuOH+ + Cl–+ H2O ⇄ Cu(OH)2 + H+ + Cl–.
При комнатной температуре соли гидролизуются, как правило, только по 1 ступени, за исключением солей, образованных катионом слабого основания и анионом слабой кислоты.
Количественно реакция гидролиза характеризуется степенью гидролиза b и константой гидролиза КГ. Степень гидролиза представляет отношение концентрации гидролизованных молекул к общей концентрации вещества. Степень гидролиза зависит от температуры и концентрации веществ. Константа равновесия реакции гидролиза называется константой гидролиза. Она связана со степенью гидролиза следующим уравнением:
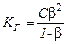 | (20) |
Константа гидролиза связана с ионным произведением воды через константы диссоциации слабых электролитов:
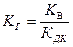 – гидролиз соли, образованной катионами сильного основания и анионами слабой (средней) кислоты; – гидролиз соли, образованной катионами сильного основания и анионами слабой (средней) кислоты; | (21) |
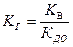 – гидролиз соли, образованной катионами слабого основания и анионами сильной кислоты; – гидролиз соли, образованной катионами слабого основания и анионами сильной кислоты; | (22) |
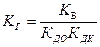 – гидролиз соли, образованной катионами слабого основания и анионами слабой кислоты. – гидролиз соли, образованной катионами слабого основания и анионами слабой кислоты. | (23) |
В уравнениях(8.2.12 – 8.2.14) КДО – константа диссоциации слабого основания, КДК – константа диссоциации слабой кислоты.
