Глава 1. предмет фармацевтической химии. основные понятия. классификация лекарственных средств
СПИСОК СОКРАЩЕНИЙ И УСЛОВНЫХ ОБОЗНАЧЕНИЙ
АПФ - ангиотензинпревращающий фермент
АФК - активные формы кислорода
БАД - биологически активные добавки
БИК - инфракрасная (ИК) спектрометрия в ближнем диапазоне
ВОЗ - Всемирная организация здравоохранения
ВЭЖХ - высокоэффективная жидкостная хроматография
ГСО - государственный стандартный образец
ГФ - Государственная фармакопея
ГХ - газовая хроматография
ДМФА - диметилформамид
ДНК - дезоксирибонуклеиновая кислота
ЕФ - Европейская фармакопея
ИБС - ишемическая болезнь сердца.
ИЮПАК (IUPAC - International Union of Pure and Applied Chemistry) - Международный союз теоретической и прикладной химии
ЛАЛ (LAL - Limulus Amebocite Lisate) - водный экстракт (лизат) амебоцитов мечехвоста полифема
ЛВ - лекарственное вещество
ЛС - лекарственное средство
ЛФ - лекарственная форма
МНН - международное непатентованное название
МФ - Международная фармакопея
НАД - никотинамидадениндинуклеотид
НАДФ - никотинамидадениндинуклеотидфосфат
НД - нормативный документ
НПВС - нестероидные противовоспалительные лекарственные средства
ОФС - общая фармакопейная статья
ПАБК - n-аминобензойная кислота
ПАСК - n-аминосалициловая кислота
ПОЛ - пероксидное окисление липидов
ПСЭ - периодическая система элементов
РНК - рибонуклеиновая кислота
РСО - рабочий стандартный образец
РФП - радиофармацевтические препараты
рКа - отрицательный логарифм константы кислотности Ка
рКb - отрицательный логарифм константы основности Кb
Трилон Б - динатриевая соль этилендиаминтетрауксусной кислоты
ТСХ - хроматография в тонком слое сорбента
УФ - ультрафиолетовый
ФАД - флавинадениннуклеотид
ФВ - фармакопея Великобритании
ФМН - флавинмононуклеотид
ФС - фармакопейная статья
ФСП - фармакопейная статья предприятия
ФЯ - фармакопея Японии
ЦОГ – циклооксигеназа
ЭДТА - этилендиаминтетрацетат
CRS (Chemical Reference Substance) - химическая субстанция, используемая в качестве стандартного образца
GCP (Good Clinical Practice) - надлежащая клиническая практика
GDP (Good Distribution Practice) - надлежащая практика оптовой торговли
GLP (Good Laboratory Practice) - надлежащая лабораторная практика
GMP (Good Manufacturing Practice) - надлежащая производственная практика
GPP (Good Pharmacy Practice) - надлежащая фармацевтическая практика
Mr - относительная молекулярная масса
Ox - окислитель
Pg (ПГ) - простагландины
ppm (parts per million - частей на млн) - единица измерения концентрации, миллионная доля, например мкг/г
QSAR (Quantitative Structure-Activity Relationship) - количественная корреляция структура-активность (ККСА)
Rd - восстановитель
ПРЕДИСЛОВИЕ
Работу по созданию учебника авторы осуществляли в рамках существующей учебной программы. При этом был использован богатый опыт, накопленный фармацевтами многих поколений, нашедший отражение в отечественной и зарубежных фармакопеях, текущей фармацевтической периодике и информационных банках данных по законодательным актам, стандартам, постановлениям. В результате обобщения этих материалов авторы пытались продемонстрировать учащимся всю систему управления качеством за период «жизни» лекарственных средств (ЛС) - от прогноза их создания до реализации в аптеке.
Особенность изложения учебного материала - использование сведений, содержащихся в мировых фармакопеях: Государственной фармакопее РФ (XI, XII, ч. 1), Европы, США, Японии, а также в монографиях и текущей научной периодике. То, что авторы при подготовке учебника использовали зарубежные фармакопеи, вполне оправдано, поскольку отечественная фармакопея в полном объеме не переиздавалась с 1968 г.
Авторы учебника - преподаватели кафедры фармацевтической и токсикологической химии медицинского факультета Российского университета дружбы народов (РУДН) и фармацевтического училища № 10 Департамента здравоохранения г. Москвы (Мосгорздрав):
Плетенева Татьяна Вадимовна - заведующая кафедрой фармацевтической и токсикологической химии РУДН, доктор химических наук, профессор.
Успенская Елена Валерьевна - доцент кафедры фармацевтической и токсикологической химии РУДН, кандидат химических наук.
Мурадова Людмила Ивановна - директор (по 2011 г.) Фармацевтического училища № 10 Департамента здравоохранения г. Москвы; заслуженный работник здравоохранения РФ.
ВВЕДЕНИЕ
В последние десятилетия в фармации произошли значительные изменения, которые в первую очередь обусловлены появлением на отечественном фармацевтическом рынке новых лекарственных средств различных химических классов, внедрением в отечественную фармацию международных стандартов создания лекарственных средств и управления их качеством.
Современную нормативную документацию на лекарственные средства разрабатывают с учетом мировых достижений в области синтеза и анализа лекарственных и вспомогательных веществ. На международных форумах фармацевты постоянно обсуждают проблему гармонизации (согласования) фармакопей разных стран. Объединенная Европа унифицировала действия фармацевтических фирм различных государств при создании и контроле качества лекарственных средств в рамках Европейской фармакопеи (ЕФ). Это особенно важно в эпоху совершенствования аналитического приборостроения. Именно развитие и применение совершенных аналитических методов позволяют осуществлять скрининг химических соединений-«претендентов» и выбор из них наиболее эффективных и безопасных, контролировать в конечном продукте различные примеси, например остаточные органические растворители или токсичные оптические изомеры. Несомненным достижением в этом плане стало внедрение в систему контроля качества лекарственных средств экспресс-метода - ИК-спектрометрии в ближнем диапазоне, которая позволяет на базе спектральных библиотек после соответствующей статистической обработки спектров обнаружить фальсифицированные лекарственные средства без вскрытия упаковки.
Материалы, изложенные в главах учебника, посвящены различным вопросам фармацевтической химии: путям создания новых лекарственных средств, их классификации, государственной системе контроля качества, структуре фармакопейных статей, контролю качества лекарственных средств заводского и аптечного производства.
ГЛАВА 1. ПРЕДМЕТ ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ. ОСНОВНЫЕ ПОНЯТИЯ. КЛАССИФИКАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Фармацевтическая химия - наука о способах получения, свойствах, молекулярно-ионных механизмах биотрансформации лекарственных веществ, а также о методах контроля качества фармацевтических субстанций и лекарственных препаратов.
Фармацевтическая химия - раздел химической науки, она тесно связана с ее отдельными дисциплинами (рис. 1.1). Используя достижения базовых химических дисциплин, фармацевтическая химия решает задачу целенаправленного поиска новых лекарственных средств.
К примеру, современные компьютерные методы позволяют прогнозировать фармакологическое действие (терапевтический эффект) лекарственных средств. В химии сформировалось отдельное направление, связанное с поиском взаимно однозначных соответствий между структурой химического соединения, его свойствами и биологической активностью (метод QSAR или ККСА - количественная корреляция структура-активность).
Взаимосвязь «структура-свойство» можно обнаружить, например, сравнивая величины топологического (показателя, отражающего структуру лекарственного вещества) и терапевтического (отношение летальной дозы к эффективной LD50 /ED50) индексов.
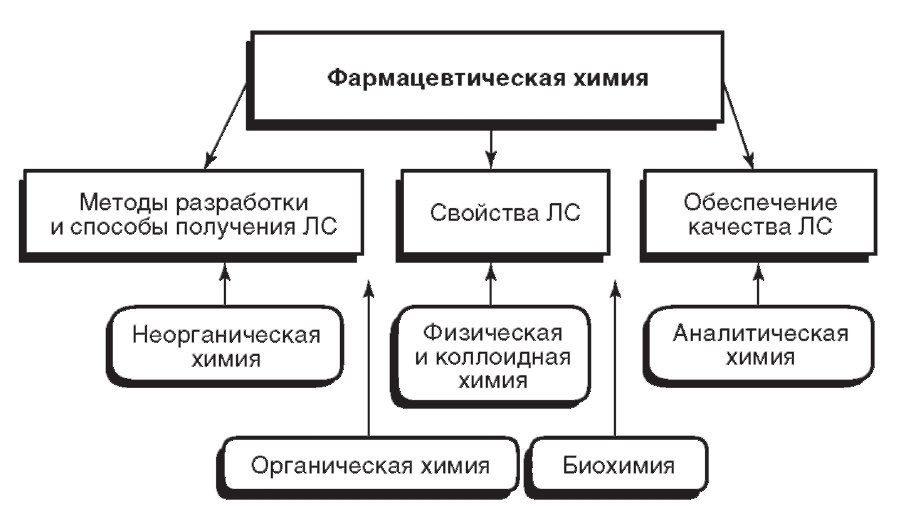
Рис. 1.1. Взаимосвязь фармацевтической химии с другими химическими дисциплинами
Фармацевтическая химия связана с другими естественнонаучными и медико-биологическими дисциплинами (рис. 1.2).
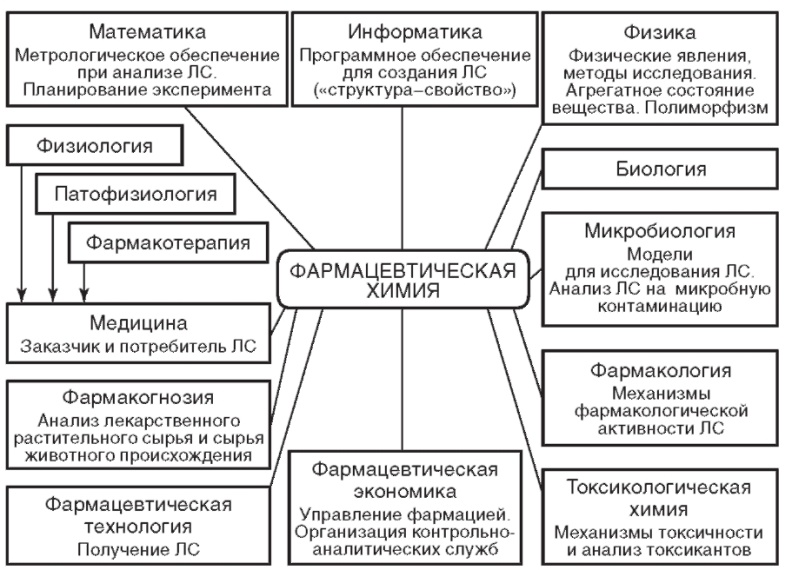
Рис. 1.2. Взаимосвязь фармацевтической химии с естественнонаучными и специальными дисциплинами
Так, знание математики позволяет, в частности, применять метрологическую оценку результатов анализа лекарственных средств (ЛС), а знание физики - использовать фундаментальные законы природы и применять современные приборы при анализе и исследованиях ЛС. Ряд дисциплин медико-биологического профиля - биология, микробиология, физиология, патология - являются основой для понимания метаболизма лекарств.
Очевидна взаимосвязь между фармацевтической химией и специальными дисциплинами. Постоянный контроль (мониторинг) качества реагентов, вспомогательных веществ, промежуточных продуктов, фармацевтических субстанций и готовых лекарственных форм - важная составляющая технологических процессов фармацевтических предприятий.
Фармакогностические исследования не возможны без анализа растительного и других видов природного сырья. Организация фармации использует информацию фармацевтической химии для совершенствования системы стандартизации и контроля качества ЛС. Определение биологически активных соединений и их метаболитов в жидких средах организма (кровь, моча, слюна) во времени (фармакокинетика) позволяет решать задачи фармакологии, к примеру проводить оценку биоэквивалентности дженериковых ЛС их оригинальным аналогам.
Фармацевтическая химия лежит в основе развития нового направления исследования ЛС - фармакогенетики, позволяющей рационализировать применение ЛС с учетом индивидуальной генетической чувствительности.
Тесная взаимосвязь со всеми перечисленными дисциплинами обеспечивает решение современных проблем фармацевтической химии. В конечном счете эти проблемы сводятся к созданию новых, более эффективных и безопасных ЛС и разработке экспрессных и достоверных методов фармацевтического анализа.
В фармацевтической химии применяют общие (используемые и в других химических дисциплинах) и специальные (сугубо фармацевтические) термины. Рассмотрим некоторые из них, наиболее важные для курса фармацевтической химии, термины в соответствии с ОСТ 91500.05.0002-2001 «Государственный информационный стандарт лекарственного средства. Основные положения».
Биодоступность - полнота и скорость всасывания лекарственных веществ (ЛВ), которые характеризуются его количеством, поступившим в организм, после применения лекарственного препарата.
Биоэквивалентность - равенство биодоступности в допустимых пределах одних и тех же лекарственных препаратов, приготовленных разными производителями.
Валидация - оценка и документальное подтверждение соответствия производственного процесса и качества продукции утвержденным требованиям.
Воспроизведенные ЛС (дженерики) - ЛС, поступившие в обращение после истечения срока действия исключительных патентных прав на оригинальные ЛС.
Вспомогательное вещество - относительно индифферентное в химическом и биологическом отношении вещество, разрешенное к медицинскому применению в целях получения лекарственной формы, придания или сохранения определенных свойств лекарственного препарата.
Качество лекарственного препарата - совокупность свойств, которые придают лекарственному препарату способность соответствовать своему назначению и отвечают требованиям, установленным стандартом.
Лекарственная форма - состояние, придаваемое ЛС или лекарственному растительному сырью, удобное для применения, обеспечивающее необходимый лечебный эффект.
Лекарственное (фармацевтическое) сырье - ЛС, лекарственное растительное сырье, вспомогательные вещества, разрешенные к медицинскому применению для производства лекарственных препаратов или другой фармацевтической продукции или полуфабрикатов. Фактически понятие «сырье» включает все исходные материалы, поступающие в производство для переработки с целью получения готового продукта или полуфабриката.
Лекарственные средства - вещества, применяемые для профилактики, диагностики и лечения болезни, предотвращения беременности, полученные из крови, плазмы крови, а также органов, тканей человека или животного, растений, микроорганизмов, минералов методами синтеза или с применением биологических технологий.
Лекарственные препараты - дозированные ЛС в определенной лекарственной форме, готовые к применению.
В зарубежной литературе иногда используют термин «фармацевтические (или лекарственные) продукты». Это связано с тем, что около 95% ЛС представляют собой лекарственные формы промышленного производства. Таким образом, можно отличить
готовые промышленные формы от лекарственных субстанций и ЛС, изготовленных в аптеках.
Наркотическое средство - ядовитое или сильнодействующее ЛС, требующее ограниченного применения и отнесенное к наркотическим в соответствии с законодательством. Наркотические средства реализуют по особым правилам, установленным Министерством здравоохранения и социального развития РФ.
Психотропные вещества - вещества, включенные в перечень, составленный и обновляемый в соответствии с Конвенцией о психотропных веществах 1971 г. и законодательством РФ.
Патентованные лекарственные средства - ЛС, право на производство и продажу которых охраняется патентным законодательством РФ.
Незаконные копии лекарственных средств - ЛС, поступившие в обращение с нарушением патентного законодательства РФ.
Оригинальные лекарственные средства - ЛС, поступившие в обращение с зарегистрированными собственными названиями.
Радиоактивное средство - ЛС, применяемое в медицинской практике в связи с его способностью к ионизирующему излучению.
Сертификат - письменное свидетельство (гарантия) того, что качество ЛС (эффективность, безопасность) отвечает установленным требованиям спецификаций, а производственный процесс - правилам GMP.
Сертификация лекарственных средств - процесс компетентного подтверждения специально аккредитованными органами безопасности и соответствия качества ЛС требованиям нормативных документов (НД).
Сильнодействующее средство - ЛС с высокой биологической активностью, прописывание, отпуск, хранение и учет которого производятся по особым правилам, установленным Минздравом России.
Срок годности - утвержденное законодательным органом на основании результатов специальных исследований время хранения ЛС (препарата), в течение которого оно сохраняет свои физико-химические, микробиологические и терапевтические свойства без изменений или в установленных для них пределах при условии соблюдения условий хранения.
Стабильность - способность ЛС (препарата) сохранять свои физико-химические и микробиологические свойства в течение определенного времени с момента его выпуска.
Фармакопейная статья - нормативный документ, который определяет состав, упаковку, срок годности и требования к качеству лекарственного препарата (лекарственной субстанции или вспомогательного вещества) и имеет статус государственного стандарта.
Ядовитое средство - ЛС с очень высокой биологической активностью, прописывание, отпуск, хранение и учет которого производятся по особым правилам, установленным Минздравом России.
К сожалению, иногда в НД встречаются устаревшие термины, не соответствующие правилам ИЮПАК. Например, натрия гидроксид называется «едкий натр», пероксид - «перекись», дисульфит (пиросульфит) - «метабисульфит». Следует иметь в виду, что гидросульфит NaHSO3 в фармацевтической литературе называют иногда устаревшим термином «метабисульфит» (Na2S2O5).
В фармакопейных статьях при характеристике растворимости ЛВ ошибочно применяют термин «медленно растворимый». Следует помнить, что этот термин характеризует не степень растворимости (в системе «раствор ЛВ - твердое ЛВ» устанавливается динамическое равновесие - термодинамическая характеристика), а скорость растворения (кинетическая характеристика).
Кроме того, не только в химии, но и в дисциплинах медико-биологического профиля (фармакология, токсикология) давно осуществлен переход на международную систему единиц измерения. В частности, доза препарата выражается не в единицах массы, а отношением количества вещества к единице массы тела (моль/кг). Концентрация ЛС, значения его биоэквивалентности также должны быть представлены с использованием единиц количества вещества (моль) или их производных (ммоль, мкмоль). В противном случае не представляется возможным сравнивать биологические активности различных веществ.
Этих ошибок удастся избежать, осуществляя подготовку НД в строгом соответствии с международными требованиями к терминологии и единицам измерения.
Известно несколько типов классификации ЛС. Среди них для фармацевтической химии важна химическая классификация, согласно которой вещества объединены в группы в соответствии с их химической природой. При химической классификации рассматривают два больших класса: ЛС неорганической и органической природы.
Фармакологическая классификация ЛС отражает преимущественное действие препарата на ту или иную систему организма (сердечно-сосудистую, нервную и т.д.). Внутри групп фармакологической классификации препаратов может рассматриваться фармакотерапевтическая классификация - лекарственные препараты группируют в зависимости от применения для лечения определенного заболевания (противомикробные, противовирусные препараты, снотворные, гипотензивные, кардиотонические, местноанестезирующие, анальгезирующие средства и т.д.).
