Методы определения дзета-потенциала
Все электрокинетические явления зависят от величины и знака дзета–потенциала. Проводя электроосмотические или электрофоретические измерения, можно определить величину дзета–потенциала.
Не останавливаясь на методике измерения, приведем конечные уравнения, связывающие дзета-потенциал со скоростью электроосмотического или электрофоретического переноса:
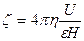 , B (8 1)
, B (8 1)
где 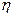 – динамическая вязкость дисперсионной среды;
– динамическая вязкость дисперсионной среды; 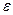 – абсолютная диэлектрическая проницаемость среды; U – скорость электрофоретического переноса (на основании измерений); Н – градиент потенциала внешнего поля, равный Е/l (Е – разность электродных потенциалов, l – расстояние между ними).
– абсолютная диэлектрическая проницаемость среды; U – скорость электрофоретического переноса (на основании измерений); Н – градиент потенциала внешнего поля, равный Е/l (Е – разность электродных потенциалов, l – расстояние между ними).
Для электроосмотического метода:
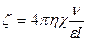 , B (8 2)
, B (8 2)
где 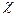 – удельная электрическая проводимость золя;
– удельная электрическая проводимость золя; 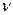 – объемная скорость, т.е. объем жидкости, перенесенной через пористую мембрану за единицу времени; I – сила тока, при которой проводился осмос.
– объемная скорость, т.е. объем жидкости, перенесенной через пористую мембрану за единицу времени; I – сила тока, при которой проводился осмос.
ЗАКЛЮЧЕНИЕ
Поверхность твердых частиц, находящихся в жидкой дисперсионной среде, приобретает электрический заряд в результате преимущественной адсорбции одного из ионов электролита либо диссоциации поверхностных ионогенных групп. Независимо от механизма возникновения заряда на коллоидной частице возникает двойной электрический слой (ДЭС), состоящий из ионов на поверхности ( потенциалопределяющих ионов) и из компенсирующих заряд поверхности ионов (противоионов) в растворе; причем часть противоионов находится в прилегающем к поверхности и прочно связанном с ней адсорбционном слое, а другая часть – в диффузном слое, удаленном от поверхности. Частицу дисперсной фазы вместе с ДЭС называют мицеллой; мицелла является нейтральной.
При движении частицы в растворе происходит разрыв мицеллы на две части: твердую частицу с противоионами адсорбционного слоя, называемую коллоидной частицей, и противоионы диффузного слоя. Границу, по которой происходит разрыв мицеллы, называют границей скольжения. Плоскость скольжения, как правило, не совпадает с границей, разделяющей адсорбционный и диффузный слои, а несколько смещена от нее в сторону раствора. Электрический потенциал на плоскости скольжения называется электрокинетическим или дзета-потенциалом, который отличается от термодинамического потенциала 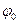 , который определяется зарядом поверхности.
, который определяется зарядом поверхности.
Наличием на частицах дисперсной фазы ДЭС обусловлены электрокинетические явления: электроосмос, электрофорез, потенциал течения и потенциал седиментации.
Интенсивность всех электрокинетических явлений определяется значением дзета-потенциала. Экспериментальное определение скорости переноса в электрическом поле дисперсионной среды (электроосмос) или дисперсной фазы (электрофорез) позволяет определить значение дзета-потенциала.
Введение в золь растворов электролитов приводит к изменению строения ДЭС и, как следствие, значения дзета–потенциала.
В зависимости от природы и концентрации электролита может происходить:
• сжатие ДЭС и уменьшение абсолютной величины дзета–потенциала;
• увеличение абсолютных величин термодинамического и дзета–потенциала;
• перезарядка поверхности частицы.
Значение дзета–потенциала зависит также от величины рН, температуры и природы дисперсионной среды.
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1. Какие вы знаете пути образования ДЭС?
2. Каково строение двойного электрического слоя?
3. В чем состоит отличие электрокинетического потенциала от термодинамического?
4. Какие вы знаете электрокинетические явления? В чем состоит сущность каждого из них?
5. Как экспериментально определяют величину дзета–потенциала?
5. В чем состоят различия неиндифферентного и индифферентного электролитов?
6. Каково строение мицеллы лиофобного золя?
7. В каких случаях при добавлении электролитов происходит перезарядка коллоидной частицы?
8. Напишите формулы мицелл следующих золей:
а) золя карбоната бария ВаСО3, стабилизированного хлоридом бария;
б) золя сульфида свинца PbS, стабилизированного сульфидом натрия;
в) золя бромида серебра AgBr, стабилизированного нитратом серебра;
г) золя гидроксида железа Fe(OH)3, стабилизированного Fe(NO3)3;
д) золя хлорида свинца РЬС12, стабилизированного хлоридом калия;
е) золя сульфата бария BaSO4, стабилизированного сульфатом калия.
10. Как изменится строение ДЭС и величина дзета-потенциала, если к золю, указанному в пункте д), прибавить:
а) нитрат натрия;
б) эквивалентное количество РЬ(NО3)2;
в) избыток Pb(NO3)2;
г) иодид натрия;
д) избыток А1(NO3)3.
Закончив изучение главы 8, вы должны
1) знать:
• основные положения теории строения ДЭС;
• электрокинетические явления;
• влияние электролитов на строение ДЭС и величину дзета-потенциала;
2) уметь;
• составлять формулы мицелл лиофобных золей;
• предсказывать изменения строения ДЭС и величины дзета-потенциала при действии электролитов,
• изменении концентрации золя и природы дисперсионной среды.
ГЛАВА 9
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ
