Тема 2.9. Сполуки Сульфуру
План
1. Сірководень.**
2. Сульфур (IV) оксид.**
3. Сульфур (VI) оксид.**
1. Сірководень – речовина молекулярної будови.
Молекулярна формула – H2S
Електронна формула 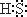
Уприроді сірководень утворюється внаслідок гниття органічних решток. Виділяється під час гниття яєчного білка. Міститься у вулканічних газах і водах мінеральних джерел.
Фізичні властивості: Сірководень – безбарвний газ із неприємнним гнилосним запахом, трохи важчий за повітря, розчинний у воді. Розчин називають сульфідною кислотою. Дуже отруйний. Вибухонебезпечний.
Хімічні властивості:
Сірководень сильний відновник.
1) На повітрі він горить блакитним полум’ям:
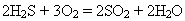
У разі неповного згоряння утворюється сірка:
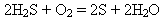
2) Взаємодіє з неметалами:
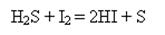
3) Взаємодіє із сріблом, тому срібні предмети з часом темнішають:
4Ag + 2H2S + O2 = 2Ag2S + 2H2O
Водний розчин сірководню – слабка двохосновна кислота:
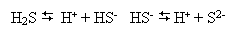
Добування. У лабораторних умовах:
а) повільно пропускають водень у пробірку з киплячою рідкою сіркою:
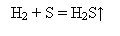
б) в апараті Кіппа дією хлоридної кислоти на ферум (ІІ) сульфід:
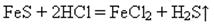
Застосування: 1) для добування сірки, сульфатної кислоти, сульфідів і важкої води;
2) як робочу речовину газових лазерів;
3) для приготування лікувальних сірководневих ванн.
2.Сульфур (IV) оксид
 Молекулярна формула – SO2.
Молекулярна формула – SO2.
Атоми в молекулі зв’язані ковалентними полярними зв’язками, що утворюють кут 120º.
Ступінь окиснення Сульфуру +4: S+4O2-2
Фізичні властивості: безбарвний газ із різким запахом, що викликає кашель, у 2,2 рази важчий за повітря, дуже легко розчиняється у воді (в 1 л води при 20ºC - 49 л оксиду).
Хімічні властивості:
1) Сульфур (IV) оксид - кислотний оксид:
· взаємодіє з основними оксидами і лугами:
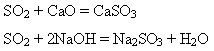
· взаємодіє з водою:
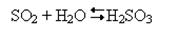
2) За наявності каталізатора приєднує кисень:
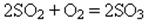
3) За наявності сильних відновників виявляє властивості окисника:
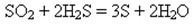
Добування. У лабораторних умовах:
а) дією хлоридної або сульфатної кислоти на сульфіти:
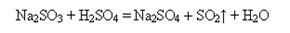
б) взаємодією концентрованої сульфатної кислоти з міддю під час нагрівання;
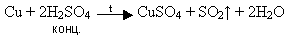
У промисловості – прожарюванням цинк сульфіду:
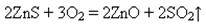
або прожарюванням піриту (залізного колчедану), який можна розглядати як ферум (ІІ) сульфід, що містить вільну сірку – Fe=S, S:
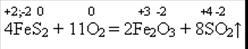
Застосування:для добування сульфатної кислоти; вибілювання соломи, вовни, шовку; як дезинфікуючий засіб.
3.Сульфур (VI) оксид
Молек  улярна формула – SO3.
улярна формула – SO3.
Атоми в молекулі зв’язані ковалентними полярними зв’язками. Молекула має будову площинного трикутника з кутом між зв’язками 120º.
Фізичні властивості: безбарвна рідина з температурою кипіння 45ºC. За температури, нижчої від 17ºC кристалізується, перетворюючись на довгі шовковисті кристали. Дуже летка речовина, токсична, уражує слизові оболонки й дихальні шляхи, викликає тяжкі опіки, руйнує органічні сполуки. Зберігають у запаяних скляних посудинах (ампулах).
Хімічні властивості:
Виявляє загальні властивості, що характерні для кислотних оксидів:
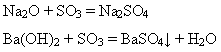
Сульфур (VI) оксид – на повітря димить, вбираючи вологу з повітря, бурхливо взаємодіє з водою:
SO3 + H2O = H2SO4
Виявляє сильні окисні властивості, відновлюючись зазвичай до сульфур (IV) оксиду:
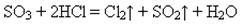
Добування. У промисловості:
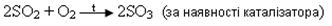
Контрольні запитання:
1. Які ступені окиснення характерні для Сульфуру?
2. Які фізичні і хімічні властивості характерні для сірководню?
3. Які оксиди утворює Сульфур? Охарактеризуйте їх.
4. Як в промисловості добувають сірководень, оксиди Сульфуру?Напишить рівняння відповідних реакцій.
5. Де використовуються сірководень, оксиди Сульфуру?
6. Яка сіль і якої масу утворюється при додаванні 4г натрій гідроксиду до розчину сульфатної кислоти масою 98г з масовою часткою кислоти 10%.
Література:
1. Данильченко В.Є., Фрадіна Н.В. Хімія. 10 – 11 класи: Навч. посібник. – Х.: Країна мрій™, 2003. - с. 6.
2. Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. ІІ, Гл. 9, §§ 75-76, с. 89-91.
3. Стахеєв О.Ю. Хімія. Узагальнюючі схеми і таблиці. – Тернопіль.: «Богдан», 1998. – с. 25.
