Взаимодействие пропилена и метана с хлором относятся соответственно к реакциям
1) обмена и замещения ; 2) присоединения и замещения
3) обмена и присоединения ; 4) замещения и присоединения
Коэффициент перед формулой окислителя в уравнении реакции, схема которой
S + HNO3 ® H2 SО4 + NО, равен
1) 1 2) 2 3) 3 4) 4
Слабым электролитом является
1) гидроксид бария ; 2) хлорид кальция ; 3) соляная кислота ; 4) угольная кислота
8. Сумма всех коэффициентов в полном и сокращенном ионных уравнениях реакции между муравьиной кислотой и гидроксидом калия равна
1) 10 и 3 2) 6 и 4 3) 7 и 3 4) 12 и 4
Сокращенное ионное уравнение реакции
2H+ + СO 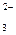 = CO2 + Н2О соответствует взаимодействию
= CO2 + Н2О соответствует взаимодействию
1) соляной кислоты с карбонатом магния
2) сероводородной кислоты с карбонатом калия
3) серной кислоты с карбонатом калия
4) азотной кислоты с оксидом углерода (IV)
Оксид серы (IV) реагирует с обоими веществами
1) железо и гидроксид ватрия
2) оксид кальция и оксид углерода (IV)
3) кислород и вода
4) хлорид натрия и оксид азота (V)
11. Сложный эфир можно получить при взаимодействии
1) C2H5OH с C2H5OH
2) CH3COOH с Na2CO3
3) СН2 = СН2 с НСl
4) СНзСООН с C2H5OH
Реакция гидролиза характерна для
1) жиров ; 2) кислот ; многоатомных спиртов ; 4) щелочей
В схеме превращений
X Y
этилацетат ® ацетат натрия ® уксусная кислота
Формулы веществ Х и Y
1) Х — H2O; Y — Н2 SO4 ; 2) Х — H2O; Y — С2Н5OH
3) Х — NaOH; Y — Н2 SO4 ; 4) X — NaOH; Y — CH3COOH
Присутствие в водном растворе гидроксида кальция можно доказать с помощью
1) лакмуса и соляной кислоты ; 2) лакмуса и углекислого газа
3) фенолфталеина и хлороводорода ; 4) фенолфталеина и аммиака
Цветную реакцию на фенол дает раствор
1) хлорида железа (III) ; 2) гидроксида кальция
3) сульфата меди (II) ; 4) хлорида бария
16. С наибольшей скоростью при комнатной температуре протекает реакция 1) С2Н5OH c Na ; 2) О2 с Н2 ; 3) Fе с H2SO4 (р-р) ; FeSO4 (р-р) с NaOH (р-р)
Химическое равновесие в системе
С4Н8 (г) + Н2 (г) Û С4Н10 (г) + Q можно сместить в сторону исходных веществ при
1) понижении температуры ; 2) повышении температуры
3) повышении давления ; 4) использовании катализатора
18.Метилацетат можно получить при взаимодействии
1) метанола с муравьиной кислотой ; 2) этанола с муравьиной кислотой
3) метанола с уксусной кислотой ; 4) этанола с уксусной кислотой
19. Для одностадийного способа получения уксусной кислоты в промышленности используют
1) ацетальдегид; 2) ацетилен ; 3) этиламин ; 4) бромэтан
Гомолог гексана
1) С6Н14 ; 2) С7Н16 ; 3) С6Н6 ; 4) С7Н14
Изомерами являются
1) формальдегид и муравьиная кислота ; 2) этанол и уксусная кислота
3) бензол и фенол ; 4) пентан и диметилпропан
22. Для нейтрализации 200г 9% -ного раствора уксусной кислоты потребуется гидроксид натрия массой
1) 6,9г 2) 9,0г 3) 12,0г 4) 15,0г
При смешивании 5,9г аммиака с 5,6л (н.у.) хлороводорода образуется хлорид аммония массой
1) 5,0г 2) 5,6г 3) 13,4г 4) 15,7г
24. Для синтеза 30кг муравьиной кислоты окислением метана (при выходе продукта 90% ) потребуется метан объемом (н.у.)
1) 13,15м3 2) 14,6м3 3) 16,2м3 4)22,4м3
Ответы к тестам
Ответы к тестам
1.Тест по теме: «Первоначальные химические понятия»
| б | ||||||||||||||||||||
| в | в | абв | вг | бв | в | а | г | в | б | б | а | в | б | в | аг | б | в | б | в | |
| б | г | бвг | аб | аг | б | в | а | б | в | в | в | в | б | б | бв | а | б | в | а |
2.Тест по теме: «Кислород. Водород»
| ав | в | а | б | в | в | б | г | в | а | в | г | в | в | в | ав | б | аб | а | б | |
| ав | а | в | б | а | в | бг | б | б | в | в | в | б | б | б | ав | а | ав | б | в |
3.Тест по теме: «Основные классы неорганических веществ»
| б | бг | аб | бд | в | б | б | бв | в | аб | а | б | |
| в | бг | вг | г | б | б | в | в | в | аг | б | в |
4.Тест по теме: «Периодический закон и периодическая система химических элементов Д.И. Менделеева
| г | г | а | г | б | г | в | а | в | г | 2,6 | |
| а | г | г | г | в | в | в | б | в | г | 3,6 | |
| б | б | в | в | г | б | б | а | б | в | 4,48 | |
| а | в | б | б | аб | в | а | а | б | а | 5,3 | |
| а | г | г | б | б | в | г | б | б | в | ||
| в | а | а | б | г | б | б | в | г | в | 6,7 | |
| в | в | г | а | в | в | в | г | в | г | 4,1 | |
| б | г | г | в | б | в | Zn | в | в | а | 2,24 | |
| б | б | б | б | в | в | в | б | в | г | 7,1 | |
| г | г | б | в | в | г | в | в | в | в |
5.Тест по теме: «Типы химической связи. Степень окисления. Окислительно - восстановительные реакции»
| а | ||||||||||||||||
| б | б | г | г | б | в | в | а | б | б | а | а | а | а | б | а | |
| г | г | а | а | а | а | б | а | г | б | б | б | аб | б | аб | б |
6.Тест по теме: «Теория электролитической диссоциации»
| а | б | г | д | в | б | а | а | в | г | б | в | б | г | б | в | |
| в | в | в | в | а | а | б | г | г | д | в | а | б | г | в | а |
7.Тест по теме: «Галогены»
| в | в | а | аб | в | в | 11,5 | в | б | ||
| б | г | г | - | 4,48 | г | в | 12,4 | в | в | |
| б | г | а | в | 33,9 | б | в | 13,3 | а | б | |
| б | в | а | в | 6,1 | в | а | 6,6 | а | в |
8.Тест по теме: «Подгруппа кислорода»
| б | в | в | г | в | в | б | 1,12 | |
| г | а | г | б | в | б | в | 3,36 | |
| а | в | в | г | а | в | а | 2,24 |
9.Тест по теме: «Азот. Фосфор»
| ав | в | г | б | в | г | б | а | г | г | б | |
| г | в | а | г | в | г | г | б | в | г | в | |
| ав | а | а | в | а | бг | а | б | г | в | б | |
| б | д | б | в | г | в | б | б | б | в | а | |
| а | Г | г | б | а | в | б | а | б | г | в |
10.Тест по теме: «Углерод. Кремний»
| г | б | в | г | а | в | б | в | г | а | а | а | в | г | г | б | |
| а | г | в | в | а | б | в | б | г | б | г | а | г | в | в | б |
11.Тест по теме: «Металлы»
| в | г | в | в | б | в | в | б | 554,3 | ||
| в | а | в | а | ав | г | г | г | бг | 4,8 | |
| в | б | г | бвг | б | а | в | а | в | 147,1 | |
| г | в | б | б | г | г | вг | в | г | 3,7 | |
| б | в | в | ав | б | а | бв | а | г | 112,1 |
