Закономерности поглощения света веществом
Свет или оптическое излучение представляет собой плоскопоперечные волны электромагнитного поля, распространяющиеся перпендикулярно направлению электрического и магнитного полей.
Основными характеристиками светового излучения являются:
- частота колебаний (величина, равная числу полных колебаний напряженности электромагнитного поля, совершаемых за одну секунду);
- длина волны (расстояние, на которое распространяется в данной среде фронт монохроматической световой волны за один период световых колебаний);
- волновое число (величина, обратная длине волны).
Различают разные спектральные области оптического излучения: инфракрасную (ИК) – от 750 до 2500 нм, видимую – от 400 до 750 нм и ультрафиолетовую (УФ) – от 2 до 400 нм. В УФ-области спектра выделяют следующие диапазоны: вакуумный (ВУФ) – 2-200 нм, коротковолновый (КУФ) – 200-280 нм, средневолновый (СУФ) – 280-315 нм и длинноволновый ультрафиолет (ДУФ) – 315-400 нм.
Оптические методы исследования предполагают изучение взаимодействия электромагнитного излучения с веществом во всем диапазоне электромагнитного спектра, поддающемся измерению. В различных областях этого диапазона используются различные физические явления, дающие возможность регистрировать энергетические изменения до и после взаимодействия излучения с исследуемым веществом.
Энергетическое состояние атома характеризуется энергией электронов, входящих в его состав, которая может принимать ряд дискретных значений, переход между которыми характеризуется изменением энергии на величину
E=ђν,
где ђ – постоянная Планка; ν – частота перехода.
Энергетическое состояние молекулы зависит не только от энергии электронов, но и от взаимного расположения атомов, входящих в состав молекулы.
Каждый электрон в молекуле находится на определенной орбитали и обладает определенной энергией. Таким образом, в молекуле существует система электронных энергетических уровней (рис. 5). Для химических и оптических свойств молекулы наиболее важны два уровня: это верхняя (по энергии) заполненная молекулярная орбиталь (ВЗМО) и нижняя свободная молекулярная орбиталь (НСМО). Значение энергии ВЗМО определяет потенциал ионизации молекулы, характеризующую способность отдавать электрон (донорные свойства). Потенциалом ионизации называют энергию, которую необходимо затратить, чтобы оторвать электрон от молекулы. Чем выше энергия ВЗМО, тем ниже потенциал ионизации молекулы и тем лучший она донор электронов. Например, высоким значением энергии ВЗМО обладает витамин Е, который поэтому легко отдает электрон в реакциях со свободными радикалами, что и обуславливает его антиоксидантные свойства.
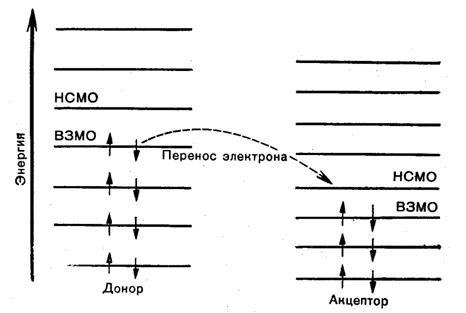
Рис.5. Схема электронных молекулярных энергетических уровней и переноса электрона между двумя различными молекулами.
Стрелками обозначены спины электронов.
Энергия НСМО определяет акцепторные свойства молекулы: чем ниже НСМО, тем охотнее данная молекула присоединяет электрон. Количественно акцепторные свойства характеризуются электронным сродством, которое равно количеству энергии, освобождающейся при перенесении свободного электрона из бесконечности на незанятую электронную орбиталь.
Окислительно-восстановительная реакция между донором и акцептором будет происходить, если энергия ВЗМО донора выше энергии НСМО акцептора (см. рис.5). Следует, однако, помнить, что перенос одного, а тем более двух электронов сопровождается перестройкой в молекуле (изменение энергии уровней, включая ВЗМО и НСМО). Поэтому редокс-потенциал не вполне точно коррелирует с донорно-акцепторными свойствами молекул.
На каждом заполненном энергетическом уровне могут находиться только два электрона, имеющие противоположные собственные магнитные моменты (спины). Если молекуле сообщить энергию, например в форме кванта света, то произойдет переход одного электрона с заполненного уровня (обозначаемого в спектроскопии S0, рис.6) на один из незаполненных уровней. Молекула при этом окажется в электронно-возбужденном состоянии. Уровни S0, S1…… Sn, называются синглетными, при переходах между ними спин электрона не меняется. Время жизни молекул в состоянии S1 составляет 10-8-10-9 с. Именно на уровне S1 решается дальнейшая судьба всех возбужденных молекул. С определенной вероятностью могут реализоваться следующие пути превращения энергии состояния S1: 1) в тепло; 2) испускание кванта флюоресценции; 3) фотохимическая реакция; 4) передача энергии возбуждения другой молекуле; 5) обращение спина электрона и переход молекулы в триплетное возбужденное состояние Т1. Переход из триплетного состояния в основное запрещен, так как спины электронов одинаковы. Поэтому в состоянии Т1 молекула находится значительно дольше (10-4-10 с).
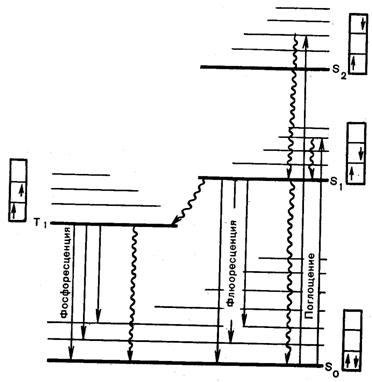
Рис. 6. Электронные переходы в биомолекулах.
Прямые стрелки – поглощательные и излучательные переходы. Жирные горизонтальные линии – «чисто» электронные уровни энергии; тонкие – колебательные подуровни. Около каждого уровня в клетках (соответствующих разным орбиталям) показано направление спина возбужденного электрона по отношению к спину оставшегося электрона.
Существует несколько путей растраты энергии из триплетного (Т1) состояния молекулы: 1) безизлучательный переход в S0 с обращением спина; 2) испускание кванта фосфоресценции; 3) фотохимическая реакция; 4) передача энергии возбуждения другой молекуле (см. рис. 6).
Общее название любых излучательных переходов в молекуле (флюоресценции, фосфоресценции) – люминесценция.
Спектрофотометрия
Способность молекул поглощать свет лежит в основе спектрофотометрии, широко используемой в биологии для качественного и количественного анализа и для выяснения химической структуры веществ. Поглощение света проявляется в ослаблении светового потока после прохождения через исследуемый объект, и оно тем больше, чем выше концентрация вещества (с, моль/л), толщина раствора (l, см) и способность вещества к поглощению. Для монохроматического света эти закономерности выражаются законом Бугера-Ламберта-Бера: если интенсивность падающего светового потока равна I0, то интенсивность света после поглощения слоем вещества I будет равняться
I=I0e-εcl,
где ε (л/моль∙см) — молярный коэффициент экстинкции (поглощения).
Коэффициент экстинкции характеризует способность молекул вещества поглощать свет определенной длины волны и определяется структурными особенностями молекул данного вещества.
Регистрация абсолютного значения интенсивности света связана с большими погрешностями. Поэтому обычно используют относительные величины. Светопропускание (Т) – это выраженная в процентах величина, равная отношению интенсивности света, вышедшего из образца, к интенсивности света, падающего на него:
Т=I/I0
В случае выполнения закона Бугера-Ламберта-Бера:
Т= e-εcl
Таким образом, светопропускание связано с концентрацией вещества экспоненциальной зависимостью, что не очень удобно. Поэтому чаще используют величину, называемую оптическая плотность (D):
D= lgT = lgI/I0= εcl
Если заменить десятичный логарифм на натуральный и концентрацию выражать в числе молекул в одном мл, то вместо ε используют поперечное сечение поглощения s (см2), связанное с ε соотношением: s = 3,8∙10-21ε. Физический смысл s – эффективное сечение молекулы, при попадании в которое происходит поглощение фотона данной длины волны.
Закон Бугера-Ламберта-Бера выведен для достаточно разбавленных растворов при использовании монохроматического света. При высоких концентрациях вещества регистрируемая оптическая плотность будет ниже теоретической, что объясняется экранированием молекул друг другом. Кроме того, значительные отклонения от закона могут быть обусловлены:
- свойствами анализируемого образца - способностью молекул вещества при больших концентрациях образовывать агрегаты, что приводит к росту светорассеяния и кажущемуся повышению его оптической плотности;
- конструкцией прибора - использование немонохроматического пучка света, работа в области, где высока погрешность прибора.
Графики, выражающие зависимость D, ε или s от длины волны, называют спектрами поглощения.
В биологии часто измеряют спектры поглощения не растворов, а мутных суспензий биологических частиц: эритроцитов, митохондрий, микроорганизмов. В таких оптически неоднородных средах наблюдается значительное светорассеивание и обусловленное этим кажущееся увеличение оптической плотности:
Dизмерения =Dпоглощения + Dрассеяния
На многих специально сконструированных для измерения мутных образцов спектрофотометрах поправка на Dрассеяния вводится автоматически. Чаще всего с этой целью кюветы помещают в интегрирующую сферу, собирающую рассеянный свет на фотоприемник.
Поглощение света осуществляется не всей молекулой, а определенными ее участками. Хромофоры - это отдельные группы атомов в молекуле вещества, поглощающие кванты света в УФ- и видимой областях спектра. Поглощение видимого и ультрафиолетового света происходит, главным образом с участием π и n-электронов (π→π* и n→ π*-переходы). Чем длиннее система сопряженных двойных связей в молекуле, то есть чем сильнее делокализованы по молекуле π-электроны, тем при большей длине волны располагается самый длинноволновый максимум поглощения (рис.7).
Простые белки (то есть состоящие только из полипептидной цепи и не содержащие простетической группы) в видимой области свет не поглощают. Основными их хромофорами в ультрафиолетовой области являются пептидные группы, ароматические аминокислоты (тирозин, триптофан, фенилаланин) с максимумом поглощения между 275 и 285 нм и цистеин. Из всех ароматических аминокислот наиболее значительным поглощением обладает триптофан. Знание молярных коэффициентов поглощения для разных белков оказывается полезным при фотометрическом определении их концентрации в растворе.
Хромофоры нуклеиновых кислот - пуриновые и пиримидиновые азотистые основания (аденин, гуанин, тимин, цитозин и урацил) - также поглощают свет только в УФ-области.
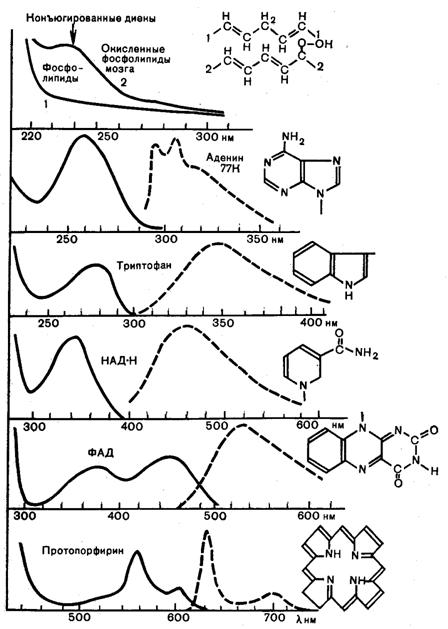
Рис.7. Спектры поглощения и флюоресценции некоторых биологически важных соединений (структурные формулы хромофоров этих молекул приведены рядом со спектрами).
Сплошные кривые – оптическая плотность; пунктирные кривые – интенсивность флюоресценции.
Хромофорами гемопротеинов в видимой области является гем. Так, благодаря железопорфирину в составе гембелка, раствор оксигемоглобина обнаруживает несколько максимумов поглощения в этой области спектра: самый значительный (интенсивный) в области 412-414 нм (полоса Соре) и максимумы меньшей интенсивности при 542 и 578 нм.
С помощью спектральных методов, измеряя оптическую плотность, можно получить следующую информацию:
- рассчитать концентрацию вещества в растворе (используя линейную зависимость оптической плотности от концентрации или по калибровочной прямой) - этот метод часто используют для определения концентрации различных белков, липидов, витаминов, для расчета активности ферментов;
- построить спектр поглощения вещества (зависимость его оптической плотности от длины волны). Спектр поглощения является характеристикой вещества, таким образом, по спектру поглощения можно определить, какое вещество (или класс веществ) находится в растворе;
- изменение структуры биополимеров отражается на их спектрах, следовательно, анализируя спектр поглощения, можно делать выводы о структурном состоянии биомолекул.
Спектральные приборы
Спектрофотометрический метод, то есть изучение оптических характеристик биологических веществ, построение спектров их поглощения - один из наиболее распространенных методов исследования в биологии.
В биологических исследованиях чаще всего используются спектрофотометры (СФ) и фотоэлектроколориметры (ФЭК). Для выделения участка спектра или отдельных длин волн в фотоколориметрах используют, как правило, светофильтры; в спектрофотометрах свет разлагается в спектр с помощью призмы или дифракционной решетки, а затем на объект направляется луч света определенной длины волны. Кроме того, в спектрофотометрах существенно шире рабочая область длин волн света (фотоэлектроколориметры обычно работают только в видимой области). Для этой цели, как правило, в спектрофотометрах имеется два различных источника света и часто два фотоэлемента или других регистрирующих свет устройства.
Принципиальная схема (рис. 8) современных фотоэлектроколориметров включает в себя следующие блоки:
1) источник света, дающий излучение в видимой области спектра - лампа накаливания;
2) оптическая система;
3) светофильтр;
4) кюветное отделение;
5) фотоэлемент (чаще всего используется селеновый фотоэлемент), преобразующий энергию светового потока в электрическую энергию;
6) блок усилителя фототока;
7) регистрирующее устройство (высокочувствительный микроамперметр или цифровой вольтметр; в современных ФЭК - вычислительный блок с микропроцессорной системой).
Блок-схема спектрофотометра принципиально отличается тем, что вместо светофильтра в этих приборах используется монохроматор (призма или дифракционная решетка).

Рис. 8. Блок-схема фотоэлектроколориметра.
Принцип действия колориметров основан на измерении светопропускания или оптической плотности исследуемого образца относительно контрольного раствора. При этом оптическую плотность контроля принимают равной нулю. Контроль, а затем опытный образец поочередно устанавливают на пути светового потока. Световые потоки фотоприемниками преобразуются в электрические сигналы.
Правила работы на фотоколориметре KF-77 следующие:
В кюветное отделение ставят кюветы с контрольным и исследуемым растворами. Каретка с кюветами должна находиться в среднем положении, при котором световой поток оказывается перекрытым. Устанавливают нужный светофильтр (указанная на оправе светофильтра длина волны должна находиться вверху). Сдвигают каретку с установленными кюветами таким образом, чтобы на пути светового луча оказалась кювета с контрольным раствором. Стрелка измерительного прибора выводится на ноль оптической плотности (100% поглощения) с помощью ручек грубой и тонкой настройки, расположенных под шкалой. Затем каретку с установленными кюветами сдвигают таким образом, чтобы ввести в световой поток кювету с исследуемым раствором, и снимают отсчет по шкале оптической плотности или светопропускания.
Понятие о ксенобиотиках
Одна из центральных проблем современной биологии — изучение молекулярных механизмов действия физико-химических факторов на биосистемы различного уровня организации. Актуальность этой проблемы в настоящее время связана, в первую очередь, с развитием глобальных экологических катастроф, являющихся следствием производственной деятельности человека. К ним следует отнести антропогенную токсикацию планеты, обусловленную попаданием в окружающую среду и накоплением в живых организмах целого ряда неорганических и органических соединений. Ответная реакция целостного организма на воздействие того или иного экологического фактора является отражением структурно-функциональных изменений биологических макромолекул и их надмолекулярных комплексов под влиянием химических и физических агентов в клетке. Кроме того, экологический мониторинг невозможен без использования современных биофизических и биохимических методов анализа состояния биологических систем, характеризующихся высокой чувствительностью, точностью, быстродействием, позволяющих исследовать биопроцессы без нарушения живых структур в отдельных клетках, тканях и организме.
К ксенобиотикам (веществам, чужеродным для организма) относят продукты хозяйственной деятельности человека (промышленности, сельского хозяйства, транспорта), вещества бытовой химии (в т.ч. моющие средства), большинство лекарственных соединений.
Все ксенобиотики в той или иной мере токсичны для организмов. очень сложна. Для количественной оценки токсичности веществ определяют дозу токсина на один кг живого веса (массы) объекта, приводящую к 100%- или 50%-ой гибели организмов (соответственно ЛД100 или ЛД50). При получении дозы, меньше летальной, происходит выведение токсинов и продуктов их превращений из организма, характеризуемое временем полувыведения — t0,5 (варьирует от нескольких часов до нескольких десятков лет). Важными характеристиками токсинов являются также время 100%- или 50%-ой гибели объектов и способность разных ксенобиотиков распределяться в различных тканях и органах.
В организме токсины подвергаются ферментативным химическим превращениям, в результате которых может происходить как их дезактивация (детоксикация), так и усиление токсичности. В процессах метаболизма ксенобиотиков (в частности, лекарственных веществ) осуществляется их модификация (освобождение функциональных групп) и конъюгация (присоединение функциональных групп или молекул). Они протекают с участием системы цитохрома Р450, локализованной в мембранах эндоплазматической сети, а также глутатионтрансфераз гиалоплазмы. В последующих процессах связывания, транспорта и выведения ксенобиотиков участвуют альбумин и липопротеины сыворотки крови, глутатион-трансферазы клеток печени, металлотионеин, Р-гликопротеин, обладающий свойствами транспортной АТФазы.
К неорганическим токсинам относят, прежде всего, тяжелые металлы: ртуть, свинец, кадмий, кобальт, никель, цинк, олово, медь, молибден, мышьяк и другие. Они способны поступать в организм человека через легкие, слизистые оболочки, кожу, желудочно-кишечный тракт. Характер распределения и степень накопления тяжелых металлов в органах и тканях зависит от их химического сродства к биомакромолекулам, прочности образуемых комплексов и скорости их элиминации. Так, свинец концентрируется в костях скелета, кадмий — в почках и легких. В клетках некоторые металлы накапливаются преимущественно в ядрах (ртуть, свинец, никель, цинк), кадмий — в цитоплазме, марганец — в митохондриях. Они способны вступать во взаимодействие со свободными аминокислотами, белками (за счет карбоксильных, амино- и SH-групп, имидазольной группы гистидина), нуклеиновыми кислотами, органическими кислотами, фосфатами. В результате происходит нарушение структурного состояния и функциональной активности биополимеров и их комплексов, клеток и, как следствие, целого организма, его органов и систем.
Установлено, что как при однократном, так и при хроническом действии различных тяжелых металлов на организм в сыворотке крови увеличивается активность растворимых ферментов цитозоля: аланин- и аспартатаминотрансфераз, лактатдегидрогеназы, альдолазы, что связано с изменением проницаемости плазматической мембраны и выходом молекул белков из клетки. Повышение активности было отмечено и при исследовании уровня лизосомальных ферментов: β-галактозидазы и β-глюкуронидазы, а также кислой фосфатазы крови. Снижение функциональной активности наблюдали при изучении щелочной фосфатазы сыворотки крови и ферментов пероксисом (каталазы, пероксидазы) в крови и тканях. Ингибирование митохондриальных ферментов (сукцинатдегидрогеназы, цитохромоксидазы, АТФазы) при воздействии соединений ртути в опытах in vitro и in vivo обусловлено, по-видимому, блокированием SH-групп белков.
Тяжелые металлы выступают в роли ингибиторов монооксигеназных систем эндоплазматического ретикулума (цитохрома Р450), участвующих в метаболизме ксенобиотиков. Их токсическое действие на организмы связано и с нарушением обмена кальция, который выступает в роли универсального вторичного посредника (мессенджера) растительных и животных клеток. Определение содержания кальция в клетке используют как тест на цитотоксическое действие тяжелых металлов, так как избыточное его содержание является следствием рецепторзависимого транспорта ионов кальция в клетке и предшествует ее структурно-функциональным нарушениям. В норме ионы Са2+ взаимодействуют с кальцийсвязывающими белками, в частности кальмодулином, которые участвуют в регуляции работы многих ферментов (аденилатциклазы, Са2+-АТФазы, фосфолипаз, фосфорилазы и др.) и внутриклеточных процессов. Ионы тяжелых металлов способны конкурировать с кальцием за связывание с кальмодулином и тем самым тормозить транспорт Са2+ внутри клетки и, следовательно, вызывать нарушения процессов клеточного метаболизма.
Детальное исследование взаимодействия тяжелых металлов и других ксенобиотиков с белками-ферментами и их надмолекулярными комплексами имеет важное значение не только для оценки степени токсичности этих соединений, но и для выявления механизмов их модифицирующего и повреждающего действия на биосистемы.
Свинец и его соединения относятся к ядам политропного действия, обладающим высокой токсичностью и представляющим значительную опасность для человека в связи с тем, что в результате его производственной деятельности ежегодно попадает в природные воды до 500-600 тыс. тонн свинца, в атмосферу - около 400 тыс. тонн, а с выхлопными газами автомобилей — до 260 тыс. тонн.
В кишечнике всасывается около 10% свинца, попавшего с пищей и водой в организм, при вдыхании же паров и аэрозолей происходит его почти полное поглощение. В клинической картине свинцовой интоксикации ведущими синдромами являются поражение крови, нервной системы, желудочно-кишечного тракта. Свинец воздействует на память, уровень артериального давления, содержание витамина D, образование гемоглобина, продолжительность жизни эритроцитов, электрическую активность нервных клеток, обмен медиаторов, порфиринов, гормонов. Основным патогенетическим механизмом токсического воздействия свинца является блокирование ряда ферментов и, в силу этого, нарушение белкового, углеводного и фосфорного обмена организма. Не исключено также, что данный агент обладает мутагенным действием.
Интенсивное использование транспортных средств привело к резкому усилению выброса в атмосферу высокотоксичных соединений, образующихся при неполном сгорании топлива и непосредственно содержащихся в бензине. К ним, помимо свинца и его солей, относят оксид углерода, ароматические и циклические углеводороды (производные бензола, алкены, алкины и т. д.).
Выхлопные газы автомобилей содержат 2-10% СО. Отравление этим газом возможно только через дыхательные пути. Из легких он проникает в кровь, где благодаря значительно большему (в 250 раз) сродству с гемоглобином образует карбоксигемоглобин (НbСО), вытесняя кислород. Это обусловлено конкуренцией его с кислородом за шестое координационное место центрального атома железа порфирина. Таким образом, моноокись углерода является экзогенным веществом, оказывающим ингибирующее действие на дыхательную функцию гемоглобина. В основе отравления СО лежит кислородное голодание тканей, особенно клеток центральной нервной системы, наиболее чувствительных к снижению концентрации кислорода. При длительном воздействии малых концентраций моноокиси углерода на организм человека возможны хронические отравления, характеризующиеся головными болями, быстрой утомляемостью, слабостью, понижением памяти. При острых отравлениях дополнительно проявляются тошнота, рвота, учащение пульса, судороги и др.
К экологическим загрязнителям химической природы относят также детергенты, которые попадают в сточные воды химических комбинатов. К группе синтетических анионных детергентов относится додецилсульфат натрия (ДСН): CH3-(CH2)11-OSO-Na+
Считают, что отрицательно заряженная "головка" молекулы ДСН может электростатически взаимодействовать с положительно заряженными аминогруппами аминокислотных остатков белка (аргинина, лизина), имидазольной группой гистидина. Неполярная углеводородная часть ДСН способна, по-видимому, проникать в гидрофобную область белка.
Для детергентов характерно наличие специфически узкой области концентраций, при которой большинство их физико-химических свойств резко изменяется. Эта концентрация называется критической концентрацией мицеллообразования (ККМ). Величина ККМ зависит от ионной силы: для ДСН она уменьшается от 8,0 до 0,5 ммоль/л при возрастании ионной силы от 0 до 0,5. При достижении ККМ происходит ассоциация нескольких десятков молекул детергента с образованием сферических мицелл с общей молекулярной массой 12000—22000.
При концентрациях ДСН, близких к ККМ, преобладающим становится электростатическое взаимодействие молекул белка и детергента. При дальнейшем повышении концентрации ДСН количество мест связывания детергента в белке резко возрастает. По-видимому, это обусловлено изменением нативной структуры биополимера, частичной или полной дезорганизацией его молекул, а именно, разворачиванием белковых глобул.
Итак, в результате воздействия высоко- и низкомолекулярных токсических веществ на организм могут проявляться как специфический, так и общетоксический эффекты, в основе которых лежат нарушения структурно-функционального состояния ключевых биополимеров клетки и их надмолекулярных комплексов. Установлено, что реакция нервной системы на действие токсических веществ возможна на такой стадии, когда еще не обнаруживаются биохимические и морфологические нарушения. Это требует необходимости разработки информативных физико-химических методов анализа биологического действия различных ксенобиотиков на молекулярном, надмолекулярном и клеточном уровнях организации живых систем.
Учитывая тот факт, что воздействие токсических соединений на организм непосредственно связано с белковыми системами крови, выполняющей защитную и транспортную функции, студентам предложены для выполнения лабораторные работы, связанные с исследованием изменений структурно-функциональных свойств гемоглобина в присутствии некоторых ксенобиотиков.
Экспериментальная часть
Опыт 1. Исследование влияния температуры на оптические свойства растворов оксигемоглобина
Цель работы: изучить оптические свойства растворов оксигемоглобина, модифицированного воздействием различных температур.
Материалы и оборудование:раствор оксигемоглобина, физиологический раствор NaCl спектрофотометр СФ-4 или электрофотоколориметр, термостат.
Ход работы
Приготовить раствор оксигемоглобина в концентрации 1∙10-5 моль/л.
Измерить оптическую плотность опытного раствора при различных длинах волн (используя прилагающиеся светофильтры при работе на фотоколориметре или изменяя длину волны от 230 до 650 нм с шагом 40-50 нм при работе на спектрофотометре); данные занести в таблицу.
Построить спектр поглощения раствора оксигемоглобина.
Для дальнейших исследований выбрать ту длину волны света, при которой оптическая плотность образца имеет наибольшую величину, так как измерения необходимо проводить в области максимума поглощения исследуемого образца.
Нагреть термостат до необходимой температуры и поместить в него растворы гемоглобина (варианты термостатирования см. ниже).
Измерить оптическую плотность термомодифицированных растворов белка.
Сделать выводы об оптических свойствах растворов гемоглобина, модифицированных воздействием различных температур; о связи оптических свойств и структуры молекулы биополимера.
Вариант 1. Растворы белка термостатировать при 35, 45 и 55°С в течение 20 мин.
Вариант 2. Растворы белка нагревать при 40°С в течение 10, 20, 30, 50 мин.
Вариант 3. Растворы белка нагревать при 50°С в течение 5; 10; 15; 20 мин.
Опыт 2. Исследование спектральных характеристик оксигемоглобина человека, модифицированного солями свинца и кадмия
Цель работы: исследовать спектральные свойства оксигемоглобина человека в нативном состоянии и в присутствии солей свинца и кадмия.
Материалы и обрудование:раствор оксигемоглобина, физиологический раствор NaCl, раствор PbNO3, раствор CdSO4, спектрофотометр СФ-4 или электрофотоколориметр..
Ход работы
Приготовить раствор оксигемоглобина в концентрации 2∙10-5 моль/л.
А) К раствору оксигемоглобина человека добавить раствор нитрата свинца в объемном соотношении 1:1 (диапазон концентраций нитрата свинца согласовывается с преподавателем). Зарегистрировать электронные спектры поглощения в области длин волн 230-650 нм контрольного образца белка с учетом эффекта разведения и смесей гемопротеида с модифицирующим агентом. Построить спектры поглощения исследуемых образцов и проанализировать, как изменяются интенсивность и λmах полос поглощения гемоглобина в присутствии соли свинца по сравнению с этими параметрами для раствора интактного гемоглобина. Сделать вывод о характере и природе структурных нарушений, возникающих в гемоглобине под влиянием модифицирующего агента.
Б) В качестве модифицирующего агента использовать сернокислый кадмий. Все операции проводить, как описано в варианте А).
Опыт 3. Исследование структурно-функциональных свойств оксигемоглобина человека, модифицированного воздействием додецилсульфата натрия
Цель работы: Изучить изменения структурно-функционального состояния оксигемоглобина человека, модифицированного воздействием додецилсульфата натрия.
Материалы и обрудование:раствор оксигемоглобина, физиологический раствор NaCl, додецилсульфат натрия, спектрофотометр СФ-4 или электрофотоколориметр.
Ход работы
Приготовить раствор оксигемоглобина в концентрации 3,4∙10-5 моль/л.
К раствору оксигемоглобина человека добавить растворы додецилсульфата натрия (6,9∙10-2 моль/л и 3,4∙10-4 моль/л) в объемном соотношении 1:1. Зарегистрировать электронные спектры поглощения в области длин волн 230-650 нм контрольного образца белка с учетом эффекта разведения и смеси гемоглобина с додецилсульфатом натрия (ДСН). Построить спектры поглощения указанных образцов и проанализировать, как изменяются интенсивность и λmах полос поглощения гемоглобина в присутствии ДСН. Сделать вывод о характере и природе структурных нарушений, возникающих в белке под влиянием модифицирующего агента в различных концентрациях.
Контрольные вопросы
1. Основные характеристики оптического излучения.
2. Понятие об оптической плотности, светопропускании, светопоглощении; взаимосвязь между данными параметрами.
3. Закон Бугера-Ламберта-Бера, причины отклонения от него.
4. Применение спектральных методов в биологии и медицине.
5. Принцип устройства фотоэлектроколориметров и спектрофотометров.
6. Связь оптических характеристик и структурного состояния биополимеров.
7. Оптическая плотность раствора D=0,08. Найдите его светопоглощение и светопропускание.
8. Интенсивность света, прошедшего через раствор, уменьшилась в 10 раз. Известно, что данное вещество имеет молярный коэффициент поглощения на данной длине волны, равный 500 моль-1см-1. Толщина кюветы с раствором — 1 см. Найдите концентрацию вещества в растворе.
9. Чему равен молярный коэффициент поглощения вещества при длине волны 400 нм, если при прохождении света через раствор с концентрацией 0,5 моль/л интенсивность света уменьшилась в 5 раз? Толщина кюветы равна 0,3 см.
10. Какие соединения относят к группе ксенобиотиков? Каковы особенности их строения, физико-химических свойств, пути попадания и механизмы утилизации в организме?
11. Каковы механизмы модифицирующего и повреждающего действия тяжелых металлов на биосистемы различного уровня организации?
12. На каком основании додецилсульфат натрия относят к группе ксенобиотиков? От каких факторов зависит характер его модифицирующего действия на биополимеры?
13. Каковы возможные последствия воздействия соединений свинца на структурно-функциональное состояние белковых компонентов крови?
Список рекомендуемой литературы
1. Кулинский В. И. Обезвреживание ксенобиотиков // Соросовский образоват. журн. — 1999. — №1 (38). — С. 8—12.
2. Пурмаль А. П. Антропогенная токсикация планеты // Соросовский образоват. журн. — 1998. — №9 (34). — С. 39—51.
3. Артюхов В. Г., Путинцева О. В. Оптические методы анализа интактных и модифицированных биологических систем. — Воронеж: Изд-во ВГУ, 1996. — 240 с.
4. Артюхов В. Г., Ковалева Т. А., Шмелев В. П. Биофизика. — Воронеж: Изд-во ВГУ, 1994. — 336 с.
5. Владимиров Ю. А., Потапенко А. Я. Физико-химические основы фотобиологических процессов. — М.: Высш. школа, 1989. — 199 с.
6.Виноградова Р.П., Цудзевич Б.А., Храпунов Б.А. Физико-химические методы в биохимии. – Киев, Вища Школа. Головное из-во, 1983. – 287 с.
7.Конев С. В., Волотовский И. Д. Фотобиология. — Минск: Изд-во БГУ, 1979. — 178 с.
ТЕМА 3. ЭЛЕКТРОФОРЕЗ
Лабораторная работа №3.1
Разделение белков сыворотки крови методом электрофореза
Белки плазмы крови
Из 9-10% сухого остатка плазмы крови на долю белков приходится 6,5-8,5%. Нормальное содержание альбуминов в плазме крови составляет 4-6 г/100 мл, глобулинов — 2-З г/100 мл, фибриногена — 0,2-0,4 г/100 мл. Физиологическая роль белков плазмы крови многогранна:
1. Поддержание онкотического давления и тем самым сохранение объема циркулирующей крови. В этом процессе особенно велика роль альбуминов.
2.Участие в свертывании крови. Ряд белков плазмы, в том числе фибриноген, являются компонентами системы свертывания крови.
3.Поддержание постоянного рН крови.
4.Транспортная функция. Белки плазмы переносят нерастворимые вещества (липиды, билирубин, жирные кислоты, жирорастворимые витамины и др.) в ткани и органы.
5.Участие в иммунных процессах организма. Сывороточные иммуноглобулины входят в состав фракции γ-глобулинов сыворотки крови.
6.Поддержание уровней катионов в крови путем образования с ними соединений. Например, 40-50% ионов Са2+ и других элементов связаны с белками сыворотки.
7.Сывороточные белки образуют «белковый резерв» организма. При голодании они могут распадаться до аминокислот, которые используются для синтеза белков головного мозга, миокарда и других органов.
В клинической практике часто встречаются состояния, характеризующиеся изменением общего количества белков плазмы крови.
Обширные ожоги, потеря воды и другие факторы могут вызвать гиперпротеинемию - повышение общей концентрации белков в плазме.
При ряде патологических состояний могут наблюдаться гиперпротеинемии, обусловленные резким увеличением количества отдельных видов белков, например, γ-глобулинов при миеломной болезни.
Гипопротеинемия — уменьшение общего количества белка в плазме крови — возникает главным образом за счет уменьшения количества альбуминов (при острой атрофии печени, поражении желудочно-кишечного тракта и др.).
Диспротеинемия — изменение процентного соотношения отдельных белковых фракций при нормальном общем содержании белка в сыворотке крови.
При остром гепатите, циррозе печени и застойных желтухах отмечается уменьшение содержания α-липопротеинов в сыворотке крови, а при хроническом гепатите их содержание нередко увеличивается. При нефротическом синдроме, микседеме, ксантоматозе, атеросклерозе увеличивается содержание β-липопротеинов. Увеличение содержания гликопроте
