Энергия системы. Внутренняя энергия. Теплота и работа. Первый закон термодинамики. Функции состояния и функции перехода. Энтальпия.
Внутренняя энергия термодинамическая функция состояния системы, ее энергия, определяемая внутренним состоянием. Внутренняя энергия складывается в основном из кинетической энергии движения частиц (атомов, молекул, ионов, электронов) и энергии взаимодействия между ними (внутри- и межмолекулярной). На внутреннюю энергию влияет изменение внутреннего состояния системы под действием внешнего поля; во внутреннюю энергию входит, в частности, энергия, связанная с поляризацией диэлектрика во внешнем электрическом поле и намагничиванием парамагнетика во внешнем магнитном поле. Кинетическая энергия системы как целого и потенциальная энергия, обусловленная пространственным расположением системы, во внутреннюю энергию не включаются. В термодинамике определяется лишь изменение внутренней энергии в различных процессах. Поэтому внутреннюю энергию задают с точностью до некоторого постоянного слагаемого, зависящего от энергии, принятой за нуль отсчета.
Теплота Q представляет собой количественную меру хаотического движения частиц данной системы или тела. Энергия более нагретого тела в форме теплоты передается менее нагретому телу. При этом не происходит переноса вещества.
Работа А является количественной мерой направленного движения частиц, мерой энергии, передаваемой от одной системы к другой за счет перемещения вещества от одной системы к другой под действием тех или иных сил, например гравитационных.Теплоту и работу измеряют в джоулях (Дж), килоджоулях (кДж) и мегаджоулях (МДж). Положительной считается работа, совершаемая системой против внешних сил (А> 0) и теплота, подводимая к системе (Q > 0). Теплота и работа зависят от способа проведения процесса, т.е. они являются функциями пути.
Первый закон(первое начало) термодинамики - это, фактически, закон сохранения энергии. Он утверждает, что энергия изолированной системы постоянна. В неизолированной системе энергия может изменяться за счет совершения работы над окружающей средой и теплообмена с окружающей средой.
Состояние системы описывается также с помощью термодинамических функций, которые зависят от параметров. Различают:
- функции состояния, которые зависят только от состояния системы и не зависят от пути, по которому это состояние получено;
- функции перехода, значение которых зависит от пути, по которому происходит изменение системы.
Примеры функций состояния: энергия U, энтальпия H, энергия Гельмгольца F, энергия Гиббса G, энтропия S. Термодинамические параметры объем V, давление p, температуру T также можно считать функциями состояния, т.к. они однозначно характеризуют состояние системы. Примеры функций перехода: теплота Q и работа A.
Функции состояния характеризуются следующими свойствами:
- бесконечно малое изменение функции f является полным дифференциалом (обозначается df);
- изменение функции при переходе из состояния 1 в состояние 2 определяется только этими состояниями: 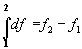 ;
;
- в результате любого циклического процесса функция состояния не изменяется: 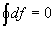
Энтальпи́я, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц. Проще говоря, энтальпия — это та энергия, которая доступна для преобразования в теплоту при определённом постоянном давлении.Энтальпия или энергия расширенно системы {\displaystyle E} равна сумме внутренней энергии газа {\displaystyle U} и потенциальной энергии поршня с грузом {\displaystyle E_{pot}=pSx=pV}
