Определение теплоты растворения соли
Цель работы:определить теплоту растворения соли с использованием термометра Бекмана.
Теоретическое обоснование.
Процесс растворения, как правило, сопровождается различными тепловыми эффектами, зависящими от многих факторов: температуры, давления, природы растворителя и растворяемого вещества, концентрации образующегося раствора и т.д.
Рассмотрим процесс растворения твердой соли в жидком растворителе. Данный процесс можно условно разделить на две стадии:
1. разрушение кристаллической решетки соли
2. образование нестойких соединений частиц растворенного вещества с молекулами растворителя – сольватация.
Обе стадии сопровождаются определенным тепловым эффектом, причем, как правило, разрушение кристаллической решетки является эндотермическим процессом, а сольватация – экзотермическим. Общий тепловой эффект растворения соли будет складываться из тепловых эффектов вышеупомянутых стадий и может быть как положительной, так и отрицательной величиной, в зависимости от их соотношения.
Для количественной характеристики процесса растворения используют понятие теплоты растворения – количество теплоты, соответствующее растворению 1 моль вещества в достаточно большом количестве растворителя при постоянном давлении и температуре. Количество растворителя при этом должно быть таким, чтобы дальнейшее добавление вещества к раствору не вызывало изменения энтальпии системы.
Обозначается Q раств , измеряется Дж/моль
Определение теплоты растворения проводят с использованием термометра Бекмана, который позволяет проводить измерение температур с точностью до 0,002 °C. Особенностью этого прибора является большая длина шкалы ( около 5 см на 1 °C) и наличие запасного резервуара со ртутью, позволяющего изменять количество ртути в рабочей части термометра.
|
|
|
|

Рисунок 1. Термометр Бекмана
Шкала термометра разделена на 5 °C. Каждый градус делится на десятые доли, а каждая десятая доля – на сотые. По термометру отмечают не абсолютную температуру, а ее изменение в ходе какого- либо процесса. Предварительно необходимо провести настройку термометра, то есть установку уровня ртути в определенном интервале температур. Если процесс будет проходить с поглощением тепла, то уровень ртути в термометре устанавливают в интервале от 3 °C до 5 °C, если с выделением тепла – в интервале от 0 °C до 2 °C при начальной температуре процесса.
С помощью термометра Бекмана можно определить перепад температур в процессе растворения соли, который вызван одномоментным выделением или поглощением теплоты, и произвести расчет теплоты растворения.
Порядок выполнения работы.
1. Собирают прибор для определения теплоты растворения соли (рисунок 2).
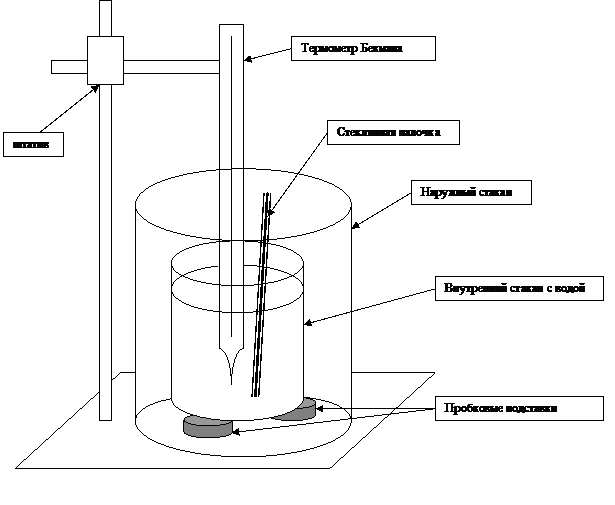
Рисунок 2. Схема прибора для определения теплоты растворения соли.
Для этого в наружный стакан помещают на пробковых подставках внутренний стакан меньшего размера. Предварительно необходимо взвесить внутренний стакан вместе со стеклянной палочкой на техно-аналитических весах с точностью до 1 грамма. Вес стакана записать.
2. Взвешивают около 5 граммов соли на аналитических весах (образец соли выдается преподавателем), точный вес соли записывают.
3. Рассчитывают количество воды, необходимое для растворения соли из расчёта на 1 моль соли – 200 моль воды.
Пример расчета:
Для анализа студенту выдана соль хлорид натрия, точный вес – 5,01234 г.
Молярная масса хлорида натрия: 58,45 г/моль
Масса воды, необходимая для растворения соли:
200·18·mсоли 200·18·5,01234
mв =----------------------=------------------------=308,72 (г) Объем воды 309 мл.
Мсоли 58,45
4. Во внутренний стакан с палочкой наливают рассчитанное количество воды и помещают термометр Бекмана, таким образом, чтобы ртуть термометра помещалась в воду полностью.
Измеряют температуру воды (без соли) в течении 10 минут через каждую минуту (промежуток времени в 1 минуту отмеряют по песочным часам).
На 11-й минуте высыпают соль, тщательно перемешивают. Когда вся соль растворяется, записывают первую температуру (после высыпания соли) и продолжают записывать температуру в течении 10 минут, проверяя значения по термометру .
Полученные данные сводят в таблицу.
Таблица результатов:
| Масса соли, mсоли , | Масса стакана, ·mстакана | Масса воды, , mводы | ||||||||||
| До растворения соли | ||||||||||||
| Время, τ, мин | ||||||||||||
| Температура, t,°C | ||||||||||||
| После растворения соли | ||||||||||||
| Время, τ, мин | ||||||||||||
| Температура, t,°C | ||||||||||||
5.По результатам исследования на миллиметровой бумаге строят график зависимости температуры раствора от времени.
По данному графику находят скачок температуры раствора в момент растворения соли. Приблизительный график зависимости t = f(τ) представлен на рисунке 3.
T, °  С
С
| |||||||
| |||||||
 | |||||||
 | |||||||
τ,мин
Рисунок 3. График зависимости температуры раствора от времени
6. Теплоту растворения данной навески соли в Дж рассчитывают по формуле:
g = (mсоли + mводы)·С·(t2 –t1) + mстакана ·α· (t2 –t1) ,
где
С – теплоемкость раствора, приблизительно принимается 4,190 Дж/г·°C
α - теплоемкость стекла, равна 0,7961 Дж/г·°C
t1– значение температуры на 10 минуте измерений (до растворения соли),
t2–наименьшая температура после растворения соли,
g - теплота растворения навески соли ( массой mсоли )
Затем рассчитывают теплоту растворения Q на 1 моль соли в Дж/моль:
g·Mсоли
Q = -------------------------
mсоли
Содержание отчета о работе
Отчет о работе должен содержать:
- Тему работы
- Цель работы
- Краткие теоретические сведения(определение теплоты растворения соли, ее основные составляющие)
- Индивидуальное задание (название соли – выдается преподавателем)
- Таблицу результатов с полученными данными
- График зависимости t = f(τ), построенный на миллиметровой бумаге
- Расчет теплоты растворения заданной соли.
Контрольные вопросы
- Дайте определение теплоты растворения соли.
- Перечислите основные составляющие теплового эффекта процесса растворения.
- Опишите устройство термометра Бекмана.
- Какие показатели и с какой точностью можно определить при измерениях с помощью термометра Бекмана?
Лабораторная работа № 4
