Строение атома. Периодическая система элементов. Химическая связь и химические свойства соединений
Строение атома
Состояние электрона в атоме можно представить в виде электронного облака, которое называют атомной орбиталью (АО). Размеры, форма и расположение АО в пространстве возле ядра атома определяются параметрами, которые получили названия квантовых чисел электрона. Каждый электрон в атоме имеет свой индивидуальный набор из четырех квантовых чисел.
ГЛАВНОЕ КВАНТОВОЕ ЧИСЛОn определяет энергетический уровень электрона (электронную оболочку) и размеры электронного облака, n имеет значения 1,2,3,4,..∞ Чем больше n, тем больше энергия электрона, тем дальше находится электрон от ядра атома.
ПОБОЧНОЕ КВАНТОВОЕ ЧИСЛОℓхарактеризует энергетический подуровень электрона и форму электронного облака. Значения ℓ зависят от n и изменяются через единицу от (n-1) до 0. Так, если n =3 (третий электронный уровень), то ℓ имеет три значения: 2,1,0. В таком случае говорят, что третий энергетический уровень атома имеет три подуровня. Соответственно, на первом уровне - один подуровень, на втором - два, на четвертом - четыре и т.д. Энергетические подуровни имеют буквенные обозначения, если ℓ=0- это s-подуровень, ℓ = 1 - р-подуровень; ℓ=2 - d-подуровень; ℓ=3 - f-подуровень. Энергетические подуровни имеют определенную емкость, на подуровне s может находиться не более двух электронов, на р – 6; на d -10 и f -14 электронов.
МАГНИТНОЕ КВАНТОВОЕ ЧИСЛОm определяет ориентацию электронного облака в пространстве и, как следствие этого, его магнитные свойства. Значения m зависят от ℓ и изменяются через единицу от + ℓ ..0...- ℓ. Так, если ℓ =3, то m имеет значения: +3, +2, +1, 0, -1, -2, -3. Графически каждое значение обозначается клеткой «□», или чертой «—« . (Одна клетка или черта соответствует одной АО).
СПИНОВОЕ КВАНТОВОЕ ЧИСЛОs характеризует собственный момент количества движения электрона, который представляют как вращение электрона вокруг собственной оси (вращение волчка). s имеет, поэтому, только два значения +1/2 и -1/2. Графически спин электронов обозначается вертикальными стрелками (↑↓) разного направления.
Распределение электронов по АО происходит в соответствии с ПРИНЦИПОМ ПАУЛИ И ПРАВИЛОМ ХУНДА.
ПРИНЦИП ПАУЛИ.В атоме не может быть электронов с одинаковым набором квантовых чисел. Электроны должны отличаться между собой хотя бы одним квантовым числом.
ПРАВИЛО ХУНДА.При последовательном заполнении электронами свободных АО электроны занимают АО вначале по одному, имея спин +1/2, (значение суммарного спина электронов должно быть максимальным).
ПРИМЕР 1
На первом энергетическом уровне может находиться два электрона. Написать электронную и электронно-графическую формулы для данного состояния.
РЕШЕНИЕ
В электронной формуле указывается значение n (n = 1 для первого уровня), буквенное значение подуровня - s и число электронов на подуровне – два. Следовательно, электронная формула этого состояния 1s2. Электронно-графическая формула выглядит, как одна АО
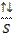 .
.
ПРИМЕР 2
Выполнить задание из примера 1 для третьего энергетического уровня, на котором находится 18 электронов.
РЕШЕНИЕ
На третьем уровне имеются три подуровня - s, p, d, на которых могут находиться соответственно 2, 6, 10 электронов. На одной АО располагаются по два электрона с противоположными спинами (принцип Паули). Значит, электронная формула данного энергетического состояния имеет вид: 3s2 Зр6 3d10 .
Электронно-графическая формула имеет вид


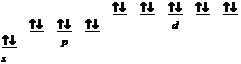
ПРИМЕР 3
Написать электронно-графическую формулу для электронов 4d5.
РЕШЕНИЕ
Для d - подуровня ℓ = 2, поэтому m имеет пять значений +2, +1, 0, -1, -2. Следовательно, на этом подуровне пять АО. В соответствии с правилом Хунда электроны заполняют эти АО по одному. Электронно-графическая формула
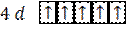 .
.
Суммарный спин s = 5·(1/2) = 2,5.
