Реакции, идущие с участием гидроксильной группы.
1. Взаимодействие с галогеноводородами.
C2H5OH + HBr = C2H5Br + HOH
2. Отщепление воды.
C2H5OH -> H2C=CH2 + H2O
3. Межмолекулярная дегидротация.
C2H5OH + HOC2H5= (C2H5)2O + H2O
Образуется диэтиловый эфир
Реакции окисления.
1. Отщепление водорода (дегидрирование).
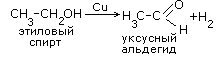
2. Окисление спиртов сильными окислителями. (например KMnO4 + H2SO4).
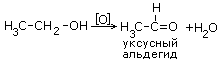
3. Реакции горения спиртов.
C2H5OH+3O2=2CO2+3H2O
3 C5H8 пентин
Гомологи
HC=-C-CH2-CH3
Бутин-1
HC=-C-CH2-CH2-CH2-CH3
Гексин-1
Изомеры
HС=-С-СH2-СH2-СH3
Пентин-1
H3C-C=-C-CH2-CH2-CH3
Пентин-2
H3C-CH2-C=-C-CH3
Пентин-3
HC=-C-CH2-CH3
'
CH3
2-метилбутин-1
4 а) Из синтез газа получаем метанол
Синтез метанола из оксида углерода и водорода проводится при высоких давлениях и пониженной температуре,которые зависят от типа катализатора.
СО+2Н2=СН3ОН экзотермическая реакция
Б) из метанола получить метиловый эфир бутановой кислоты
Реакция этерефикации
При температуре 140 с использованием реостата
CH3OH+H3C-CH2-CH2-C=O = H3C-CH2-CH2-C=O +H20
-OH -OCH3
В) из метанола метилат натрия
Реакция замещения
CH3OH+Na=CH3ONa+H2
Г) Основной способ получения формальдегида — окисление метанола:
2CH3OH + O2 → 2HCHO + 2H2O
Окисление метанола в формальдегид проводится с использованием серебряного катализатора при температуре 650 °C и атмосферном давлении. Это хорошо освоенный технологический процесс, и 80 % формальдегида получается именно по этому методу. Недавно разработан более перспективный способ, основанный на использовании железо-молибденовых катализаторов. При этом реакция проводится при 300 °C. В обоих процессах степень превращения составляет 99 %.
Д) из муравьиного альдегида получить металлическое серебро
HCHO + Ag2O = Ag2O + HCOOH
Билет13
Альдеги́ды (от лат. alcohol dehydrogenatus — спирт, лишённый водорода) — класс органических соединений, содержащих альдегидную группу (-CHO)[1]. ИЮПАК определяет альдегиды как вещества вида R-CHO, в которых карбонильная группа связана с одним атомом водорода и одной группой R[2].
Содержание
- 1 Названия альдегидов
- 1.1 Этимология
- 1.2 Тривиальные названия
- 1.3 Систематическая номенклатура
- 2 Классификация альдегидов
- 3 Нахождение в природе
- 4 Методы синтеза альдегидов
- 4.1 Лабораторные методы получения альдегидов
- 4.1.1 Окислительные методы
- 4.1.2 Восстановительные методы
- 4.1.3 Синтез ароматических альдегидов
- 4.1.4 Другие методы
- 4.2 Промышленные методы получения альдегидов
- 5 Физические свойства альдегидов
- 6 Строение
- 7 Химические свойства
- 7.1 Реакции присоединения к карбонильной группе
- 7.2 Реакции сопряжённого присоединения
- 7.3 Реакции α-метиленового звена
- 7.4 Реакции окисления
- 7.5 Реакции восстановления
- 7.6 Альдегиды как основания Льюиса
- 7.7 Другие реакции
- 8 Химические методы идентификации альдегидов
- 8.1 Качественный анализ карбонильных групп
- 8.2 Количественный анализ альдегидов
- 9 Спектральные методы анализа альдегидов
- 9.1 ИК-спектроскопические методы анализа альдегидов
- 9.2 Масс-спектрометрические методы анализа альдегидов
- 9.3 ЯМР-спектроскопические методы анализа альдегидов
- 9.4 УФ-спектроскопические методы анализа альдегидов
- 9.5 Электронно-спектроскопические методы анализа альдегидов
- 10 Биологическое действие
- 11 Применение
- 12 Примечания
- 13 Литература
Названия альдегидов
Этимология
Слово альдегид было придумано Юстусом фон Либихом как сокращение латинского alcohol dehydrogenatus — дегидрированный спирт[3] (в некоторых источниках — alcohol dehydrogenatum[1]). Название радикала формил, а также другие однокоренные слова (формальдегид, формиаты), произошли от лат. formica — муравей[источник не указан 1612 дней].
Тривиальные названия
В популярной и научной литературе можно нередко встретить исторические, или тривиальные, названия альдегидов, которые вследствие сложившейся традиции используются вместо систематических названий. Тривиальные названия обычно происходят от названия соответствующих карбоновых кислот, а также от названия источника, из которого был выделен тот или иной альдегид. Так, например, формальдегид называют муравьиным альдегидом, этаналь — уксусным, пентаналь — валериановым альдегидом, цитронеллаль получил своё название, поскольку был выделен из масла цитрусовых.
Исторически сложилось, что парфюмеры называют многие пахучие вещества альдегидами, даже те, которые не имеют ничего общего с ними. Среди таковых, например, персиковый, земляничный и кокосовый альдегид, которые являются не альдегидами, а сложными эфирами или лактонами. Также некоторые альдегиды традиционно называются по числу атомов углерода, например, персиковый альдегид, обозначаемый как «альдегид C14», на самом деле имеет лишь 11 атомов углерода[4].
