Электронное строение органических соединений
11. sp2 – Гибридных атомов нет в составе:
+ 1. глицерина;
- 2. пропановой кислоты;
+ 3. бутана;
+ 4. этилового спирта;
- 5. анилина.
12. Пиррольные гетероатомы входят в состав следующих соединений:
+ 1. анилин;
- 2. этанол;
+ 3. фенол;
- 4. бензальдегид;
- 5. 3-метилбутанамин-1.
13. π-π – сопряжение есть в структуре:
+ 1. бензола;
+ 2. пентадиена – 1,3
- 3. пентадиена – 1,4
- 4. пропаналя;
- 5. пропановой кислоты.
14. p-π – сопряжение есть в структуре:
+ 1. уксусной кислоты;
+ 2. 2-гидроксипропановой кислоты;
- 3. этиленгликоля;
- 4. пиридина;
- 5. пропен-2-аля.
15. Ароматическими являются следующие соединения:
- 1. циклогексан;
- 2. циклооктатетраен;
+ 3. нафталин;
+ 4. пиррол;
+ 5. бензол
16. Ароматическими не являются следующие соединения:
- 1. пиридин;
+ 2. циклогексен-1;
- 3. антрацен;
+ 4. циклопентадиен-1,3
- 5. фуран.
17. У функциональной группы есть отрицательный мезомерный эффект в соединениях:
- 1. этанол;
- 2. глицерин;
- 3. ацетон;
+ 4. бутен-2-аль-1;
- 5. 4-метиланилин.
18. У функциональной группы есть только отрицательный индуктивный эффект в соединениях:
- 1. фенол;
+ 2. этиленгликоль;
+ 3. уксусная кислота;
- 4. этандиовая кислота;
- 5. метилфенилкетон.
19. Все функциональные группы являются электроноакцепторными в соединениях:
+ 1. 2-аминоэтанол-1;
- 2. 2-гидроксибензойная кислота;
- 3. 4-аминобензолсульфоновая кислота.
- 4. 4-гидрокси-3-метоксибензальдегид;
+ 5. 2,3-дигидроксипропаналь.
20. В соединении:

Электронодонорами являются следующие функциональные группы:
- 1. аминогруппа;
- 2. гидроксильная спиртовая группа;
+ 3. гидроксильные фенольные группы;
- 4. бензольное кольцо и аминогруппа;
- 5. все гидроксильные группы.
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ.
21. Проекционные формулы Ньюмена записывают, чтобы показать различия:
- 1. в химическом строении соединений;
+ 2. в конформациях молекулы;
- 3. структурных изомеров;
- 4. в конфигурационном строении энантиомеров;
- 5. в строении Е и Z π – диастереомеров.
22. Энергия пропанола–1 в анти-конформации меньше, чем в скошенной, т.к. в анти–конформации:
- 1. меньше угловое напряжение;
- 2. изменилась конфигурация;
+ 3. уменьшилось Ван-дер-Ваальсово отталкивание;
- 4. стало меньше торсионное напряжение;
- 5. изменилось химическое строение.
23. Энергия 2–хлорбутана в заслоненной конформации больше, чем в скошенной, т.к. в заслоненной конформации:
- 1. у молекулы другая конфигурация;
- 2. больше торсионное напряжение;
- 3. у молекулы другое электронное строение;
- 4. больше угловое напряжение;
+ 5. увеличивается Ван-дер-Ваальсово отталкивание.
24. Конформации 1–хлор–пропана с торсионным углом 60˚ и 300˚ являются вырожденными, т.к. в этих конформациях у молекулы:
- 1. одинаковая конфигурация;
- 2. одинаковое химическое строение;
- 3. разное конформационное строение;
+ 4. одинаковые торсионное, Ван-дер-Ваальсовое и угловое напряжения;
+ 5. одинаковая энергия.
25. Молекула 1,2 – диметилциклогексана имеет максимальный запас энергии, если:
- 1. оба метильных заместителя на экваториальных связях;
+ 2. оба метильных заместителя на аксиальных связях;
- 3. один из двух заместителей на аксиальной связи;
- 4. один из двух заместителей на экваториальной связи;
- 5. один заместитель на аксиальной, второй на экваториальной связи.
26. Хиральными молекулами являются:
- 1. глицин (2-аминоэтановая кислота);
+ 2. серин (2-амино-3-гидроксипропановая кислота);
+ 3. D-рибоза;
- 4. бутанол-1;
+ 5. бутанол – 2.
27. Хиральными молекулами являются:
+ 1. D – глюкоза;
+ 2. аланин (2-аминопропановая кислота);
- 3. 2 – аминоэтанол;
+ 4. ментол (ментанол – 3);
- 5. фурфурол (фуран-2-карбальдегид).
28. Рацемат может иметь удельный угол вращения плоскости поляризованного света при 25˚С:
- 1. +5,2˚;
+ 2. 0,0˚;
- 3. –8,3˚;
- 4. –5,2˚;
- 5. +6,0˚.
29. 2-аминопропановая кислота имеет следующее количество стереоизомеров:
- 1. 1;
+ 2. 2;
- 3. 3;
- 4. 4;
- 5. 5
30. 2, 3, 4-тригидроксибутановой кислоте соответствует следующее количество стереоизомеров:
- 1. 1;
- 2. 2;
- 3. 3;
+ 4. 4;
- 5. стереоизомерия невозможна.
КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ.
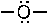 | 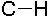 | 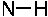 | 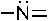 | 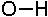 | |||||
31. Кислотными реакционными центрами являются:
-1. +2. +3. -4. +5.
32. Кислотный реакционный центр имеют функциональные группы:
- 1. сложных эфиров;
- 2. кетонов;
+ 3. сульфоновых кислот;
+ 4. аминов;
- 5. простых эфиров.
33. Основными реакционными центрами являются:
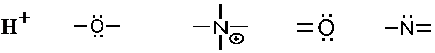
-1. +2. -3. +4. +5.
34. Основный реакционный центр на атоме кислорода имеют функциональные группы:
+ 1. кетонов;
+ 2. амидов;
- 3. нитрилов;
- 4. галогенопроизводных углеводородов;
+ 5. ангидридов.
 |  | 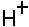 | 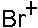 | 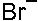 | |||||
35. Электрофильными частицами являются:
-1. -2. +3. +4. -5
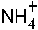 |
36. Нуклеофилами являются:
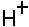 |  |  |  | ||||
-1. +2. +3. +4. -5.
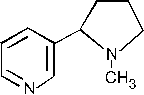 |
37. Наиболее сильным основным центром молекулы никотина является:
- 1. π–электронная система шестичленного цикла;
+ 2. sр3–гибридный атом азота;
- 3. sр2–гибридный атом азота;
- 4. атом азота с пиридиновым строением;
+ 5. атом азота в пирролидиновом цикле.
38. Наиболее сильным кислотным центром молекулы оксипролина (4-гидроксипирролидин-2-карбоновая кислота) является:
+ 1. гидроксильная группа с пиррольным строением кислорода;
- 2. гидроксильная группа с sр3–гибридным кислородом;
- 3. N–Н кислотный центр;
- 4. ОН– группа, связанная с гетероциклом непосредственно;
+ 5. ОН– группа, в составе функциональной группы карбоновых кислот.
39. Наиболее сильно выражены кислотные свойства у соединения:
- 1. уксусная кислота;
- 2. пропановая кислота;
- 3. 2-метилпропановая кислота;
+ 4. 2,2,2-трихлорэтановая кислота;
- 5. 2-аминопропановая кислота.
40. Самой слабой кислотой является:
+ 1. этанамин;
- 2. этанол;
- 3. фенол;
- 4. этановая кислота;
- 5. этантиол.
41. Самым сильным основанием является:
- 1. 2-аминоэтанол;
- 2. этанамин;
- 3. метиламин;
+ 4. диметиламин;
- 5. пиридин.
