Энтальпийный и энтропийный факторы
Вопрос 1. Основные понятия термодинамики. Интенсивные и экстенсивные свойства системы. Внутренняя энергия. Работа и теплота – две формы передачи энергии. Типы термодинамических систем и процессов.
Основные понятия термодинамики:
Термодинамическая система – это отдельное тело или группа тел фактически или мысленно отделенных от окружающей среды.
Интенсивные и экстенсивные свойства системы:
1. Экстенсивное свойство системы прямо пропорционально массе системы и обладает аддитивностью (можно складывать): V, H, Uвн, S, G, F.
2. Интенсивное свойство системы не зависит от массы системы и не обладает свойством аддитивности: Q, A, T, P.
Термодинамический процесс – переход системы из одного состояния в другое, сопровождающееся изменением параметров.
Внутренняя энергия(U) – сумма всех кинетических и потенциальных составляющих системы. (мах)
Известны 2 формы передачи энергии:
1. Упорядоченную форму передачи энергии называют работой;
2. Неупорядоченную форму передачи энергии называют теплотой.
Типы термодинамических систем:
1. Изолированная – это система, которая не обменивается с окружающей средой ни массой, ни энергией.
2. Закрытая – это система, которая не обменивается с определенной средой массой, но обменивается энергией (ампула с лекарством, термос).
3. Открытая – это система, которая обменивается массой и энергией с окружающей средой.
Типы термодинамических процессов:
1. Если Т=const, то ∆U=0 и ∆H=A – изотермический процесс. (внут.энергия не изменяется)
2. Если ∆H=0, ∆U=-А и -∆U=А – адиабатический процесс. (работа производится только за счет изменения внут.энергии системы)
3. Если А=0 (р∆V=0), то ∆H=∆U, Qv=∆U – изохорный процесс. (все тепло идет на изменение внутренней энергии, работы нет)
4. Если p=const - изобарный процесс.
Вопрос 2. Первое начало термодинамики. Энтальпия. Стандартная энтальпия образования, стандартная энтальпия сгорания. Закон Гесса. Термохимические процессы. Применение первого начала термодинамики к биосистемам. Примеры экзэргонических и эндэргонических процессов, протекающих в организме.
Первое начало термодинамики: (По своему существу первое начало термодинамики представляет собой закон сохранения и превращения энергии)
1. Энергия не создается и не уничтожается, возможно лишь превращение из одного вида в другой.
2. Вечный двигатель первого рода невозможен, т.е невозможно создать такой двигатель, который совершил бы работу без затраты энергии.
3. Внутренняя энергия изолированной системы есть величина постоянная.
Уравнение: Q=∆U+W (Q=∆U+p∆V)
Энтальпия – это то количество тепловой энергии, которое выделяется или поглощается при протекании процесса в условиях постоянства t и p(изобара) или t и V(изохора).
∆Н0хр= 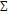 vj∆H0f(продуктов) -
vj∆H0f(продуктов) - 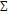 vi∆H0f(исх.вв)
vi∆H0f(исх.вв)
Стандартная энтальпия образования вещества (∆H0f) – изменение (уменьшение или увеличение) энтальпии, сопровождающее образование 1 моль вещества в стандартных условиях из простых веществ, взятых в устойчивых модификациях.
Стандартная энтальпия сгорания вещества (∆Н0с) равна уменьшению энтальпии при окислении в избытке кислорода 1 моль вещества, взятого в стандартном состоянии, до конечных продуктов окисления: оксида углерода(IV), воды, азота, оксида серы(IV).
Закон Гесса:
Теплота химической реакции , протекающей при постоянном объеме (или постоянном давлении) определяется только природой исходных веществ и продуктов реакции и не зависит от числа и последовательности промежуточных стадий, при условии, что теплоты измерены при одинаковой t.
Следствия из закона Гесса:
1. энтальпия образования любого соединения из простых веществ равна энтальпии его разложения на эти же вещества, но в обратным знаком ∆Н0обр= -∆Н0разл
2. энтальпия химической реакции равна разности сумм энтальпии образования продуктов реакции и исходных веществ ∆Н0хр= 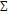 vi∆H0f(продуктов) -
vi∆H0f(продуктов) - 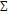 vj∆H0f(исх.вв)
vj∆H0f(исх.вв)
3. энтальпия химической реакции равна разности сумм энтальпии сгорания продуктов реакции и исходных веществ ∆Н0хр= 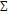 vi∆H0с(продуктов) -
vi∆H0с(продуктов) - 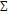 vj∆H0с(исх.вв)
vj∆H0с(исх.вв)
4. свободная энергия реакции равна разности сумм свободной энергии продуктов и исходных веществ ∆G0р= 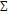 vi∆G0обр(продуктов) -
vi∆G0обр(продуктов) - 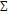 vj∆G0(исх.вв)
vj∆G0(исх.вв)
5.энтропия реакции ∆S0р= 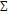 viS0обр(продуктов) -
viS0обр(продуктов) - 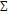 vjS0(исх.вв)
vjS0(исх.вв)
Термохимические процессы – переход системы из одного состояния в другое, сопровождающееся изменением параметров.
Применение первого начала термодинамики к биосистемам.
В 19 столетии было доказано экспериментально, что первый закон термодинамики применим к процессам, которые происходят в биологических системах.
Поступление пищи обеспечивает энергию, которая используется для выполнения различных функций организма или сохраняется для последующего использования. Энергия высвобождается из пищевых продуктов в процессе их биологического окисления, которое является многоступенчатым процессом. Энергия пищевых продуктов используется в клетках первоначально для синтеза макроэргических соединений - например, аденозинтрифосфорной кислоты (ATФ). ATФ, в свою очередь, может использоваться как источник энергии почти для всех процессов в клетке.
Пищевые вещества окисляются вплоть до конечных продуктов, которые выделяются из организма. Например, углеводы окисляются в организме до углекислого газа и воды. Такие же конечные продукты образуются при сжигании углеводов в калориметре:
C6H12O6 + 6O2 = 6CO2 + 6H2O
Величина энергии, высвобождаемой из каждого грамма глюкозы в этой реакции, составляет 4,1 килокалории (кКал). Столько же энергии, образуется при окислении глюкозы в живых клетках, несмотря на то, что процесс окисления в них является многоступенчатым процессом и происходит в несколько стадий. Этот вывод основан на принципе Гесса, который является следствием первого закона термодинамики: тепловой эффект многоступенчатого химического процесса не зависит от его промежуточных этапов, а определяется лишь начальным и конечным состояниями системы.
Таким образом, исследования с помощью калориметра показали среднюю величину физиологически доступной энергии, которая содержится в 1грамме трех пищевых продуктов (в килокалориях): углеводы - 4,1; белки - 4,1; жиры - 9,3.
С другой стороны, в конечном итоге вся энергия, поступившая в организм, превращается в теплоту. Также при образовании АТФ лишь часть энергии запасается, большая - рассеивается в форме тепла. При использовании энергии ATФ функциональными системами организма большая часть этой энергии также переходит в тепловую.
Оставшаяся часть энергии в клетках идёт на выполнении ими функции, однако, в конечном счёте, превращается в теплоту. Например, энергия, используемая мышечными клетками, расходуется на преодоление вязкости мышцы и других тканей. Вязкое перемещение вызывает трение, что приводит к образованию тепла.
Другим примером является расход энергии, передаваемой сокращающимся сердцем крови. При течении крови по сосудам вся энергия превращается в тепло вследствие трения между слоями крови и между кровью и стенками сосудов.
Следовательно, по существу вся энергия, потраченная организмом, в конечном счете, преобразуется в теплоту. Из этого принципа существует лишь единственное исключение: в случае, когда мышцы выполняют работу над внешними телами.
Если человек не выполняет внешней работы, то уровень высвобождения организмом энергии можно определить по величине общего количества теплоты, выделенной телом. Для этого применяют метод прямой калориметрии, для реализации которого используют большой, специально оборудованный калориметр. Организм помещают в специальную камеру, которая хорошо изолирована от среды, то есть не происходит обмена энергией с окружающей камеру средой. Количество теплоты, выделенной исследуемым организмом, можно точно измерить. Эксперименты, выполненные этим методом, показали, что количество энергии, поступающей в организм, равно энергии, выделяющейся при проведении калориметрии.
Прямая калориметрия в проведении трудоёмка, поэтому в настоящее время используют метод непрямой калориметрии, который основан на вычислении энергетического выхода организма по использованию им кислорода.
Примеры экзэргонических и эндэргонических процессов, протекающих в организме.
Термические реакции, при протекании которых происходит уменьшение энергии Г(dG<0) и совершается работа называются ЭКЗЕРГОНИЧЕСКИМИ(окисление глюкозы дикислородом- C6H12O6+6O2=6CO2+6H2O, dG=-2880 кДж/моль! Реакции в результате которых энергия Г возрастает (dG>0) и над системой совершается работа, наз-ся ЭНДЕРГОНИЧЕСКИМИ!
Вопрос 3. Второе начало термодинамики. Обратимые и необратимые в термодинамическом смысле процессы. Энтропия. Энергия Гиббса. Стандартная энергия Гиббса. Прогнозирование направления самопроизвольного процесса в изолированной и закрытой системах. Роль энтальпийного и энтропийного факторов.
Второй закон термодинамики:
1. Невозможен самопроизвольный переход от тела менее нагретого к более нагретому.
2. Невозможно превратить теплоту в работу не приводя никакого другого действия, кроме охлаждения источника тепла.
3. Вечный двигатель 2-го рода невозможен, т. е. такой двигатель, результатом которого было бы получение работы за счет тепла окружающей среды.
4.Все самопроизвольные процессы в макроскопических сис-мах протекают в направлении от менее вероятного к более вероятному состоянию сис-мы.
Обратимые– такие термодинамические процессы, при которых возвращение системы в первоначальное состояние не требует затраты энергии извне и связанных с этим изменений в окружающей среде.
Необратимые – термодинамические процессы, при которых возвращение системы в исходное состояние возможно лишь при условии затрат внешней энергии, что влечет за собой определенные изменения в окружающей среде.
Энтропия(S)характеризует меру беспорядка в расположении и поведении частиц составляющих сис-му, а также меру стремления частиц занять как можно больший V. Чем больше беспорядка, тем выше энтропия.
∆S0=∑vj(ню) S0(прод) - ∑vj(ню) S0(исх.в-в)
Энергия Гиббса(G) - часть внутренней энергии системы которая может быть переведена в работу.
Под стандартной энергией Гиббса образования ΔG°, понимают изменение энергии Гиббса при реакции образования 1 моль вещества, находящегося в стандартном состоянии. Это определение подразумевает, что стандартная энергия Гиббса образования простого вещества, устойчивого в стандартных условиях, равна нулю.
В самопроизвольной реакции:
∆G<0 (G2-G1<0) ∆G>0
∆S>0 (S2-S1>0) реакция пойдет → ∆S<0 реакция пойдет ←
Формула для I и II т/д:
∆Gт=∆H0хр - Т∆S
Кинетические уравнения.
Зависимость скорости химической реакции от концентрации описывается кинетическим уравнением. Например, для реакции:
аА + ЬВ → продукты
v = kc(A)рс(B)q,
где р, q — эмпирические, т. е. найденные экспериментальным путем коэффициенты, не обязательно совпадающие со стехиометрическими коэффициентами а и Ь, к — константа скорости реакции, размерность которой зависит от значений р, q. Константа скорости зависит от тех же факторов, что и скорость химической реакции, но не зависит от концентрации.
Порядок реакции – число, равное сумме показателей степеней концентраций реагирующих веществ в кинетическом уравнении реакции. Порядок реакции характеризует формально кинетическую зависимость скорости реакции от концентрации реагирующих веществ, а молекулярность – элементарный механизм отдельных стадий сложного процесса.
Вопрос 5. Зависимость скорости реакции от концентрации реагентов. Кинетические уравнения реакций первого, второго и нулевого порядков.
Закон действующих масс(Гультберг, Вааге):
Скорость химической реакции пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов.
V=kCaA*CbB
k – константа скорости хим р-ции (отвечает за природу химических веществ, агрегатное состояние)
С – молярная концентрация
Зависимость скорости химической реакции от концентрации описывается кинетическим уравнением. Например для реакции:
 aA + bB продукты
aA + bB продукты
V=kc(A)в степени p * c(B) в степени q
Где p,q – найденные экспериментальным путем коэффициенты
k-константа скорости реакции, размерность которой зависит от значений p,q
C-концентрации реагентов А и В
a, b – стехиометрические коэффициенты
Константа скорости есть величина постоянная, не зависящая от концентрации реагентов.
При представлении концентрационной зависимости скорости в виде закона действующих масс предполагается, что скорость зависит от концентрации реагентов А и В. Физический смысл константы скорости реакции нетрудно установить – она численно равна скорости реакции, в которой концентрации реагирующих веществ равна 1 моль\ л или их произведения равно единице:
Если (А) = (В) = 1 моль\л = V = k *1 * 1 , т.е. V = k.
Это скорость данной реакции в стандартных условиях.
Порядок реакции - это число равное сумме показателей степеней концентраций реагирующих веществ в кинетическом уравнении реакции. Порядок реакций характеризует формально кинетическую зависимость скорости реакции от концентрации реагирующих веществ. Реальный порядок реакций устанавливается экспериментальным путем и часто не совпадает с теоретическим.
Реакции нулевого порядка:
-dc/dt =k откуда С0 – Сt =kt
По нулевому порядку проходят следующие процессы:
-фотохимические реакции, скорость которых определяется количеством поглощенного света.
- каталитические реакции, скорость которых зависит от концентрации только катализатора
-реакции, в которых убыль исходного вещества постоянно восполняется его поступлением из другой фазы.
Прямая идет параллельно оси абсцисс, tg( альфа )=0, т.е. p + q =0
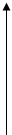 V
V
 | |||
 |
C
Реакции первого порядка: втом случае если угол наклона прямой на графике составляет 45 градусов, tg= 1
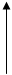

 -dc/dt=kc
-dc/dt=kc
v
c
Реакции второго порядка:
-dc/dt=kt(в квадрате)
График кривая
Вопрос 6. Зависимость скорости реакции от температуры. Температурный коэффициент скорости реакции и его особенности для биохимических процессов. Понятие о теории активных соударений. Энергетический профиль реакции; энергия активации; уравнение Аррениуса.
Зависимость скорости реакции от температуры.
1. Правило Вант-Гоффа: скорость большинства реакций увеличивается приблизительно в 2-4 раза при увеличении температуры на 100С: Vt2=Vt1*γt2-t1/10, где γ – температурный коэффициент константы скорости реакции(in vitro - в стекле, стакане, вне γ=(2-4), in vivo – внутри γ=(15-9))
2. Уравнение Аррениуса для константы скорости: k=Ae-Ea/RT, где Еа (энергия активации Дж/моль) и А – постоянные, не зависящие от температуры величины, R – универсальная газовая постоянная, Т – абсолютная температура.
Уравнение, которое часто используют для различных расчетов, получают путем неопределенного интегрирования : k=А*e(-E/RT), где k – константа (моль*л/сек), А – предэкспотенциальный множитель, где Еа - энергия активации (Дж/моль).
Теория активных соударений (Аррениус):
1. Реакционноспособными являются не все молекулы, а только те, которые находятся в особом активном состоянии.
2. Активные молекулы образуются из обычных в результате протекания обратимого процесса поглощения энергии.
3. Активные молекулы превращаются в молекулы конечного продукта со скоростью, не зависящей от температуры.
4. Влияние температуры на скорость химического процесса сводится к смещению равновесия между обычными и активными молекулами в сторону увеличения концентрации последних.
Энергия активации – это тот энергетический барьер, который должны преодолеть исходные вещества по пути превращения в продукты реакции.
Вопрос 8. Химическое равновесие. Обратимые и необратимые по направлению реакции. Термодинамические условия равновесия. Константы химического равновесия. Прогнозирование смещения химического равновесия.
Химическое равновесие: динамическое состояние, при котором скорость прямой и обратной реакций равны.
Обратимая р-ция: при данных условиях самопроизвольно протекающая как в прямом, так и в обратном направлении.
Необратимая р-ия: при данных условия протекает в одном направлении.
Образуется:
- Труднорастворимый осадок
- газ
- малодиссоциирующее в-во (вода)
- устойчивое комплексное соединение
Термодинамические условия равновесия:
G2-G1=0
S2-S1=0
Константа равновесия: при постоянных внешних условиях в равновесии отношение произведение концентраций продуктов к произведению концентраций реагентов с учетом стехиометрии есть величина постоянная, не зависящая от химического состава системы.
Количественной характеристикой состояния равновесия является константа химического равновесия К, которая определяется отношением констант скоростей прямой и обратной реакцией
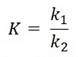
В подавляющем большинстве случаев константы скоростей прямой и обратной реакций не равны. Константа равновесия – постоянная при данной температуре величина и определяет соотношение между равновесными концентрациями продуктов реакции и исходных веществ, возведенных в степени их стехиометрических коэффициентов.
Например, для процесса N2 + 3H2 ↔ 2NH3
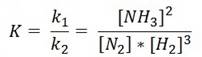
Принцип Ле-Шателье: воздействие какого-либо фактора (t, c, p) на равновесную систему стимулирует смещение равновесия в таком направлении, которое способствует восстановлению первоначальных характеристик системы.
| Положение химического равновесия зависит от следующих параметров реакции: температуры, давления и концентрации. Влияние, которое оказывают эти факторы на химическую реакцию, подчиняются закономерности, которая была высказана в общем виде в 1884 году французским ученым Ле-Шателье .Современная формулировка принципа Ле-Шателье такова:Если на систему,находящуюся в состоянии равновесия, оказать внешнее воздействие, то система перейдет в другое состояние так, чтобы уменьшить эффект внешнего воздействия. |
Роль воды и растворов в жизнедеятельности. Физико-химические свойства воды, обуславливающие её уникальную роль как единственного биорастворителя; влияние внешних условий на растворимость. Термодинамика растворения.
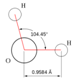 Вода состоит из атомов водорода (в трех изотопах 1,2,3) и кислорода (в трех изотопах 16,17,18). Составляет основную часть внутренней среды организма, обеспечивает процессы всасывания, передвижения питательных веществ и продуктов обмена по организму. Кроме того, вода участвует в процессе терморегуляции (потоотделение) и в процессе дыхания (человек может дышать абсолютно сухим воздухом, но не долго).
Вода состоит из атомов водорода (в трех изотопах 1,2,3) и кислорода (в трех изотопах 16,17,18). Составляет основную часть внутренней среды организма, обеспечивает процессы всасывания, передвижения питательных веществ и продуктов обмена по организму. Кроме того, вода участвует в процессе терморегуляции (потоотделение) и в процессе дыхания (человек может дышать абсолютно сухим воздухом, но не долго).
Свойства:
1)Вода - единственное известное вещество, которое встречается в естественных условиях в твердом, жидком и газообразном состоянии.
2)Вода - уникальный растворитель, т.к. диэлектрическая проницаемость воды (Е в единицах СГСЭ) 81,0 при 20 гр..С. У большинства других тел она находится в пределах 2 - 3, за исключением ряда кислот (муравьиная - 58, ацетон - 21) и цианистого водорода, у которого диэлектрическая проницаемость 107.
3)Воду очень трудно окислить, сжечь или разложить на составные части. Вода - химически стойкое вещество.
4)Вода имеет редкую способность при замерзании расширяться, вследствие чего лед плавает на воде, остающейся в жидкой фазе. Только немногие вещества (висмут, галлий, германий и др.) имеют такую же аномалию, при которой твердая фаза легче жидкой.
5)Вода в форме сферических капель имеет наименьшую поверхность при заданном объеме. Поверхностное натяжение (на границе с воздухом при 20 гр. С равно 72,75 дин/см) является необходимым условием капиллярных процессов, столь важных для жизнедеятельности растений и животных.
6)Вода обладает способностью поглощать большое количество теплоты и сравнительно мало при этом нагреваться.
7)Поверхностное натяжение - это степень сцепления молекул воды друг с другом. Чем ниже поверхностное натяжение, тем выше растворяющая способность воды, тем лучше вода выполняет свои основные функции. В том числе и роль транспортной системы. Чем ниже поверхностное натяжение, тем выше растворяющие свойства, тем выше текучесть.
8)Кислотно-щелочное равновесие воды. Основные жизненные среды (кровь, лимфа, слюна, межклеточная жидкость, спинномозговая жидкость и др.) имеют слабощелочную реакцию. При сдвигах их в кислую сторону, меняются биохимические процессы, организм закисляется.
9)Структура воды. Вода представляет собой жидкий кристалл. Диполи молекулы воды ориентируются в пространстве определенным образом, соединяясь в структурные конгломераты. Это позволяет жидкости составлять единую биоэнергоинформационную среду. Когда вода находится в состоянии твердого кристалла (льда), молекулярная решетка жестко ориентирована. При таянии разрываются жесткие структурные молекулярные связи. И часть молекул, высвобождаясь, образует жидкую среду. В организме вся жидкость структурирована особым образом.
10)Информационная память воды. За счет структуры кристалла происходит запись информации, исходящей от биополя. Это одно из очень важных свойств воды, имеющее большое значение для всего живого.
Растворимость различных веществ в определённом растворителе зависит от внешних условий, прежде всего - от температуры и давления. Давление наиболее сильно сказывается на растворимость газов. Изменение внешних условий влияет на растворимость в соответствии с принципом смещения равновесий Ле-Шателье: воздействие какого-либо фактора (t, c, p) на равновесную систему стимулирует смещение равновесия в таком направлении, которое способствует восстановлению первоначальных характеристик системы.
Влияние температуры зависит от знака теплового эффекта реакции. При повышении температуры химическое равновесие смещается в направлении эндотермической реакции, при понижении температуры — в направлении экзотермической реакции.
Влияние давления.При повышении давления равновесие сдвигается в направлении, в котором уменьшается суммарное количество молей газов и наоборот.
Влияние концентрации. При повышении концентрации одного из исходных веществ равновесие сдвигается в направлении образования продуктов реакции. При повышении концентрации одного из продуктов реакции равновесие сдвигается в направлении образования исходных веществ.
Согласно второму началу термодинамики при р, Т = const вещества самопроизвольно могут растворяться в каком-либо растворителе, если в результате этого процесса энергия Гиббса системы уменьшается, т. е. ΔG = (ΔН – TΔS) < 0.
Величину ΔН называют энтальпийным фактором, а величину TΔS – энтропийным фактором растворения.
При растворении жидких и твердых веществ энтропия системы обычно возрастает (ΔS > 0), так как растворяемые вещества из более упорядоченного состояния переходят в менее упорядоченное. Вклад энтропийного фактора, способствующий увеличению растворимости, особенно заметен при повышенных температурах, потому что в этом случае множитель Т велик и абсолютное значение произведения TΔS также велико, соответственно возрастает убыль энергии Гиббса.
При растворении газов в жидкости энтропия системы обычно уменьшается (ΔS < 0), так как растворяемое вещество из менее упорядоченного состояния (большого объема) переходит в более упорядоченное (малый объем). Снижение температуры благоприятствует растворению газов, потому что в этом случае множитель Т мал и абсолютное значение произведения TΔS будет тем меньше, а убыль энергии Гиббса тем больше, чем ниже значение Т.
В процессе образования раствора изменение энтальпии процесса растворения нужно рассматривать в соответствии с законом Гесса как алгебраическую сумму эндо– и экзотермических вкладов всех процессов, сопровождающих процесс растворения. Иначе говоря, изменение энтальпии представляет собой алгебраическую сумму изменения энтальпии ΔНкр в результате разрушения кристаллической решетки и изменения энтальпии ΔНсол за счет сольватации (взаимод. молекул растворенного в-ва с молекулами р-рителя) частицами растворителя:
ΔНраств = ΔНкр + ΔНсол,где ΔНраств – изменение энтальпии при растворении.
При растворении твердых веществ с молекулярной кристаллической структурой и жидкостей молекулярные связи не очень прочные, и поэтому обычно ΔНсол > ΔНкр Это приводит к тому, что растворение, например, спиртов и сахаров представляет собой экзотермический процесс (ΔНраств < 0).
При растворении твердых веществ с ионной решеткой соотношение энергий Екр и Есол могут быть различным. Однако в большинстве случаев энергия, выделяемая при сольватации ионов, не компенсирует энергию, затрачиваемую на разрушение кристаллической решетки, следовательно, и процесс растворения является эндотермическим.
10. Понятие об идеальном растворе. Константа растворимости. Условия растворения и образования осадков.
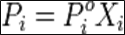 Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
Первый закон Рауля связывает давление насыщенного пара над раствором с его составом; он формулируется следующим образом:
Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причём коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом.
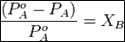 Для бинарного раствора, состоящего из компонентов А и В (компонент А считаем растворителем) удобнее использовать другую формулировку:
Для бинарного раствора, состоящего из компонентов А и В (компонент А считаем растворителем) удобнее использовать другую формулировку:
Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе.
Растворы, для которых выполняется закон Рауля, называются идеальными. Идеальными при любых концентрациях являются растворы, компоненты которых очень близки по физическим и химическим свойствам (оптические изомеры, гомологи и т. п.), и образование которых не сопровождается изменением объёма и выделением либо поглощением теплоты. В этом случае силы межмолекулярного взаимодействия между однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Константа растворимости (ПР, Ksp) — произведение концентрации ионов малорастворимого электролита в его насыщенном растворе при постоянной температуре и давлении. Произведение растворимости — величина постоянная.
При постоянной температуре в насыщенных водных растворах малорастворимых электролитов устанавливается равновесие между твердым веществом и ионами, образующими это вещество. Например, в случае для CaCO3 это равновесие можно записать в виде:
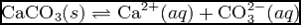
Константа этого равновесия рассчитывается по уравнению:
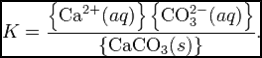
В общем виде, произведение растворимости для вещества с формулой AmBn, которое диссоциирует на m ионов An+ и n ионов Bm-, рассчитывается по уравнению:
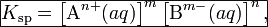
где [An+] и [Bm-] — равновесные молярные концентрации ионов, образующихся при электролитической диссоциации.
Данное уравнение не учитывает коэффициенты активности, то есть степень влияния ионных сил. Для растворов с концентрациями большими, чем 1×10−4 моль/л необходимо использовать произведение активностей:
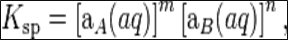 где аA и аB — активности ионов A и B.
где аA и аB — активности ионов A и B.
Произведение активностей ионов для насыщенных растворов малорастворимых электролитов при данной температуре постоянная величина. Она зависит от температуры и природы растворителя.
Произведение растворимости связано с растворимостью следующим соотношением:
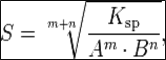 где:m+n — суммарное количество молей катионов и анионов
где:m+n — суммарное количество молей катионов и анионов
m —количество молей катиона
n — количество молей аниона
Ksp — произведение растворимости
S — растворимость вещества (моль/л)
Образование осадка происходит, если:
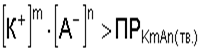 Это достигается прибавлением избытка электролита, содержащего одноименный ион K+ или A-.
Это достигается прибавлением избытка электролита, содержащего одноименный ион K+ или A-.
Например, если в раствор малорастворимого электролита СаСО3 внести хорошо растворимый сильный электролит Nа2СО3, то повысится концентрация иона СО32- и понизится концентрация иона Ca2+ и следовательно, снизится растворимость СаСО3, таким путем можно осаждать малорастворимые соединения.
Растворение осадка происходит, если:
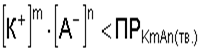 Это происходит, если связывается один из ионов, посылаемых осадком в раствор.
Это происходит, если связывается один из ионов, посылаемых осадком в раствор.
Например, растворение электролита FeS происходит при добавлении раствора соляной кислоты HCl. Ионы водорода связывают ионы S2- в молекулы H2S, которые удаляются в виде газа. Произведение концентрации ионов Fe2+ и S2- становится меньше произведения растворимости сульфида железа, и осадок растворяется.
Зная величину ПР, можно регулировать образование или растворение осадка, также оценить выпадает ли в данных условиях осадок. Для этого концентрацию ионов подставляют в выражение:
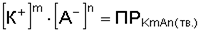 и полученную величину сравнивают со справочной. Осадок выпадет, если полученная величина ПР превышает табличную.
и полученную величину сравнивают со справочной. Осадок выпадет, если полученная величина ПР превышает табличную.
11.
Коллигативные свойства растворов- такие свойства растворов, которые зависят в основном от концентрации растворенных частиц и в значительно меньшей степени от их размера, молярной массы и других свойств. Проникновение воды через животную мембрану из конц. раствора, т.е. то, что мы называем осмосом, впервые описал Ноле. Блегден установил, что понижение температуры замерзания растворителя зависит от массы растворенного вещества. Оба явления-понижение температуры замерзания растворителя и осмос – следствия проявления общего закона, в соответствие с которым давление насыщенного пара растворителя над раствором нелетучего вещества меньше давления насыщенного пара над чистым растворителем при тойже температуре.
Закон Рауля: Первый закон Рауля
Давление пара раствора, содержащего нелетучее растворенное вещество, прямо пропорционально мольной доле растворителя в данном растворе:
p = p0 · χр-ль, где
p — давление пара над раствором, ПА;
p0 — давление пара над чистым растворителем;
χр-ль —— мольная доля растворителя.
Для растворов электролитов используют несколько другую форму уравнения, позволяющую добавить в неё изотонический коэффициент:
Δp = i · p0 · χв-ва, где
Δp — собственно изменение давления по сравнению с чистым растворителем;
χв-ва — мольная доля вещества в растворе
Второй закон Рауля
Тот же Рауль экспериментально доказал, что
повышение температуры кипения раствора по сравнению с температурой кипения растворителя, а равно и понижение температуры замерзания раствора по сравнению с аналогичным характеризующей величиной для растворителя прямо пропорциональна моляльности раствора, то есть,
ΔTкип/зам= Kэб/кр · mв-ва, где
Kэб/кр — соответственно эбулиоскопическая (от лат. ebullire — «кипеть» и др.-греч. σκοπέω — «наблюдаю») и криоскопическая (относится к замерзанию) константы, характерные для данного растворителя;
mв-ва — моляльность вещества в растворе.
Растворы электролитов
Законы Рауля не выполняются для растворов (даже бесконечно разбавленных), которые проводят электрический ток — растворов электролитов. Для учёта этих отклонений Вант-Гофф внёс в приведённые выше уравнения поправку — изотонический коэффициент i, неявно учитывающий диссоциацию молекул растворённого вещества:
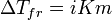 ;
; 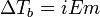
Неподчинение растворов электролитов законам Рауля и принципу Вант-Гоффа послужили отправной точкой для создания С. А. Аррениусом теории электролитической диссоциации.
Изоосмия, изотония (от изо... и греч. osmós — толчок, tónos — напряжение), относительное постоянство осмотического давления в жидких средах и тканях организма, обусловленное поддержанием на данном уровне концентраций содержащихся в них веществ: электролитов, белков и т. д. И. — одна из важнейших физиологических констант организма, обеспечиваемых механизмами саморегуляции (см. Гомеостаз). Отклонение осмотического давления от нормального физиологического уровня " 0,76—0,81 Мн/м2(7,6—8,1 ат) влечёт за собой нарушение обменных процессов между кровью и тканевой жидкостью.
Роль осмоса: явление переноса из раствора с меньшей С в большую. Так осуществляется обмен молекулами между клеткой и внешней средой)
Гемолиз- разрушение- лопаются клетки в гипотоническом растворе
Плазмолиз-сморщивание клеток)
12.
Для неэктролитов i=1,Для электролитов I больше 1, причем с разбавлением раствора I растет ,
