Все химические реакции можно разделить на два типа.
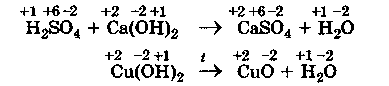 – к первому типу относятся реакции, которые идут без изменения степени окисления атомов реагирующих веществ. Это реакции обмена и некоторые реакции соединения и разложения. Например:
– к первому типу относятся реакции, которые идут без изменения степени окисления атомов реагирующих веществ. Это реакции обмена и некоторые реакции соединения и разложения. Например:
В этих случаях степень окисления каждого из атомов до и после реакции остается без изменения.
– ко второму типу относятся реакции, которые идут с изменением степени окисления атомов реагирующих веществ.
Окислительно-восстановительная реакция (ОВР)−это единый процесс, состоящий из двух разных полуреакций: полуреакции окисления и полуреакции восстановления, которые идут одновременно.
Окисление− это процесс потери электронов атомом, молекулой или ионом. Восстановление− это процесс присоединения электронов атомом, молекулой или ионом.
Окислителем называется вещество, атомы, молекулы или ионы которого присоединяют электроны:
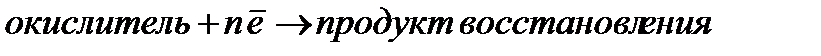
Окислитель восстанавливается в процессе восстановления.
Восстановителем называется вещество, атомы, молекулы или ионы которого отдают электроны:
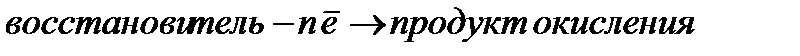
Восстановитель окисляется в процессе окисления.
Число электронов, отданных восстановителем, равно числу электронов, принятых окислителем.
Атомы в высшей степени окисления могут быть только окислителями.
Атомы в низшей степени окисления могут быть только восстановителями.
№14
Типы окислительно-восстановительных реакций:
Межмолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl
Внутримолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
2H2O → 2H2 + O2
Диспропорционирование (самоокисление-самовосстановление) — реакции, в которых один и тот же элемент выступает и как окислитель, и как восстановитель, например:
Cl2 + H2O → HClO + HCl
Репропорционирование (конпропорционирование) — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления, например:
NH4NO3 → N2O + 2H2O
В качестве типичных окислителей могут выступать:
1) простые вещества, образуемые атомами с большой электроотрицательностью, т. е. типичные неметаллы, расположенные, прежде всего, в главных подгруппах шестой и седьмой групп периодической системы;
2) вещества, содержащие элементы в высших и промежуточных положительных степенях окисления, в том числе в виде ионов, как простых, элементарных (Fе3+), так и кислородсодержащих, оксоанионов (перманганат-ион);
3) перекисные соединения (пероксиды, супероксиды и т. д.);
4) Кислородсодержащие анионы, содержащие атом неметалла в высшей положительной степени окисления (SO4 (степень окисления серы +6), NO3 (степень окисления азота +5)
К ним относятся F2, Cl2, O2, KClO3, H2SO4, HNO3, KMnO4, MnO2, K2Cr2O7, PbO2 и др.
В качестве восстановителей могут выступать простые или сложные вещества, содержащие атомы, которые находятся не в высшей из возможных для них степени окисления, а потому могут повышать свою степень окисления.
В качестве типичных восстановителей могут выступать:
1) простые вещества, атомы которых имеют низкую электроотрицательность («активные» металлы);
2) катионы металлов в низших степенях окисления (Fе2+);
3) простые, элементарные анионы, например сульфид-ион;
4) кислородсодержащие анионы (оксоанионы), соответствующие низшим положительным степеням окисления элемента (нитрит, сульфит);
5) катод электролизной ячейки.
Вещества, применяемыми на практике в качестве восстановителей, являются, щелочные и щелочноземельные металлы, сульфиды, сульфиты, галогеноводороды (кроме НF), соли двухвалентного железа, органические вещества - формальдегид, глюкоза, щавелевая кислота, а также водород, углерод, монооксид углерода и алюминий при высоких температурах.
Типичными (сильными) восстановителями являются H2, C (графит), Zn, Al, Ca, KI, HCl (конц.), H2S, CO и др.
При написании уравнений ОВР используют два метода расстановки коэффициентов: метод электронного баланса и метод полуреакций.
Метод электронного баланса (окислительных чисел) рассмотрим на примере реакции

Для расстановки коэффициентов выполняем следующие действия.
1. Определяем элементы, атомы которых изменяют степень окисления:

2. Находим окислитель и восстановитель в данной ОВР и пишем отдельно электронные уравнения процессов окисления и восстановления:


3. Уравниваем число электронов в процессе окисления и восстановления (электронный баланс):

4. Коэффициенты 5 и 2 из электронных уравнений переносим в молекулярное уравнение ОВР:

5. Окончательно уравниваем число атомов каждого элемента в обеих частях молекулярного уравнения:

Mетод полуреакций (ионно-молекулярный метод) основан на составлении уравнений процессов окисления и восстановления с помощью ионов и молекул, реально существующих в растворе.
Сильные электролиты записывают в виде ионов, а слабые электролиты, газы и малорастворимые вещества − в виде молекул. Степень окисления атомов не используют, а учитывают заряды реальных ионов и характер среды, в которой идет процесс окисления или восстановления. Алгебраическую сумму зарядов в левой и правой частях полуреакций (процессов окисления и восстановления) уравнивают с помощью определенного числа электронов, которые участвуют в процессе. После записи полуреакций окисления и восстановления уравнивают число электронов, отданных восстановителем и принятых окислителем с помощью дополнительных коэффициентов (как в методе электронного баланса). С учетом этих коэффициентов записывают сокращенное ионно-молекулярное уравнение, а затем и молекулярное уравнение ОВР.
Используем метод полуреакций для той же реакции:


Чтобы связать 4 моль атомов кислорода, требуется 8 моль атомов водорода (процесс идет в кислой среде):

Уравниваем алгебраическую сумму зарядов слева и справа:


Чтобы получить 1 моль атомов кислорода для окисления SO32-до SO42-, требуется 1 моль молекул H2O (процесс идет в кислой среде):

Уравниваем алгебраическую сумму зарядов слева и справа:

Теперь уравниваем число электронов в полуреакциях окисления и восстановления и получаем сокращенное ионно - молекулярное уравнение ОВР:

Записываем молекулярное уравнение ОВР:

№15
Органическая химия – наука, изучающая соединения углерода, называемые органическими веществами. В связи с этим органическую химию называют также химией соединений углерода.
Важнейшие причины выделения органической химии в отдельную науку заключаются в следующем.
1.Многочисленность органических соединений по сравнению с неорганическими соединениями.
2. Органические вещества имеют исключительное значение как вследствие их крайне многообразного практического применения, так и потому, что они играют важнейшую роль в процессах жизнедеятельности организмов.
3. Имеются существенные отличия в свойствах и реакционной способности органических соединений от неорганических, вследствие чего возникла необходимость в развитии многих специфических методов исследования органических соединений.
Предметом органической химии является изучение способов получения, состава, строения и областей применения важнейших классов органических соединений.
