Основные этапы развития представлений о строении атомы и ядра. Квантово-механическая модель атома.
Английский физик Э.Резерфорд в 1911 г. предложил ядерную (планетарную) модель строения атома. Согласно этой модели, атом состоит из положительно заряженного ядра, в котором сосредоточена почти вся масса атома. Вокруг ядра на значительном расстоянии от него вращаются электроны, образующие электронную оболочку атома. Размер всего атома около 10-10 м, ядра – порядка 10-15 м, т.е. по размеру ядро примерно в 100 000 раз меньше атома.
Атом в целом электронейтрален, поэтому суммарный заряд электронов должен быть равен заряду ядра. Дальнейшие исследования показали, что положительный заряд ядра атома численно равен порядковому номеру элемента в Периодической системе Менделеева.
Положительный заряд ядра каждого атома, а также число движущихся в атоме электронов равны атомному номеру элемента.
Ядро атома водорода – элементарная частица, которую называют протоном. В настоящее время в ядре атома открыты различные элементарные частицы. Важнейшими из них являются протоны (р) и нейтроны (n).
| Частица | Символ | Масса покоя | Заряд | |
| г | а.е.м. | |||
| Протон | р | 1,679*10-24 | 1,007 | +1 |
| Нейтрон | n | 1,675*10-24 | 1,008 | |
| Электрон | e | 9,108*10-28 | 0,0005 | -1 |
Советские ученые Иваненко и Гапон создали протонно-нейтронную теорию строение ядра (1932 г.) . Согласно этой теории, ядра всех атомов, кроме ядра атома водорода, состоят из Z протонов и (А- Z) нейтронов, где Z – атомный номер элемента; А – массовое число.
Массовое число А равно сумме числа протонов Z и нейтронов N в ядре атома, т.е. А= Z+ N.
Силы, удерживающие протоны и нейтроны в атоме называются ядерными.
Разновидности атомов одного элемента, обладающие одинаковыми зарядами ядер, но разными атомными массами, называются изотопами.
Каждый изотоп характеризуется двумя величинами: атомной массой (записывается вверху слева от химического знака) и зарядом ядра (записывается внизу слева от химического знака).
Атомная масса элемента равна среднему значению масс всех его природных изотопов с учетом их распространенности в природе.
Атомная масса элемента зависит от состава ядра. Заряд ядра, численно равный порядковому номеру элемента, определяет состав атома, число электронов в электронной оболочке атома, ее строение, а тем самым и свойства химического элемента. Именно заряд ядра, а не атомная масса является самой главной характеристикой атома, а значит, и элемента.
Химический элемент – это определенный вид атомов с одинаковым зарядом ядра.
Билет
Электронное облако — это наглядная модель, отражающая распределение электронной плотности в атоме или молекуле. В качестве наглядной модели состояния электрона в атоме в химии принят образ облака, плотность соответствующих участков которого пропорциональна вероятности обнаружить там электрон. Электронное облако рисуется наиболее плотным (там, где наибольшее число точек) в областях наиболее вероятного обнаружения электрона. Так как электрон несет отрицательный заряд, то его орбиталь представляет собой определенное распределение заряда, которое получило название электронного облака.
Волновая функция:
Вероятность нахождения электрона в определённой области пространства описывается волновой функцией , которая характеризует амплитуду волны, как функцию координат электрона. В наиболее простом случае эта функция зависит от трёх пространственных координат и называется орбиталью. В соответствии с определением волновой функции, орбиталью называется область околоядерного пространства, в котором наиболее вероятно нахождение электрона.
Билет
Квантовые числа:
Для характеристики поведения электрона в атоме введены квантовые числа: главное, орбитальное, магнитное и спиновое.
Главное квантовое число п определяет энергию и размеры электронных орбиталей, принимает значения 1,2,3,4… и характеризует оболочку или энергетический уровень. Чем больше п, тем выше энергия. Оболочки (уровни) имеют буквенные обозначения:K (n=1), L (n=2), M (n=3), N (n=4), Q (n=5).
Орбитальное l – определяет форму атомной орбитали. Электронные оболочки расщеплены на подоболочки, поэтому орбитальное квантовое число также характеризует энергетические подуровни в электронной оболочке атома. Орбитальные кв. числа принимают целочисленные значения от 0 до (п-1). Подоболочки также обозначаются буквами: подоболочка (подуровень).
Электроны с орбитальным кв. числом 0 называются s- электронами, имеют сферическую форму.
Электроны с орбитальным кв. числом 1 называются р- электронами, форма, напоминающая гантель.
Электроны с орбитальным кв. числом 2 называются d- электронами, форма сложнее чем р- орбитали.
Электроны с орбитальным кв. числом 2 называются f - электронами, форма сложнее чем d- орбитали.
Магнитное кв. число т1 характеризует ориентацию орбитали в пространстве. Принимает целые значения от -1 до +1, включ 0.
Спиновое кв.число тs характеризует собственное вращательное движение электрона вокруг собственной оси, т.е. показывает величину и ориентацию спина, имеет только 2 значения +1/2 и -1/2.
Билет
При заполнении атомных орбиталей электронами облюдаются три основные правила.
Заселение атомных орбиталей электронами определяется правилом минимума энергии, принципом Паули и правилом Хунда.
Электроны заселяют атомные орбитали, начиная с подуровня с меньшей энергией. В этом состоит правило минимума энергии. Последовательность в нарастании энергии подуровней акова: 1s < 2s < 2p < 3s < 3p < 4s ≤ 3d < 4p < 5s и так далее …
Правило Клечковского. Заполнение уровней и подуровней происходит в порядке возрастания суммы главного и орбитального квантовых чисел. Если для двух орбиталей эта сумма будет одинакова, то электрон идет в ту орбиталь, где n меньше.
1s < 2s < 2p < 3s < 3p < 4s < 3d ...
Принцип Паули. На одной атомной орбитали могут находиться не более двух электронов с противоположными спинами и с набором всех 4-х квантовых чисел.
Правило Гунда. Суммарный спин электронов на подуровне должен быть максимален, т.е. электроны стремятся занять максимальное число свободных квантовых состояний.
Билет
Емкость – максимальное число энергетического уровня, определяющееся по формуле 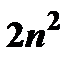 , где n – номер уровня. Емкость подуровня
, где n – номер уровня. Емкость подуровня 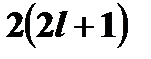 , где l – орбитальное квантовое число характеризующееся для данного подуровня.
, где l – орбитальное квантовое число характеризующееся для данного подуровня.
