Лабораторно-практическое занятие № 25. «Фенолы. Ароматические спирты. Хиноны» (2ч)
Цель:сформировать знания о строении, свойствах получении и идентификации фенолов, познакомиться с особенностями ароматических спиртов и хинонов
Вопросы для обсуждения:
1. Фенолы, их реакционные свойства и центры.
2. Кислотно-основные свойства фенолов.
3. Реакции с участием нуклеофильного и электрофильного центров.
4. Реакции электрофильного замещения в ароматическом ядре.
5. Окисление и восстановление фенолов.
6. Получение и идентификация фенолов.
7. Особенности ароматических спиртов и хинонов.
Материалы и примеры для самостоятельного изучения
Пример 1. Объясните, как осуществить нитрование фенола до пикриновой кислоты.
Решение. Фенол при взаимодействии с разбавленной азотной кислотой при комнатной температуре образует смесь орто- и пара-нитрофенолов, которая легко разделяется перегонкой с паром вследствие более высокой летучести opmo-изомера, образующего внутримолекулярную водородную связь:
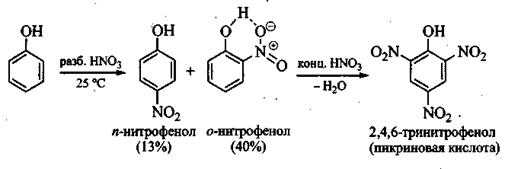
Дальнейшим нитрованием смеси действием конц. HNO3 можно получить пикриновую кислоту, о которой шла речь в предыдущей главе. Прямое нитрование фенола с помощью конц. HNO3 осложняется его окислением. Для сравнения: нитрование бензола возможно только конц. HNO3 или смесью конц. НNО3 и конц. H2SO4.
Пример 2. В чем особенности окисления фенола? В чем причина «порозовения» фенола при хранении?
Есть принципиальное отличие в отношении к окислителям спиртов и фенолов, которое связано со структурой первичного продукта окисления. Если в фенолах окисление идет по более слабой связи О-Н (Ео-н = 355,6 кДж/моль, Ес-н = = 430,9 кДж/моль), то в спиртах, наоборот, реакция идет по более слабой связи С 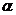 -Н (Ео-н = 427 кДж/моль, Е с(
-Н (Ео-н = 427 кДж/моль, Е с( 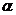 )-н =371 кДж/моль, E с(
)-н =371 кДж/моль, E с( 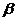 )-н = 405,8 кДж/моль).
)-н = 405,8 кДж/моль).
Для первичного продукта окисления фенола — фенокси-радикала (арокси-радикал для производных фенола) — характерна резонансная стабилизация, что делает его более стабильным по сравнению с AlkO. радикалами.
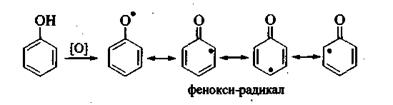
При наличии в орто-положениях фенола объемных заместителей (пространственно-затрудненные фенолы) арокси-радикалы дополнительно стабилизируются из-за пространственных затруднений доступа к ароксильному кислороду других реагентов.
Дальнейшая судьба арокси-радикалов зависит от строения фенола и условий реакции.
Пространственно-затрудненные фенолы (ПЗФ) в радикально-цепных процессах обрывают цепь за счет дезактивации активного радикала и превращения, в стабильный арокси-радикал, не способный продолжать цепной процесс.
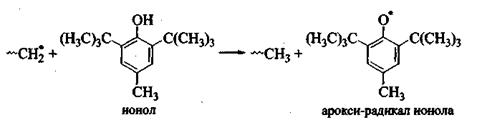
Таким образом, являясь ингибиторами цепных радикальных реакций, ПЗФ широко используются для замедления процессов окисления (то есть как антиоксиданты), старения, разрушения, деструкции самых разнообразных материалов и объектов — машинных, пищевых масел, жидкого топлива, полимеров, биологических органов (лекарства) и др. .
Димеризация арокси-радикалов по типу «хвост - хвост» с последующим окислением димера приводит к образованию окрашенных в красный цвет дифенохинонов:
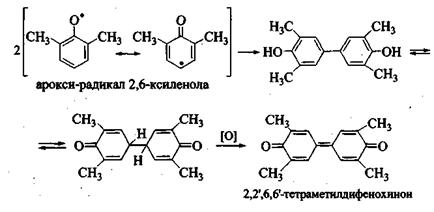
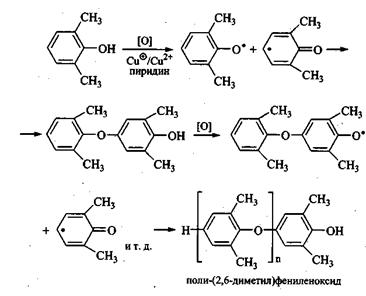 Последние, собственно, и ответственны за окрашивание (порозовение на первых порах) фенола при стоянии, так как легко образуются при контакте фенола с кислородом воздуха.
Последние, собственно, и ответственны за окрашивание (порозовение на первых порах) фенола при стоянии, так как легко образуются при контакте фенола с кислородом воздуха.
Однако наиболее интересен случай взаимодействия арокси-радикалов по типу «голова - хвост», в результате которого образуются полимеры класса ароматических полиэфиров.
Решение типовых задач
Задача 25.1.Составьте структурные формулы следующих органических соединений:
а) мета-крезол;
б) пара-аминофенол;
в) орто-бромфенол;
г) 2-хлорфенол;
д) 4-нитрофенол;
е) 2,5-диэтил-1-гидроксибензол;
ж) 2,4,6-тринитрофенол (пикриновая кислота);
з) этоксибензол (фенетол);
и) метанитрометоксибензол (мета-нитроанизол);
к) 2,4-динитро-6-гидрокситолуол;
л) феноксибензол;
м) фенол-2,4-дисульфокислота.
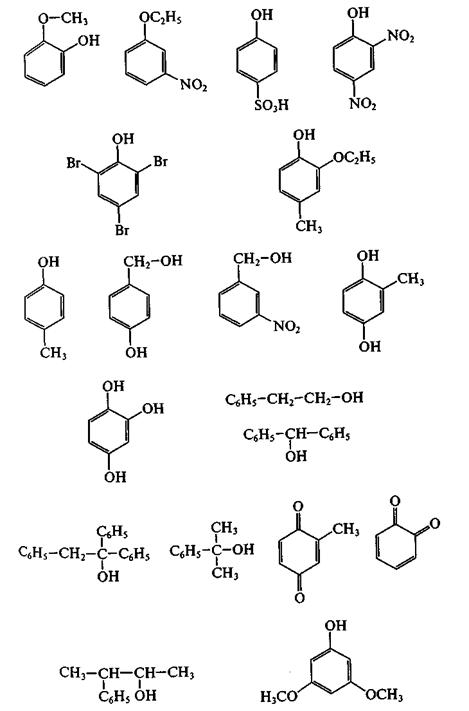
Задача 25.2.Назовите соединения, формулы которых приведены:
Задача 25.3.Объясните, чем обусловлены кислотные свойства фенола? Сравните константы кислотности фенола (рКа 10,0) и угольной кислоты (рКа 6,36). Какое из этих соединений является более сильной кислотой? Какое соединение образуется при пропускании оксида углерода (IV) через водный раствор фенолята натрия? Напишите уравнение реакции.
Задача 25.4. Расположите следующие вещества в порядке возрастания кислотных свойств: вода, уксусная кислота, фенол, бензиловый спирт, этанол, угольная кислота. Дайте объяснение с учетом электронных (индукционного и мезомерного) эффектов. Все ли из перечисленных соединений будут взаимодействовать с щелочами?
Задача 25.5. Объясните причины усиления кислотных свойств в ряду следующих соединений: фенол (рКа = 10,0), мета-нитрофенол (рКа = 8,39), пара-нитрофенол (рКа =7,15).
Задача 25.6. Какие из следующих соединений будут давать цветную реакцию с водным раствором хлорида железа (III):
а) бензиловый спирт;
б) пара-крезол;
в) 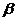 -фениловый спирт;
-фениловый спирт;
г) фенол?
Напишите уравнения реакций.
Задача 25.7.Напишите уравнения реакций и назовите соединения, образующиеся при взаимодействии фенолята натрия со следующими веществами:
а) 2-бромбутан;
б) изопропилхлорид;
в) метиловый эфир пара-толуолсульфокислоты;
г) изоамилбромид;
д) разбавленная серная кислота.
Задача 25.8.Рассмотрите механизм реакции алкилирования фенолов на примере взаимодействия:
а) фенола с метилиодидом в щелочной среде;
б) мета-крезола с хлористым бензилом в присутствии гидроксида натрия;
в) пара-крезолята натрия с бромистым аллилом;
г) фенолята калия с диметилсульфатом.