Лабораторно-практическое занятие № 17. «Моноциклические ароматические углеводороды: строение и свойства» (2ч)
Цель:сформировать знания о строении и реакционной способности моноциклических ароматических углеводородов.
Вопросы для обсуждения:
1. Арены, их реакционные центры и свойства
2. Реакции электрофильного замещения.
3. Реакции моноядерных аренов с нарушением ароматической системы.
4. Реакции боковых цепей в алкилбензолах.
5. Правила ориентации электрофильного заместителя в моно- и дизамещенное бензольное кольцо.
6. Правила ориентации электрофильного заместителя в дизамещенном бензольном кольце.
Материалы и примеры для самостоятельного изучения
Пример 1. На одной из стадий биосинтеза хлортетрациклина в грибах осуществляется хлорирование фенольного фрагмента молекулы. Смоделируйте эту реакцию in vitro на примере хлорирования фенола и объясните механизм реакции.
Решение. Заместители в ароматическом ядре существенно влияют на реакционную способность соединений в реакциях электрофильного замещения. Гидроксильная группа в молекуле фенола проявляет отрицательный индуктивный (-I) и положительный мезомерный (+M) эффекты. Преобладающим является + М- эффект.
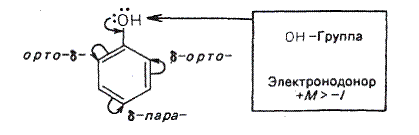
Гидроксильная группа, во-первых, оказывает активирующее влияние (электронная плотность в ароматическом кольце увеличивается). Так, если для хлорирования бензола необходим катализатор (кислота Льюиса), то хлорирование фенола проходит в мягких условиях без катализатора. Во-вторых, ОН-группа оказывает ориентируюшее влияние, т. е. направляет вновь входящие заместители в орто- и пара-положения (ориентант I рода). Поэтому в результате реакции образуются продукты орто- и пара-замещения.
Хлорирование фенола протекает по общему для ароматических соединений механизму электрофильного замещения с образованием о- и n-хлорфенолов.
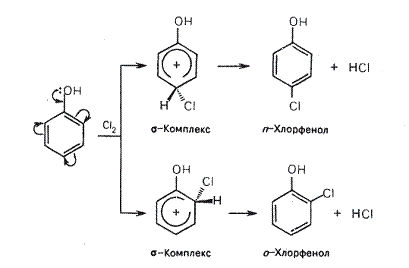
В процессе биосинтеза антибиотика хлортетрациклина галогенирование ароматического кольца осуществляется ферментативным путем. Особенностью такой реакции является ее избирательность: хлорирование происходит только в пара-положение к гидроксильной группе.
Пример 2. Окисление ароматических соединений является одной из часто встречающихся реакций в биотрансформации ксенобиотиков в живых организмах. Какие продукты образуются при биологическом окислении толуола и фенамина (1-фенилпропанамина-2)?
Решение. Незамещенное ароматическое кольцо устойчиво к окислению. Так, бензол окисляется только в жестких условиях с использованием сильных окислителей и катализаторов при высокой температуре. Для замещенных аренов характерно либо окисление боковых цепей, либо гидроксилирование ароматических колец. В первом случае окислению подвергается а-углеродный атом (соседний с ароматическим кольцом), и независимо от длины и разветвленности боковой цепи в процессе окисления образуются кислоты, в которых карбоксильные группы непосредственно связаны с ароматическим кольцом.
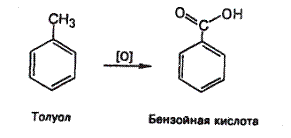
Окисление толуола in vivo и in vitro приводит к образованию бензойной кислоты. При синтезе ароматических кислот из гомологов бензола в качестве окислителя используют раствор перманганата калия в щелочной среде, либо раствор дихромата калия в кислой среде при нагревании.
Фенамин — сильный стимулятор ЦНС. Одной из основных реакций его метаболических превращений является гидроксилирование ароматического кольца в пара-положение к имеющемуся заместителю. Например, с мочой крыс выделяется свыше 50%от введенной дозы фенамина в виде пара-гидроксилированного метаболита.
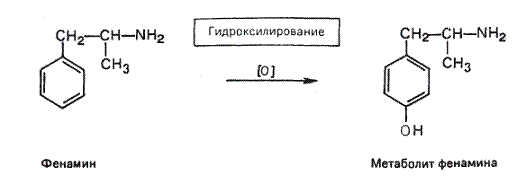
Ферментативное гидроксилирование ароматического кольца происходит под действием молекулярного кислорода с участием восстановителя — кофермента НАДФН.Промежуточным этапом реакции является образование ареноксидов, которые преобразуются в σ-комплекс с последующим восстановлением ароматичности кольца и получением гидроксилированного продукта.
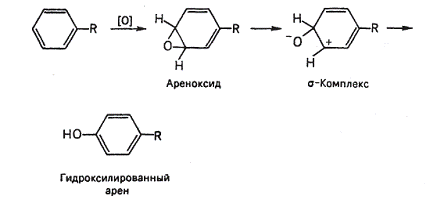
Окисление боковых цепей дренов и гидроксилирование ароматического кольца приводит к образованию более полярных соединений (кислот, фенолов), которые легче выводятся из организма. Таким образом, процесс окисления способствует снижению токсичности исходных ксенобиотиков. Так, толуол сравнительно быстро по сравнению с бензолом (ПДК бензола 5 мг/м3, толуола - 50 мг/м3
Задачи для самостоятельного решения
Номенклатура и изомерия
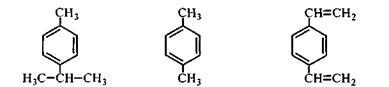
Задача 17.1. Дайте название следующим соединениям:
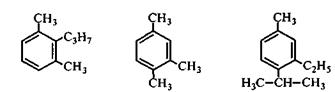
Задача 17.2. Напишите структурные формулы всех изомерных ароматических углеводородов состава C8H10 и назовите их по систематической номенклатуре
