Занятие 9. Химическая кинетика. Катализ. Химическое равновесие
Цель занятия:
Получить системные знания о закономерностях протекания химических и биохимических реакций, влияния различных факторов на скорости реакций.
Содержание занятия:
1. Обсуждение теоретических вопросов по теме.
2. Решение задач.
3. Выполнение демонстрационных работ.
Вопросы, предлагаемые для обсуждения на занятии:
1. Предмет химической кинетики.
2. Скорость химической реакции (средняя, истинная).
3. Зависимость скорости реакции от концентрации реагирующих веществ. Закон действия масс. Константа скорости реакции. Выражение закона действующих масс для гомогенных и гетерогенных систем. Примеры. Понятия о молекулярности и порядке реакции.
4. Зависимость скорости реакции от температуры. Теория активных соударений, активные молекулы, энергия активации, энергетический барьер реакции.
5. Катализ. Катализаторы. Основные признаки каталитических процессов. Примеры катализа. Свойства катализаторов. Теории гомогенного и гетерогенного катализа – теория промежуточных соединений и адсорбционная. Биологические катализаторы (ферменты), их особенности.
6. Радиационно-химические реакции (радиолиз воды), влияние их на биологические объекты.
7. Необратимые и обратимые химические реакции. Химическое равновесие. Константа равновесия.
8. Смещение (сдвиг) химического равновесия. Принцип Ле-Шателье–Брауна.
Лабораторная работа. Зависимость скорости реакции от концентрации.
Познакомьтесь с содержанием демонстрационных работ и оформите их результаты после выполнения по предлагаемой форме.
В трех пронумерованных стаканчиках готовят растворы различной концентрации:
1 стакан – 10 мл раствора Na2S2O3 + 20 мл Н2О, перемешать;
2 стакан – 20 мл раствора Na2S2O3 + 10 мл Н2О, перемешать;
3 стакан – 30 мл раствора Na2S2O3.
В стакан 1 вливают цилиндром 10 мл раствора H2SO4, перемешивают. В момент сливания растворов включают секундомер и отсчитывают время до появления легкого помутнения.
Аналогично поступают со стаканами 2 и 3.
Na2S2O3 + H2SO4= H2S2O3 + Na2SO4;
H2S2O3 = S↓ + H2SO3
Результаты сводят в таблицу и затем строят график зависимости υ—C, т. е. скорости реакции (ось ординат) от концентрации Na2S2O3 (ось абсцисс).
| № п/п | Объем, мл | Концентрация С= 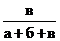 | Промежуток времени от начала отсчета до помутнения t, с | Скорость реакции υ = 1/t | ||
| a Na2S2O3 | б Н2О | в H2SO4 | ||||
| – |
Вывод:…
Контрольные вопросы и задачи
1. В системе 2 SO2(г) + О2(г) = 2 SO3(г) концентрацию оксида серы (IV) увеличили с 0.2 до 0.4 моль/л, а концентрацию кислорода с 0.4 до 1.2 моль/л. Во сколько раз возрастает скорость прямой реакции?
2. Во сколько раз следует увеличить давление, чтобы скорость образования NO2 по реакции 2NO(г) + О2(г) = 2NО2(г) возросла в 103 раз?
3. Разложение N2O при высоких температурах протекает по уравнению:
2 N2O(г) → 2 N2(г) + O2(г).
Константа скорости данной реакции равна 5∙10-4 моль/л при 900°С. Начальная концентрация N2О = 3.2 моль/л. Определите скорость реакции при заданной температуре в начальный момент времени и в тот момент, когда разложилось 25% N2O.
4. Скорость реакции увеличится в 4 раза при повышении температуры на 10°С. Во сколько раз возрастет скорость реакции при повышении температуры от 45°С до 75°С?
5. Допустимый срок хранения лекарственного вещества при комнатной температуре (20°С) 3 года. В процессе ускоренного определения его стабильности при 70°С, оно потеряло свои свойства через 40 суток. Соответствует ли лекарственное вещество предъявленным требованиям, если температурный коэффициент скорости реакции равен 2?
6. Реакция при температуре 20°С протекает за 12 мин 48 с. На сколько градусов необходимо повысить температуру системы для завершения этой реакции за 48 с (температурный коэффициент равен 2)?
7. Реакция идет по уравнению: N2(г) + O2(г) = 2 NO(г). Концентрации исходных веществ до начала реакции были (моль/л): [N2] = 0.049; [O2] = 0.01. Вычислите концентрацию этих веществ в момент, когда [NО] стала равной 0,005.
8. Реакция идет по уравнению: N2(г) + 3 Н2(г) = 2 NH3(г). Концентрации участвующих в ней веществ были (моль/л): [N2] = 0.8; [H2] = 1.5; [NH3] = 0.1. Вычислите концентрацию водорода и аммиака, когда [N2] стала равной
0.5 моль/л.
9. Вычислите равновесные концентрации Н2 и I2, если известно, что их начальные концентрации были равны 0.1 и 0.2 моль/л, а равновесная концентрация HI равна
0.1 моль/л. Вычислите константу равновесия в данных условиях.
10. В реакторе объемом 10 л содержится 5.6 г С2Н4, 150 г С2Н6 и водород. Константа равновесия реакции
Н2(г) + С2Н4(г) = С2Н6(г), выраженная через молярные концентрации, равна 50. Рассчитайте массу водорода.
Занятие 10. Химическая термодинамика.
Химическая кинетика и равновесие
Содержание занятия
1. Контрольная работа.
Вопросы для подготовки к контрольной работе
1. I и II начала (законы) термодинамики.
2. Закон Гесса и следствия из него.
3. Энтальпия химических процессов. Стандартные условия.
4. Термодинамические потенциалы (Гиббса, Гельмгольца). Энтропия.
5. Скорость гомогенных и гетерогенных химических реакций.
6. Закон действующих масс.
7. Зависимость скорости реакции от различных факторов (концентрации, температуры, давления).
8. Правило Вант-Гоффа, уравнение Аррениуса.
9. Гомогенный, гетерогенный катализ, теория их объясняющая.
10. Константа химического равновесия и факторы на нее влияющие.
11. Принцип Ле-Шателье–Брауна.
