Закон Авогадро: В равных объемах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул.
Из закона Авогадро вытекают два следствия:
1. Одинаковое число молекул любых газов при одинаковых условиях занимают одинаковый объем.
2. Относительная плотность одного газа по другому равна отношению их молярных масс.
Число Авогадро – число частиц в моле любого вещества; NA = 6,02∙1023 моль–1.
Молярный объем – объем моля любого газа при нормальных условиях(температура 273 К, давление 101,3 кПа); равен 22,4 л∙моль–1.
Молярная масса (M) – масса одного моля вещества, численно совпадающая с относительными массами атомов, ионов, молекул, радикалов и других частиц, выраженных в г∙моль–1.
Выполнить вопросы №4, №6, №7, №8 из теста.
Химические реакции.
Взаимодействие химических соединений записывается с помощью химических уравнений, отражающих материальный баланс всех реагирующих веществ. Это достигается с помощью стехиометрических коэффициентов перед формулами соединений:
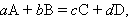 |
где A, B, C, D – реагирующие вещества; a, b, c, d – стехиометрические коэффициенты.
Можно выделить четыре основных типа химических реакций:
Соединения:
 |
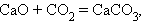 |
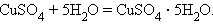 |
Замещения:
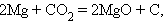 |
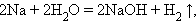 |
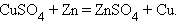 |
Разложения:
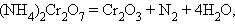 |
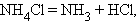 |
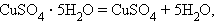 |
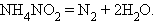 |
Обмена:
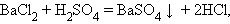 |
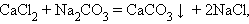 |
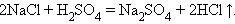 |
Реакции, сопровождающиеся изменением степени окисления всех или некоторых реагирующих веществ, называются окислительно-восстановительными. Из написанных выше реакций к таковым относятся:
 |
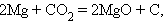 |
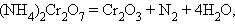 |
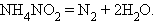 |
Способы получения солей.
 |
| Рисунок 1.5. Медный купорос, смешиваясь с водой, приобретает ярко-голубой оттенок. |
1. Взаимодействие простых веществ
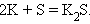 |
2. Взаимодействие оксидов
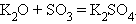 |
3. Взаимодействие кислот и оснований (нейтрализация)
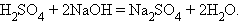 |
4. Взаимодействие соли и кислоты
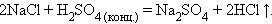 |
5. Взаимодействие соли и щелочи
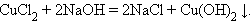 |
6. Взаимодействие двух солей (обменная реакция)
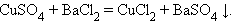 |
7. Взаимодействие оксида с кислотой
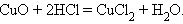 |
8. Замещение водорода
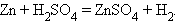 |
9. Замещение металла
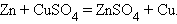 |
10. Термолиз кислых солей
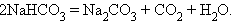 |
11. Взаимодействие двух солей (присоединение)
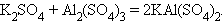 |
12. Взаимодействие двух солей (комплексообразование)
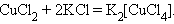 |
Способы получения оксидов.
 |
| Рисунок 1.6. Лесные пожары – один из источников углекислоты. |
1. Окисление простых и сложных веществ
| S + O2 = SO2; 2Mg + O2 = 2MgO, |
2.
| 2CuS +3O2 = 2CuO + 2SO2. |
3. Разложение гидроксидов
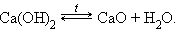 |
4. Разложение карбонатов и других солей
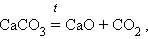 |
5.
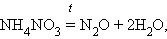 |
6.
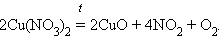 |
7. Взаимодействие металла с другим оксидом
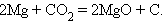 |
Способы получения кислот.
1. Взаимодействие кислотного оксида с водой
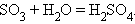 |
2. Вытеснение летучих кислот
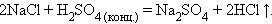 |
3. Взаимодействие соли и кислоты с образованием нерастворимой соли
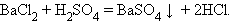 |
4. Взаимодействие водорода с элементом с образованием бескислородной кислоты
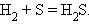 |
5. Комплексные кислоты
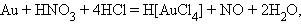 |
6.
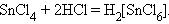 |
Способы получения оснований.
 |
| Рисунок 1.7. Несмотря на то, что натрий тяжелее воды, он «бегает» по ее поверхности, подталкиваемый пузырьками водорода, образующимися в результате реакции. В результате образуется гидроксид натрия. |
1. Взаимодействие металла с водой
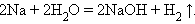 |
2. Взаимодействие оксида с водой
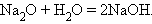 |
3. Разложение соли водой (гидролиз)
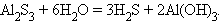 |
4. Взаимодействие соли и щелочи
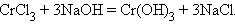 |

Тема 2: Электронное строение атомов.
Цель:
1. Понять как устроена электронная оболочка атома.
2. Уметь называть основные типы атомных орбиталей.
3. Уметь перечислять и характеризовать квантовые числа электрона.
4. Понять что такое энергетический уровень.
5. Уметь формулировать принцип Паули.
6. Знать какая последовательность энергетических уровней в многоэлектронных атомах.
7. Узнать чем определяется последовательность энергетических уровней в многоэлектронных атомах.
8. Узнать сколько энергетических уровней может быть при заданном l.
9. Уметь записывать все квантовые числа электронов в атоме бора.
10. Узнать сколько элементов относятся к главным подгруппам.
11. Научиться выделять из периодической таблицы все d-элементы.
12. Какие семейства элементов вам известны.
13. Понять, как меняется электроотрицательность в природе и подгруппе.
14. Узнать, как соотносятся между собой атомные и ионные радиусы.
15. Знать чем обусловлено f-сжатие и проявляется f-сжатие.
16. Научиться указывать все элементы, относящиеся к неметаллам.
